Clear Sky Science · zh
对MAPT V337M神经元的多组学表型分析揭示轴突发生和tau磷酸化的早期变化
这项研究为何关乎大脑健康
包括阿尔茨海默病和额颞叶痴呆在内的许多痴呆形式,都会在脑细胞内出现一种名为tau的蛋白质聚集。临床上可见异常tau与记忆和认知障碍高度相关,但tau究竟如何出问题——以及它对仍在发育的年轻神经元造成了什么影响——一直不清楚。此项研究聚焦于与额颞叶痴呆相关的一种遗传性tau突变,提出一个简单却至关重要的问题:在症状出现之前很久,神经元会发生什么变化?
更仔细地审视一种高风险的tau变体
研究者集中研究MAPT基因中的一个单一基因变异,称为V337M,该基因为tau提供蓝图。携带该突变的人几乎确定会在中年时期发展为额颞叶痴呆。为研究其早期影响,团队使用了人类诱导多能干细胞——将成体细胞重编程为类似胚胎细胞的状态——并在实验室中将其分化为神经元。他们比较了具有正常tau的神经元、携带一拷贝或两拷贝V337M突变的神经元,以及那些刻意降低tau水平的神经元。
同时追踪多条分子线索
科学家们没有只追踪一条信号,而是采用“多组学”视角:测量基因活性(RNA测序)、控制基因的DNA区域开放性(ATAC-seq),以及数千种蛋白及其化学标记(蛋白质组学与磷蛋白组学)。在这些不同层面上,一致的信息浮现出来。在携带V337M突变的神经元以及tau水平被降低的神经元中,最明显的变化涉及构建和塑造轴突的基因与蛋白质——轴突是将信号传递到其它细胞的长电缆样突起。这些变化在神经元发育的最初几周内就出现了,比细胞死亡或蛋白聚集等明显现象要早得多。
年轻神经元生长更短,而非更强
为检验这些分子变化是否确实影响细胞形态,团队在培养皿中观察了年轻神经元的生长。他们用荧光标记标记细胞膜,并在数天内追踪轴突在培养皿上的延伸。携带V337M突变的神经元和tau被降低的神经元都表现出明显较短的主轴突和较少的总延伸量,尽管小侧枝的数量并未显著改变。换言之,神经元的中心“导线”未能像应有的那样延伸到足够远的位置。这指向了tau在轴突延伸方面正常支持功能的丧失,而非一种明显致死的毒性效应。
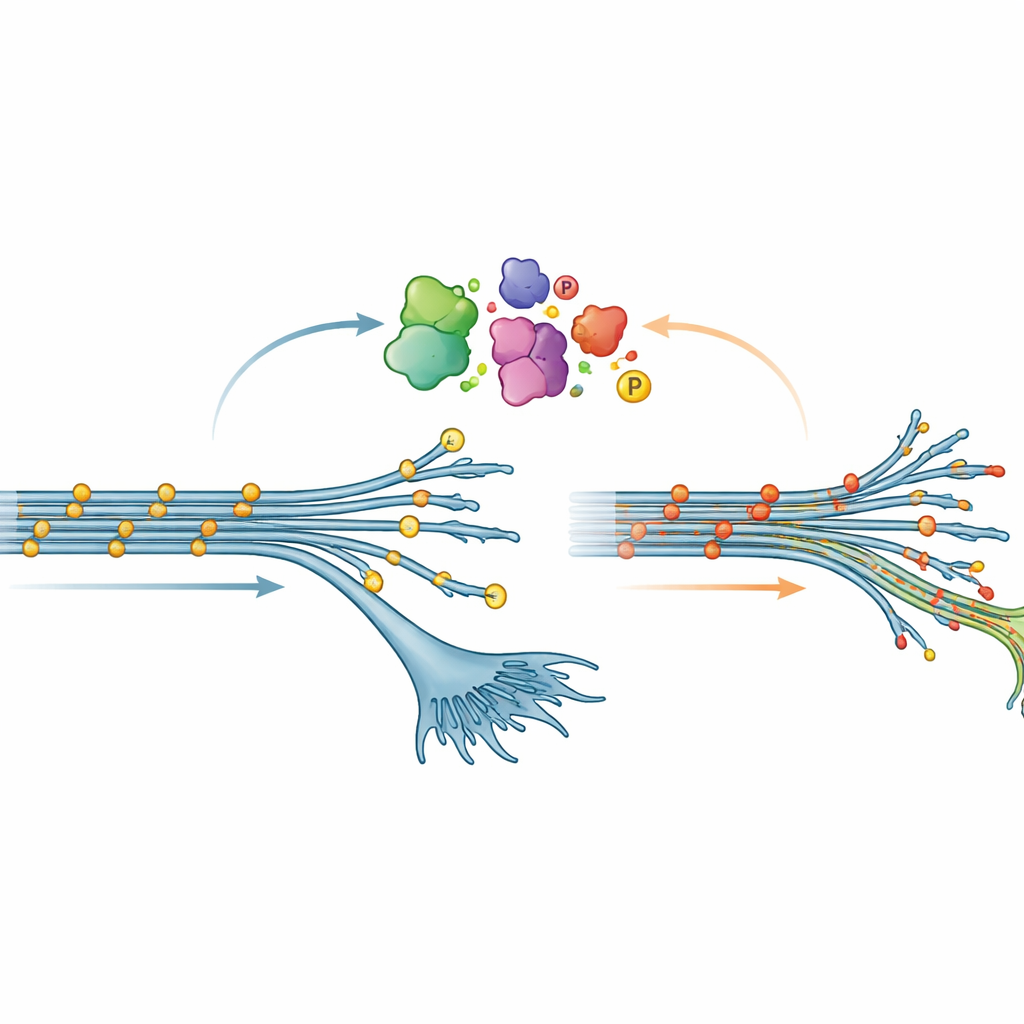
出人意料的tau化学修饰模式
其中一项最令人惊讶的发现涉及磷酸化——这是向蛋白质附加微小磷酸基团的一种常见化学修饰。在许多脑病中,tau会被大量磷酸化;这通常被视为促使tau形成缠结的有害改变。然而在此研究中,携带V337M突变的早期神经元显示出相反的模式:tau在许多位点上比正常水平的磷酸化更少。这种“低磷酸化”状态会随着神经元成熟逐渐减弱,但通过质谱和常规蛋白检测均被稳健地证实。当研究团队在自身tau被下调的神经元中过度表达V337M tau时,同样的低磷酸化状态再次出现,表明该突变本身改变了细胞内tau的修饰方式。
重塑轴突与tau的信号通路
为了解驱动这些变化的机制,研究者们寻找在V337M神经元中改变的信号通路——即一系列添加或去除磷酸基团的酶链。他们的磷蛋白组学数据指向参与神经元投射生长的蛋白以及特定的激酶家族,包括已知会影响神经突起生长的p38 MAP激酶通路。随后他们进行了大规模CRISPR筛选,通过上调或下调数千个基因来观察哪些基因会改变一种关键磷酸化形式的tau水平。许多命中基因与细胞内部骨架和轴突结构的组织有关,且若干p38通路成分在V337M神经元中特异性地影响tau磷酸化。这表明构建轴突的机械与调整tau化学状态的机制之间存在密切联系。
这对理解痴呆风险意味着什么
综合来看,这些发现表明V337M tau突变并非仅仅以经典意义上使tau更具毒性。相反,在生命早期它似乎削弱了tau对轴突生长的常规支持,并改变了tau的磷酸化方式,其影响与tau减少或丢失时的变化有重叠。发育期或青年早期的微妙连线缺陷——加上持续的tau化学状态变化——可能有助于解释为什么携带MAPT突变的人在明显痴呆出现的几十年前就显示出认知差异。这项工作强调,旨在广泛降低tau水平的治疗策略需要考虑tau在年轻健康神经元中的有益作用,并且谨慎调节而非简单抑制tau相关通路可能是长期保护大脑的关键。
引用: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
关键词: tau蛋白, 额颞叶痴呆, 轴突生长, 神经元发育, 蛋白质磷酸化