Clear Sky Science · es
Fenotipado multiómico de neuronas MAPT V337M revela cambios tempranos en la axonogénesis y la fosforilación de la tau
Por qué esta investigación importa para la salud cerebral
Muchas formas de demencia, incluida la enfermedad de Alzheimer y la demencia frontotemporal, implican acúmulos de una proteína llamada tau dentro de las neuronas. Los médicos observan que la tau anómala se correlaciona fuertemente con los problemas de memoria y pensamiento, pero no está claro cómo falla exactamente la tau ni qué efecto tiene sobre las neuronas jóvenes en desarrollo. Este estudio se centra en una mutación hereditaria de la tau vinculada a la demencia frontotemporal y plantea una pregunta simple pero crucial: ¿qué ocurre en las neuronas mucho antes de que aparezcan los síntomas?
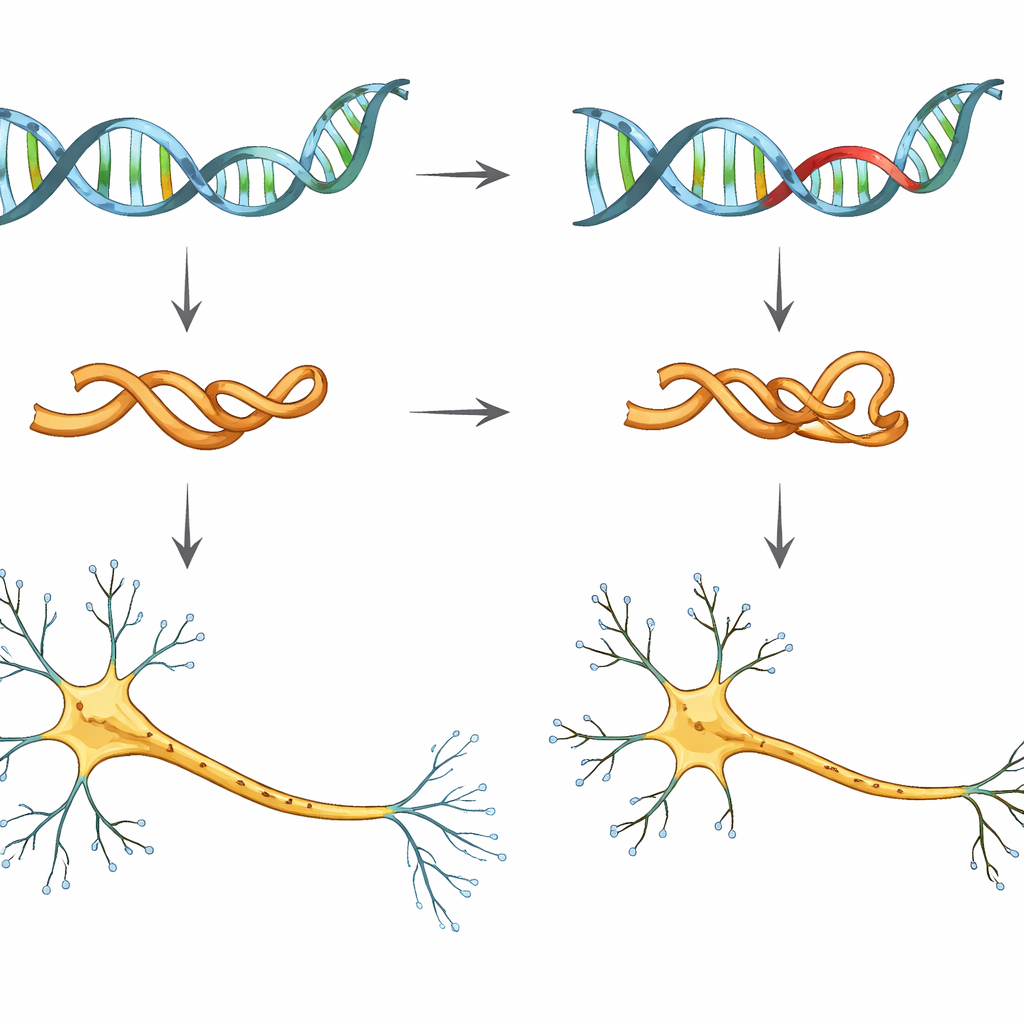
Una mirada más cercana a una versión arriesgada de la tau
Los investigadores se centraron en un único cambio genético, llamado V337M, en el gen MAPT, que codifica la tau. Las personas que portan esta mutación tienen casi la certeza de desarrollar demencia frontotemporal, a menudo en la mediana edad. Para estudiar sus efectos tempranos, el equipo utilizó células madre pluripotentes inducidas humanas—células adultas reprogramadas para comportarse como células embrionarias—y las diferenciaron en neuronas en el laboratorio. Compararon neuronas con tau normal, neuronas con una o dos copias de la mutación V337M y neuronas en las que los niveles de tau se redujeron deliberadamente.
Siguiendo muchas pistas moleculares a la vez
En lugar de seguir una sola señal, los científicos adoptaron una perspectiva “multiómica”: midieron la actividad génica (secuenciación de ARN), la accesibilidad de regiones del ADN que controlan genes (ATAC-seq) y miles de proteínas y sus etiquetas químicas (proteómica y fosfoproteómica). A través de estas capas, emergió un mensaje consistente. En las neuronas con la mutación V337M, y en las neuronas con tau reducida, los cambios más fuertes afectaron a genes y proteínas que construyen y moldean los axones—las largas proyecciones en forma de cable que llevan señales a otras células. Estos cambios aparecieron pronto, durante las primeras semanas de desarrollo neuronal, antes de cualquier signo evidente de muerte celular o agregación proteica.
Neuronas jóvenes crecen más cortas, no más fuertes
Para comprobar si estos cambios moleculares afectaban realmente la morfología celular, el equipo observó el crecimiento de neuronas jóvenes en platos de cultivo. Marcaron las membranas celulares con un marcador fluorescente y trazaron los axones durante varios días mientras se extendían por la placa. Las neuronas con la mutación V337M y las neuronas con tau reducida produjeron axones principales notablemente más cortos y menor crecimiento total, aunque el número de pequeñas ramas laterales no varió de forma drástica. En otras palabras, el “cable” central de la neurona no alcanzó la longitud esperada. Esto sugiere una pérdida del papel de soporte normal de la tau en la extensión axonal, más que un efecto tóxico evidente que mate a las células de forma directa.
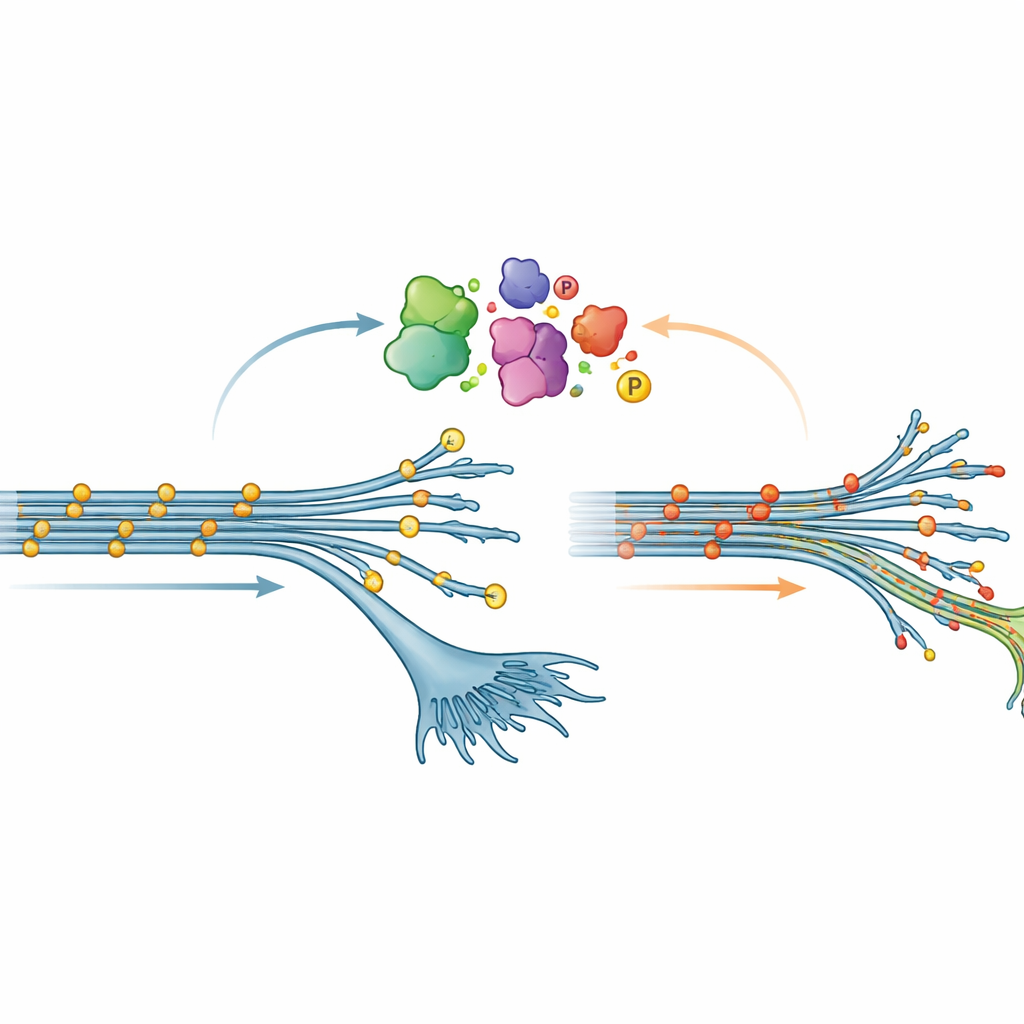
Un patrón inesperado en la química de la tau
Uno de los hallazgos más sorprendentes se refirió a la fosforilación, una modificación química común en la que pequeños grupos fosfato se añaden a las proteínas. En muchas enfermedades cerebrales, la tau se hiperfosforila; esto suele considerarse un cambio dañino que favorece la formación de ovillos. Aquí, sin embargo, las neuronas en fase temprana que llevaban la mutación V337M mostraron el patrón opuesto: la tau estaba menos fosforilada en muchos sitios respecto a lo normal. Esta “hipofosforilación” se atenuó gradualmente a medida que las neuronas maduraban, pero fue lo suficientemente robusta como para confirmarse tanto por espectrometría de masas como por ensayos proteicos estándar. Cuando el equipo sobreprodujo artificialmente tau V337M en neuronas cuya tau endógena había sido reducida, reapareció el mismo estado de baja fosforilación, lo que sugiere que la mutación en sí modifica cómo se altera químicamente la tau dentro de las células.
Vías de señalización que remodelan axones y la tau
Para entender qué impulsa estos cambios, los investigadores buscaron vías de señalización—cadenas de enzimas que añaden o eliminan grupos fosfato—alteradas en neuronas V337M. Sus datos fosfoproteómicos señalaron proteínas implicadas en el crecimiento de proyecciones neuronales y a familias específicas de quinasas, incluida la vía de las quinasas p38 MAP, conocida por influir en el crecimiento de neuritas. Luego realizaron grandes cribados CRISPR, activando o reprimiendo miles de genes para ver cuáles modulaban el nivel de una forma fosforilada clave de la tau. Muchos de los genes identificados organizan el citoesqueleto celular y la estructura axonal, y varios componentes de la vía p38 afectaron la fosforilación de la tau específicamente en neuronas V337M. Esto sugiere un vínculo íntimo entre la maquinaria que construye los axones y la que ajusta el estado químico de la tau.
Qué significa esto para entender el riesgo de demencia
En conjunto, los hallazgos sugieren que la mutación V337M en la tau no la hace simplemente más tóxica en el sentido clásico. En cambio, en fases muy tempranas parece atenuar el apoyo habitual de la tau al crecimiento axonal y altera cómo se fosforila la tau, de maneras que se solapan con lo que ocurre cuando la tau se reduce o se pierde. Defectos sutiles en el cableado durante el desarrollo o la edad adulta temprana—combinados con cambios continuos en la química de la tau—podrían ayudar a explicar por qué las personas con mutaciones en MAPT muestran diferencias cognitivas décadas antes de que surja una demencia clara. Este trabajo subraya que las terapias destinadas a reducir ampliamente la tau podrían necesitar considerar los roles beneficiosos de la tau en neuronas jóvenes y sanas, y que afinar con cuidado, en lugar de bloquear de forma absoluta, las vías relacionadas con la tau podría ser clave para proteger el cerebro a lo largo de la vida.
Cita: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Palabras clave: proteína tau, demencia frontotemporal, crecimiento axonal, desarrollo neuronal