Clear Sky Science · fr
Phénotypage multi-omique de neurones portant MAPT V337M révèle des changements précoces dans l’axonogenèse et la phosphorylation de la protéine tau
Pourquoi cette recherche compte pour la santé cérébrale
De nombreuses formes de démence, y compris la maladie d’Alzheimer et la démence frontotemporale, impliquent des agrégats d’une protéine nommée tau à l’intérieur des cellules cérébrales. Les cliniciens observent que des anomalies de la tau sont fortement corrélées aux troubles de la mémoire et des fonctions cognitives, mais la manière précise dont la tau dysfonctionne — et son impact sur les neurones jeunes en cours de développement — restait floue. Cette étude se concentre sur une mutation héréditaire de la tau liée à la démence frontotemporale et pose une question simple mais cruciale : que deviennent les neurones bien avant l’apparition des symptômes ?
Un examen approfondi d’une version à risque de la tau
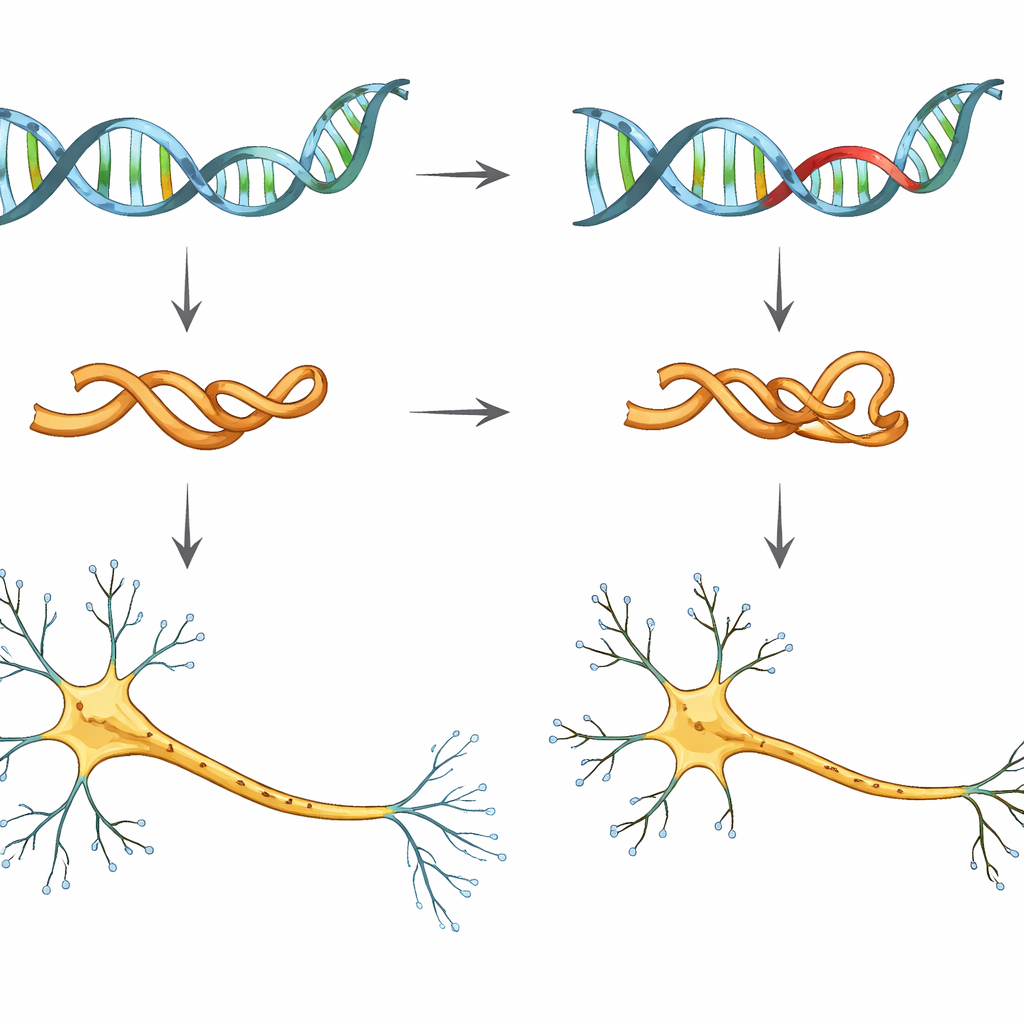
Les chercheurs se sont focalisés sur un seul changement génétique, appelé V337M, dans le gène MAPT, qui code la protéine tau. Les personnes porteuses de cette mutation ont presque toutes la probabilité de développer une démence frontotemporale, souvent à l’âge moyen. Pour étudier ses effets précoces, l’équipe a utilisé des cellules souches pluripotentes induites humaines — des cellules adultes reprogrammées pour retrouver un état embryonnaire — et les a différenciées en neurones en laboratoire. Ils ont comparé des neurones portant la tau normale, des neurones avec une ou deux copies de la mutation V337M, et des neurones dont le niveau de tau avait été intentionnellement réduit.
Suivre simultanément de nombreux indices moléculaires
Plutôt que de suivre un seul signal, les scientifiques ont adopté une approche « multi-omique » : ils ont mesuré l’activité génique (séquençage de l’ARN), l’accessibilité des régions d’ADN qui contrôlent les gènes (ATAC-seq), et des milliers de protéines et leurs marques chimiques (protéomique et phosphoprotéomique). À travers ces différentes couches, un message cohérent est apparu. Dans les neurones porteurs de la mutation V337M, et dans les neurones où la tau était diminuée, les changements les plus marqués concernaient les gènes et protéines impliqués dans la formation et la structuration des axones — ces longues extensions en forme de câble qui transmettent les signaux aux autres cellules. Ces altérations se manifestaient tôt, dès les premières semaines du développement neuronal, avant tout signe évident de mort cellulaire ou d’agrégation protéique.
Les neurones jeunes grandissent moins loin, pas mieux
Pour déterminer si ces modifications moléculaires affectaient réellement la morphologie cellulaire, l’équipe a observé la croissance de jeunes neurones en culture. Ils ont marqué les membranes cellulaires avec un traceur fluorescent et suivi l’extension des axones sur plusieurs jours. Les neurones portant la mutation V337M et ceux avec une tau réduite présentaient des axones principaux nettement plus courts et un moindre étalement total, même si le nombre de petites ramifications latérales n’était pas fortement modifié. En d’autres termes, le « fil » central du neurone n’atteignait pas la même distance qu’attendu. Cela suggère une perte du rôle habituel de la tau dans le soutien de l’extension axonale, plutôt qu’un effet toxique évident entraînant directement la mort cellulaire.
Un profil chimique de la tau inattendu
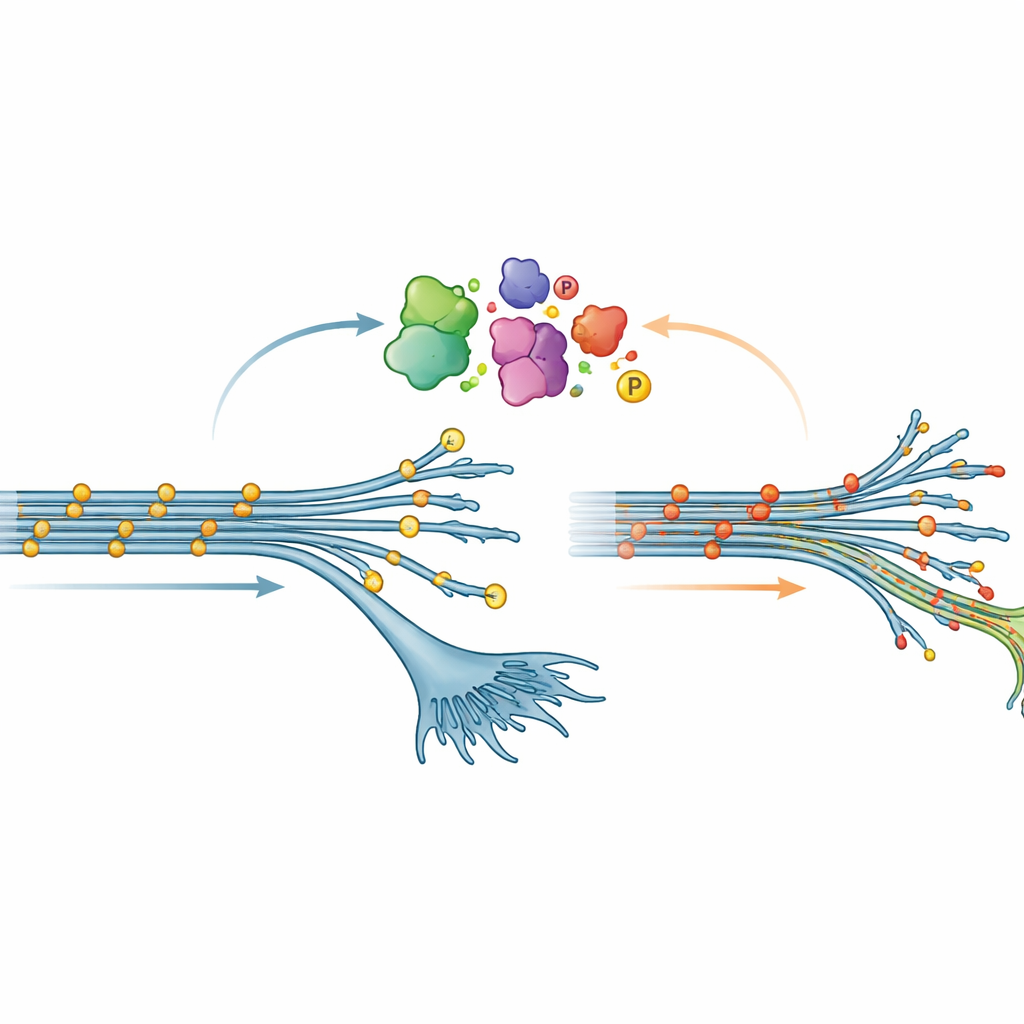
La découverte la plus surprenante concernait la phosphorylation, une modification chimique courante par laquelle de petits groupes phosphate sont ajoutés aux protéines. Dans de nombreuses maladies cérébrales, la tau devient fortement phosphorylée ; cela est souvent considéré comme un changement délétère favorisant la formation d’enchevêtrements de tau. Ici, toutefois, les neurones en stade précoce porteurs de la mutation V337M montraient le schéma inverse : la tau était moins phosphorylée en de nombreux sites par rapport à la normale. Cette « hypophosphorylation » s’atténuait progressivement à mesure que les neurones mûrissaient, mais elle était suffisamment robuste pour être confirmée par spectrométrie de masse et par des tests protéiques classiques. Lorsque l’équipe a surproduit artificiellement la tau V337M dans des neurones dont la tau endogène avait été réduite, le même état de faible phosphorylation réapparaissait, suggérant que la mutation elle-même modifie la manière dont la tau est modifiée à l’intérieur des cellules.
Voies de signalisation qui restructurent les axones et la tau
Pour comprendre ce qui pilote ces changements, les chercheurs ont recherché des voies de signalisation — des cascades d’enzymes ajoutant ou retirant des groupes phosphate — altérées dans les neurones V337M. Leurs données phosphoprotéomiques ont mis en évidence des protéines impliquées dans la croissance des projections neuronales et des familles de kinases spécifiques, y compris la voie p38 MAP kinase, connue pour influencer la croissance des neurites. Ils ont ensuite réalisé des criblages CRISPR à grande échelle, modulant des milliers de gènes pour identifier ceux qui changeaient le niveau d’une forme phosphorylée clé de la tau. De nombreux résultats concernaient des gènes organisant le cytosquelette cellulaire et la structure axonale, et plusieurs composants de la voie p38 modifiaient la phosphorylation de la tau spécifiquement dans les neurones V337M. Cela suggère un lien étroit entre la machinerie qui construit les axones et celle qui règle l’état chimique de la tau.
Que signifie cela pour la compréhension du risque de démence
Ensemble, ces résultats indiquent que la mutation V337M de la tau ne rend pas simplement la protéine plus toxique au sens classique. Au contraire, très tôt dans la vie elle semble atténuer le rôle habituel de la tau dans la croissance axonale et modifier sa phosphorylation, de manière qui recoupe ce qui se produit lorsque la tau est réduite ou perdue. Des défauts subtils du câblage lors du développement ou au début de l’âge adulte — associés à des modifications persistantes de la chimie de la tau — pourraient aider à expliquer pourquoi les porteurs de mutations MAPT présentent des différences cognitives des décennies avant l’apparition d’une démence nette. Ce travail souligne que des thérapies visant à réduire globalement la tau devraient prendre en compte les rôles utiles de la tau dans les neurones jeunes et sains, et que régler finement, plutôt que simplement bloquer, les voies liées à la tau pourrait être la clé pour protéger le cerveau sur l’ensemble de la vie.
Citation: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Mots-clés: protéine tau, démence frontotemporale, croissance axonale, développement neuronal, phosphorylation des protéines