Clear Sky Science · ru
Мультиомное фенотипирование нейронов с мутацией MAPT V337M выявляет ранние изменения аксонообразования и фосфорилирования тау
Почему это исследование важно для здоровья мозга
Во многих формах деменции, включая болезнь Альцгеймера и фронтотемпоральную деменцию, внутри нейронов образуются скопления белка под названием тау. Врачи хорошо видят, что аномальный тау тесно связан с нарушениями памяти и мышления, но то, как именно тау начинает работать неправильно — и что это делает с молодыми, ещё развивающимися нервными клетками — оставалось неясным. В этом исследовании авторы подробно изучают наследственную мутацию тау, связанную с фронтотемпоральной деменцией, и задают простой, но важный вопрос: что происходит с нейронами задолго до появления симптомов?
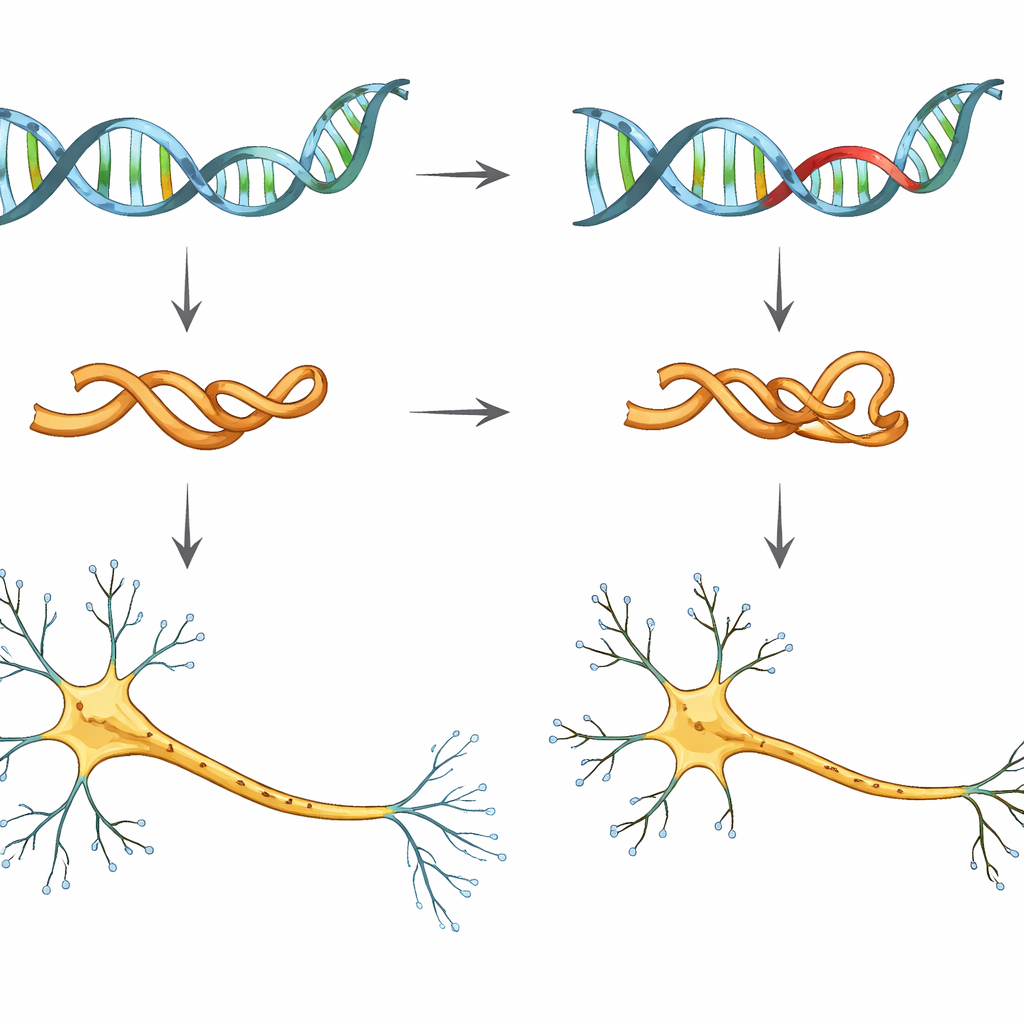
Более пристальный взгляд на рискованную версию тау
Исследователи сосредоточились на одной генетической замене, называемой V337M, в гене MAPT, который кодирует тау. Люди, несущие эту мутацию, почти наверняка разовьют фронтотемпоральную деменцию, часто в среднем возрасте. Чтобы изучить её ранние эффекты, команда использовала индуцированные плюрипотентные стволовые клетки человека — взрослые клетки, перепрограммированные на поведение, похожее на эмбриональные — и в лаборатории превратила их в нейроны. Они сравнили нейроны с нормальным тау, нейроны с одной или двумя копиями мутации V337M и нейроны, в которых уровни тау сознательно снижали.
Одновременное отслеживание множества молекулярных следов
Вместо того чтобы изучать только один показатель, учёные применили «мультиомный» подход: они измеряли активность генов (РНК-секвенирование), доступность участков ДНК, контролирующих гены (ATAC-seq), а также тысячи белков и их химические метки (протеомика и фосфопротеомика). На разных уровнях последовательно проявлялась одна и та же картина. В нейронах с мутацией V337M и в нейронах с пониженным уровнем тау наиболее заметные изменения касались генов и белков, которые строят и формируют аксоны — длинные, кабелеподобные отростки, по которым сигналы передаются другим клеткам. Эти изменения появлялись рано, в первые недели развития нейронов, задолго до каких‑либо явных признаков гибели клеток или образования белковых агрегатов.
Молодые нейроны растут короче, не сильнее
Чтобы проверить, влияют ли эти молекулярные изменения на форму клеток, команда наблюдала за ростом молодых нейронов в культурах. Они меченили клеточные мембраны флуоресцентным маркером и отслеживали аксоны в течение нескольких дней, пока они тянулись по пластине. Нейроны с мутацией V337M и нейроны с пониженным уровнем тау давали заметно более короткие основные аксоны и меньше общего роста отростков, хотя число мелких боковых ветвей существенно не менялось. Иными словами, центральный «провод» нейрона не достигал нужной длины. Это указывает на утрату обычной поддерживающей роли тау в удлинении аксона, а не на явный токсический эффект, который бы напрямую убивал клетки.
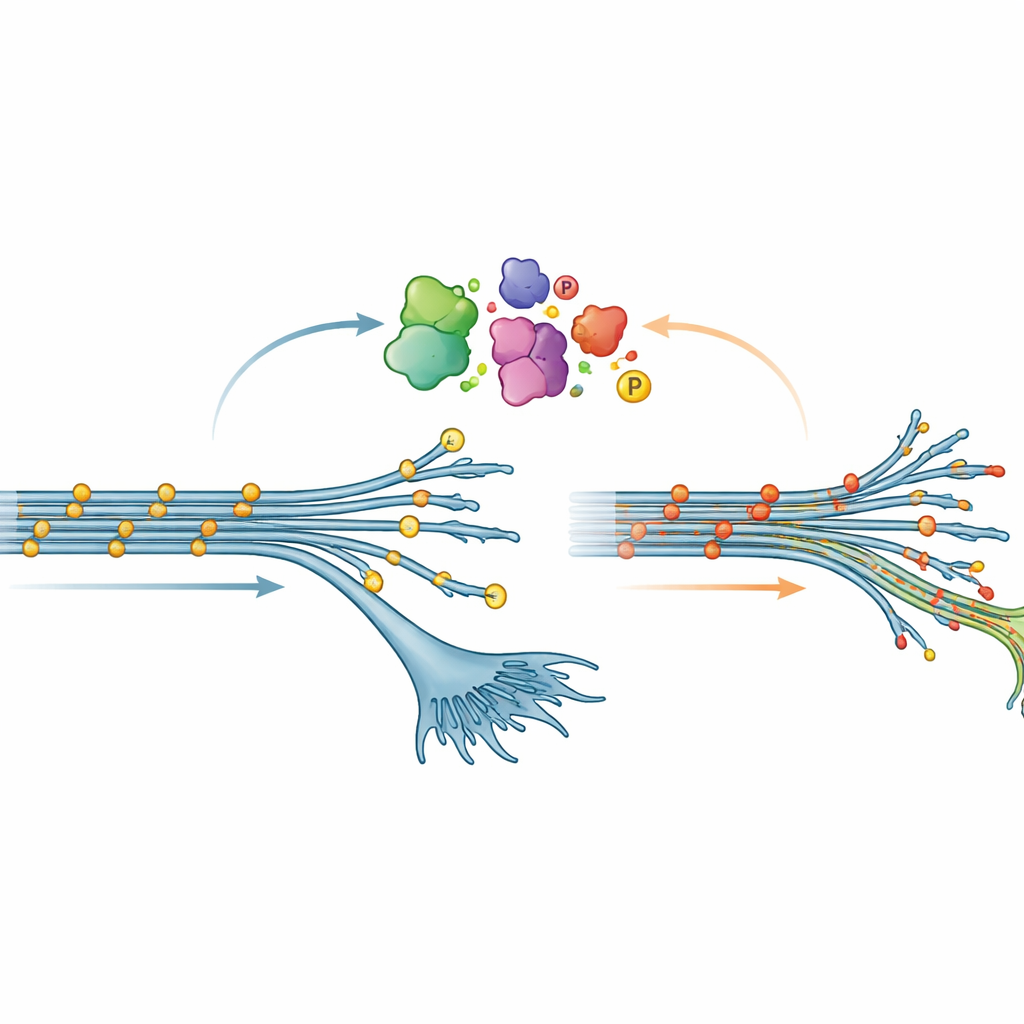
Неожиданная картина химии тау
Одним из самых удивительных открытий было фосфорилирование — распространённая химическая модификация, при которой к белкам прикрепляются фосфатные группы. При многих заболеваний мозга тау становится сильно фосфорилированным; это часто считают вредным изменением, способствующим образованию сплетений тау. Здесь, однако, в нейронах на ранних стадиях, несущих мутацию V337M, наблюдался противоположный эффект: тау был менее фосфорилирован по множеству сайтов, чем в норме. Эта «гипофосфорилизация» постепенно ослабевала по мере созревания нейронов, но была достаточно выраженной, чтобы её подтвердили и масс‑спектрометрия, и стандартные белковые тесты. Когда команда искусственно переставляла экспрессию V337M тау в нейронах, у которых собственный тау был снижен, та же низкая степень фосфорилирования повторялась, что говорит о том, что сама мутация изменяет способы модификации тау внутри клетки.
Сигнальные пути, перестраивающие аксоны и тау
Чтобы понять, что вызывает эти изменения, исследователи искали сигнальные пути — цепочки ферментов, добавляющих или убирающих фосфатные группы — изменённые в нейронах с V337M. Данные фосфопротеомики указывали на белки, вовлечённые в рост нейронных отростков, и на конкретные семейства киназ, включая путь p38 MAP киназы, известный влиянием на рост нейритов. Затем они провели масштабные CRISPR‑скрины, поднимая или подавляя тысячи генов, чтобы увидеть, какие из них меняют уровень ключевой фосфорилированной формы тау. Многие «попадания» оказались генами, организующими внутриклеточный скелет и структуру аксона, а несколько компонентов пусти p38 специфически влияли на фосфорилирование тау в нейронах с V337M. Это указывает на тесную связь между механизмами, строящими аксоны, и механизмами, регулирующими химическое состояние тау.
Что это значит для понимания риска деменции
В совокупности результаты предполагают, что мутация V337M в тау не просто делает тау более токсичным в классическом смысле. Вместо этого на очень ранних этапах она, похоже, ослабляет обычную поддержку тау в росте аксона и меняет его фосфорилирование — в аспектах, пересекающихся с тем, что происходит при снижении или утрате тау. Тонкие дефекты проводки во время развития или в ранней взрослой жизни в сочетании с продолжающимися изменениями в химии тау могут помочь объяснить, почему носители мутаций MAPT демонстрируют когнитивные отличия за десятилетия до явной деменции. Эта работа подчёркивает, что терапия, направленная на широкое снижение тау, должна учитывать полезные роли тау в молодых и здоровых нейронах, и что аккуратная настройка, а не просто блокирование тау‑связанных путей, может оказаться ключом к защите мозга на протяжении всей жизни.
Цитирование: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Ключевые слова: белок тау, фронтотемпоральная деменция, рост аксона, развитие нейронов, фосфорилирование белков