Clear Sky Science · it
Fenotipizzazione multi-omica di neuroni MAPT V337M rivela cambiamenti precoci nell’assonogenesi e nella fosforilazione della tau
Perché questa ricerca è importante per la salute del cervello
Molte forme di demenza, compresi il morbo di Alzheimer e la demenza frontotemporale, implicano aggregati di una proteina chiamata tau all’interno delle cellule cerebrali. I medici osservano che una tau anomala è fortemente correlata ai disturbi della memoria e del pensiero, ma il modo esatto in cui la tau si altera — e cosa provoca nelle cellule nervose giovani e ancora in sviluppo — è rimasto poco chiaro. Questo studio si concentra su una mutazione ereditaria della tau legata alla demenza frontotemporale e pone una domanda semplice ma cruciale: cosa succede ai neuroni molto prima della comparsa dei sintomi?
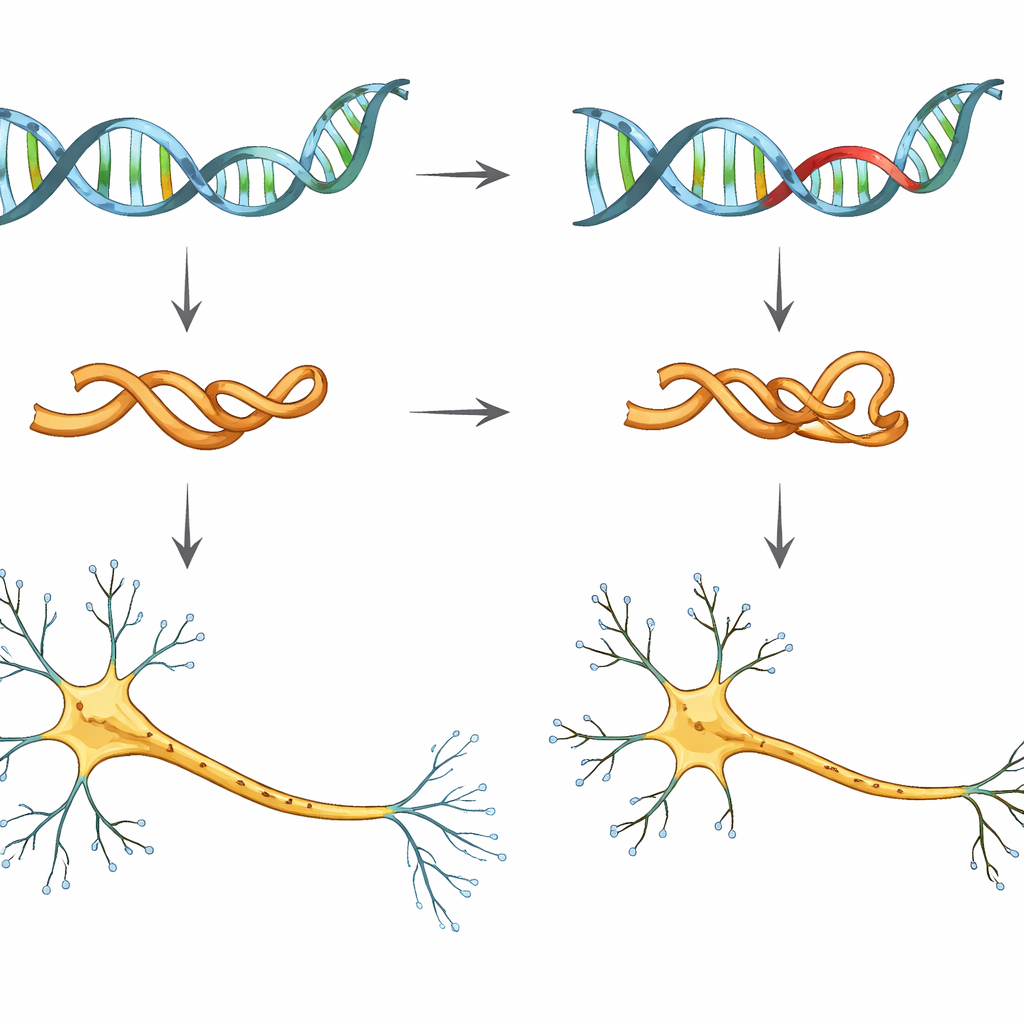
Uno sguardo ravvicinato a una versione rischiosa della tau
I ricercatori si sono concentrati su una singola variazione genetica, chiamata V337M, nel gene MAPT, che contiene il progetto della tau. Le persone portatrici di questa mutazione sono quasi certe di sviluppare demenza frontotemporale, spesso in età adulta di mezza età. Per studiarne gli effetti precoci, il gruppo ha usato cellule staminali pluripotenti indotte umane — cellule adulte riprogrammate per comportarsi come cellule embrionali — e le ha differenziate in neuroni in laboratorio. Hanno confrontato neuroni con tau normale, neuroni portatori di una o due copie della mutazione V337M e neuroni in cui i livelli di tau erano deliberatamente ridotti.
Seguire molte tracce molecolari contemporaneamente
Invece di monitorare un singolo segnale, gli scienziati hanno adottato una prospettiva «multi-omica»: hanno misurato l’attività genica (sequenziamento dell’RNA), l’accessibilità delle regioni di DNA che regolano i geni (ATAC-seq) e migliaia di proteine e dei loro segni chimici (proteomica e fosfoproteomica). Attraverso questi diversi livelli, è emesso un messaggio coerente. Nei neuroni con la mutazione V337M, e nei neuroni in cui la tau era ridotta, i cambiamenti più marcati riguardavano geni e proteine che costruiscono e modellano gli assoni — le lunghe proiezioni simili a cavi che trasmettono segnali ad altre cellule. Questi cambiamenti sono comparsi precocemente, nelle prime settimane di sviluppo neuronale, prima di qualsiasi segno evidente di morte cellulare o di aggregazione proteica.
I neuroni giovani crescono più corti, non più robusti
Per verificare se questi cambiamenti molecolari influenzassero effettivamente la forma cellulare, il team ha osservato la crescita di neuroni giovani in piastre di coltura. Hanno marcato le membrane cellulari con un indicatore fluorescente e tracciato gli assoni per diversi giorni mentre si estendevano sulla superficie. I neuroni con la mutazione V337M e i neuroni con tau ridotta hanno entrambi prodotto assoni principali visibilmente più corti e una minore crescita totale, anche se il numero di piccoli rami laterali non è cambiato in modo drastico. In altre parole, il «cavo» centrale del neurone non raggiungeva la distanza attesa. Ciò indica una perdita del ruolo di supporto normale della tau nell’estensione assonale, piuttosto che un evidente effetto tossico che uccide le cellule in modo diretto.
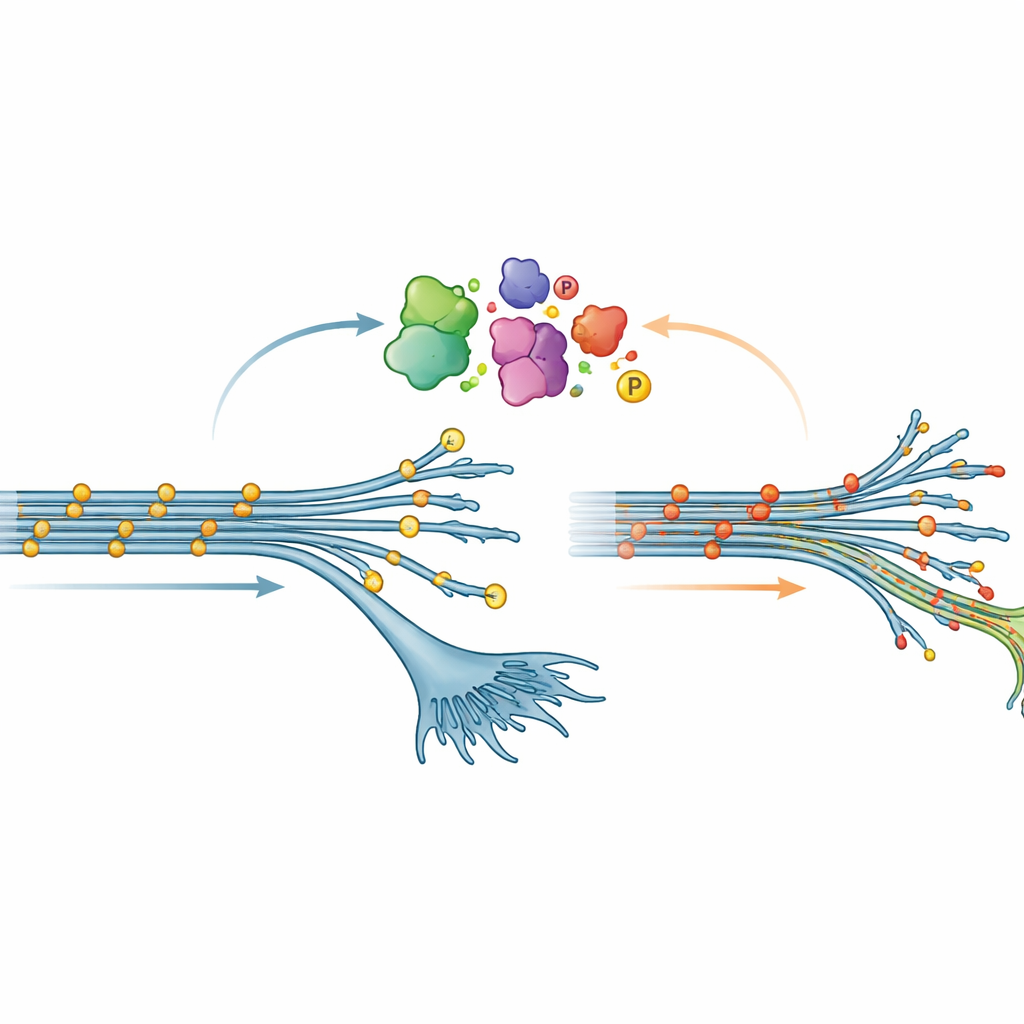
Un pattern inatteso nella chimica della tau
Una delle scoperte più sorprendenti riguardava la fosforilazione, una modifica chimica comune in cui minuscoli gruppi fosfato si legano alle proteine. In molte malattie cerebrali, la tau diventa fortemente fosforilata; questo è spesso visto come un cambiamento dannoso che favorisce la formazione di grovigli. Qui, tuttavia, i neuroni in fase iniziale portatori della mutazione V337M hanno mostrato il quadro opposto: la tau era meno fosforilata in molti siti rispetto al normale. Questa «ipofosforilazione» è svanita gradualmente con la maturazione dei neuroni, ma è stata sufficientemente robusta da essere confermata sia dalla spettrometria di massa sia da test proteici standard. Quando il team ha sovraespresso artificialmente la tau V337M in neuroni il cui tau endogena era stata abbassata, lo stesso stato a bassa fosforilazione è riapparso, suggerendo che la mutazione di per sé rimodella come la tau viene modificata all’interno delle cellule.
Vie di segnalazione che rimodellano assoni e tau
Per comprendere cosa guida questi cambiamenti, i ricercatori hanno cercato vie di segnalazione — catene di enzimi che aggiungono o rimuovono gruppi fosfato — alterate nei neuroni V337M. I dati di fosfoproteomica hanno indicato proteine coinvolte nella crescita delle proiezioni neuronali e famiglie di chinasi specifiche, inclusa la via della p38 MAP chinasi, nota per influenzare la crescita dei neuriti. Hanno quindi eseguito grandi screening CRISPR, modulando migliaia di geni per vedere quali alteravano il livello di una forma fosforilata chiave della tau. Molti risultati sono stati geni che organizzano lo scheletro interno della cellula e la struttura assonale, e diversi componenti della via p38 hanno influenzato la fosforilazione della tau specificamente nei neuroni V337M. Questo suggerisce un legame stretto tra la macchina che costruisce gli assoni e quella che regola lo stato chimico della tau.
Cosa significa per comprendere il rischio di demenza
Messi insieme, i risultati suggeriscono che la mutazione V337M della tau non si limita a rendere la proteina più tossica nel senso classico. Piuttosto, nelle fasi molto precoci della vita sembra attenuare il supporto normale della tau per la crescita assonale e altera come la tau viene fosforilata, in modi che si sovrappongono a quanto avviene quando la tau è ridotta o persa. Difetti sottili nel cablaggio durante lo sviluppo o la prima età adulta — combinati con cambiamenti persistenti nella chimica della tau — potrebbero aiutare a spiegare perché le persone portatrici di mutazioni MAPT mostrano differenze cognitive decenni prima che emerga una demenza chiara. Questo lavoro sottolinea che terapie mirate a ridurre in modo ampio la tau potrebbero dover considerare i ruoli utili della tau nei neuroni giovani e sani, e che una regolazione attenta, piuttosto che un blocco netto, delle vie legate alla tau potrebbe essere la chiave per proteggere il cervello nel corso della vita.
Citazione: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Parole chiave: proteina tau, demenza frontotemporale, crescita dell’assone, sviluppo neuronale, fosforilazione delle proteine