Clear Sky Science · sv
Multi-omisk fenotypning av MAPT V337M-neuroner avslöjar tidiga förändringar i axonogenes och tau-fosforylering
Varför denna forskning spelar roll för hjärnhälsa
Många former av demens, inklusive Alzheimers sjukdom och frontotemporal demens, innebär ansamlingar av ett protein kallat tau inne i hjärnceller. Kliniska fynd visar att onormal tau starkt korrelerar med minnes- och tankeproblem, men exakt hur tau går fel — och vad det gör mot unga, fortfarande utvecklande nervceller — har varit oklart. Denna studie zoomar in på en ärftlig tau-mutation kopplad till frontotemporal demens och ställer en enkel men avgörande fråga: vad händer med neuroner långt innan symtomen uppträder?
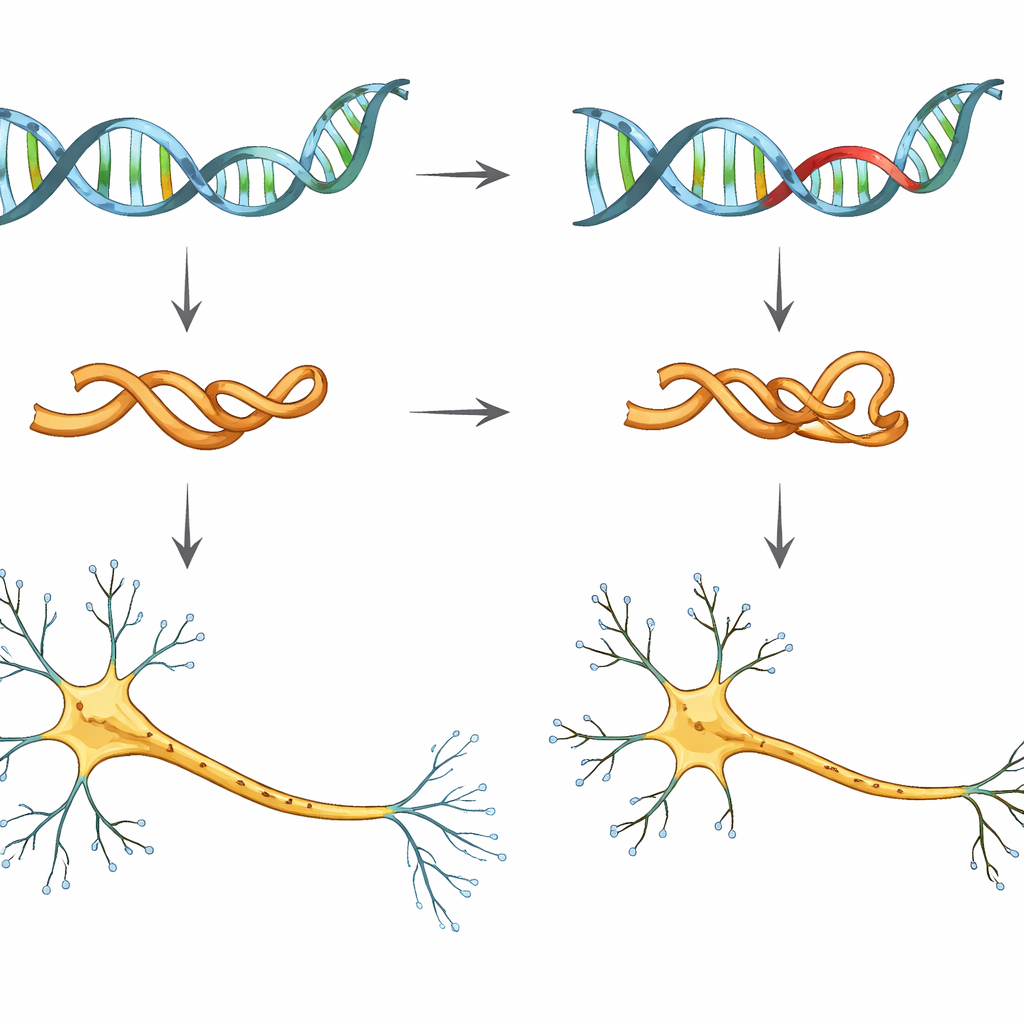
Närmare titt på en riskfylld variant av tau
Forskarna fokuserade på en enda genetisk förändring, kallad V337M, i MAPT-genen som ger ritningen för tau. Personer som bär denna mutation har nästan säker utveckling av frontotemporal demens, ofta i medelåldern. För att studera dess tidiga effekter använde teamet humana inducerade pluripotenta stamceller — vuxenceller omprogrammerade att bete sig som embryonala celler — och omvandlade dem i laboratoriet till neuroner. De jämförde neuroner med normal tau, neuroner som bar en eller två kopior av V337M-mutation, och neuroner där tau-nivåerna medvetet sänkts.
Följer många molekylära ledtrådar samtidigt
I stället för att följa bara en signal tog forskarna ett "multi-omiskt" grepp: de mätte genaktivitet (RNA-sekvensering), öppenheten i DNA-regioner som styr gener (ATAC-seq), och tusentals proteiner och deras kemiska märkningar (proteomik och fosfoproteomik). Över dessa olika nivåer framträdde ett konsekvent budskap. I neuroner med V337M-mutation, och i neuroner där tau var sänkt, rörde de starkaste förändringarna gener och proteiner som bygger och formar axoner — de långa, kabel-liknande utlöparna som för signaler till andra celler. Dessa förändringar uppträdde tidigt, inom de första veckorna av neuronal utveckling, innan några tydliga tecken på celldöd eller proteinansamling syntes.
Unga neuroner växer kortare, inte starkare
För att se huruvida dessa molekylära förändringar faktiskt påverkade cellform observerade teamet unga neuroner växa i odlingsskålar. De märkte cellmembran med en fluorescerande markör och följde axoner över flera dagar när de sträckte sig över plattan. Neuroner med V337M-mutation och neuroner med reducerad tau producerade båda märkbart kortare huvudaxoner och mindre total utväxt, även om antalet små sidogrenar inte förändrades dramatiskt. Med andra ord nådde neuronernas centrala "ledning" inte så långt som den borde. Detta pekar på en förlust av taus normala stödjande roll i axonextension, snarare än en tydlig toxisk effekt som dödar celler direkt.
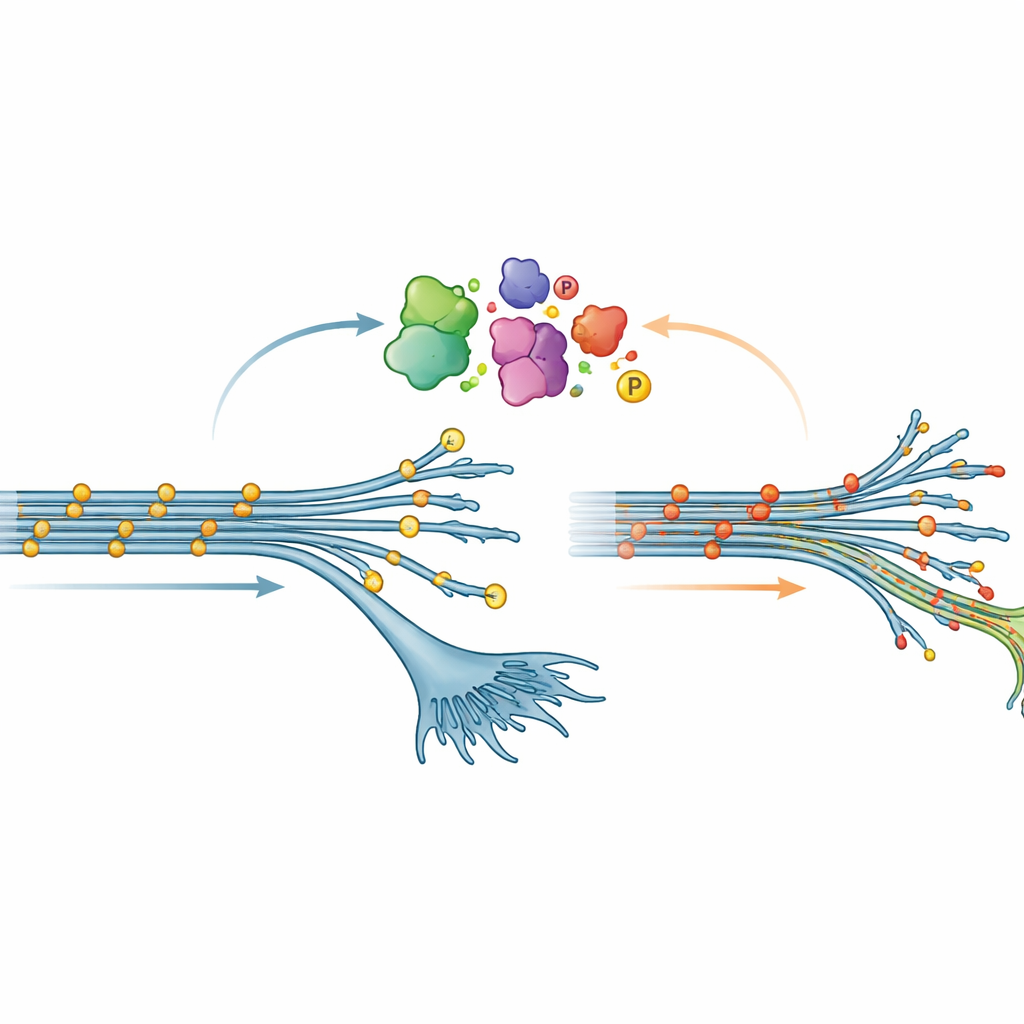
Ett oväntat mönster i taus kemi
En av de mest överraskande upptäckterna rörde fosforylering, en vanlig kemisk modifiering där små fosfatgrupper fästs vid proteiner. I många hjärnsjukdomar blir tau kraftigt fosforylerat; detta ses ofta som en skadlig förändring som främjar att tau bildar trassel. Här visade dock tidiga neuroner som bar V337M-mutation motsatt mönster: tau var mindre fosforylerat på många platser än normalt. Denna "hypofosforylering" avtog gradvis när neuronerna mognade, men var tillräckligt tydlig för att bekräftas både med masspektrometri och vanliga proteintester. När teamet konstgjorde överproduktion av V337M-tau i neuroner vars egna tau hade sänkts återuppstod samma låga fosforyleringsstatus, vilket tyder på att mutationen i sig omformar hur tau modifieras inne i cellerna.
Signalkedjor som omformar axoner och tau
För att förstå vad som driver dessa förändringar sökte forskarna efter signalvägar — kedjor av enzymer som lägger till eller tar bort fosfatgrupper — som var förändrade i V337M-neuroner. Deras fosfoproteomikdata pekade på proteiner involverade i utväxt av neuronala utskott och på specifika kinasfamiljer, inklusive p38 MAP-kinasvägen, som är känd för att påverka neuritutväxt. De genomförde sedan storskaliga CRISPR-skärmar där tusentals gener skruvades upp eller ner för att se vilka som ändrade nivån av en nyckel-fosforylerad form av tau. Många träffar var gener som organiserar cellens interna skelett och axonstruktur, och flera komponenter i p38-vägen påverkade tau-fosforylering specifikt i V337M-neuroner. Detta tyder på en intim koppling mellan maskineriet som bygger axoner och det som finjusterar taus kemiska tillstånd.
Vad detta betyder för förståelsen av demensrisk
Sammantaget tyder fynden på att V337M-tau-mutationen inte bara gör tau mer toxisk i klassisk mening. Istället verkar den i mycket tidiga skeden dämpa taus vanliga stöd för axontillväxt och ändra hur tau fosforyleras, på sätt som överlappar med vad som händer när tau minskas eller förloras. Subtila kopplingsfel under utveckling eller tidig vuxenålder — i kombination med fortlöpande förändringar i taus kemi — kan bidra till att förklara varför personer med MAPT-mutationer uppvisar kognitiva skillnader decennier innan tydlig demens uppträder. Detta arbete belyser att terapier som syftar till att i allmänhet sänka tau kan behöva ta hänsyn till taus nyttiga roller i unga och friska neuroner, och att noggrann fininställning snarare än enkel blockering av tau-relaterade vägar kan vara nyckeln till att skydda hjärnan över livet.
Citering: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Nyckelord: tauprotein, frontotemporal demens, axonväxt, neuronal utveckling, proteinfosforylering