Clear Sky Science · de
Multi-omische Phänotypisierung von MAPT V337M-Neuronen zeigt frühe Veränderungen in der Axonogenese und Tau-Phosphorylierung
Warum diese Forschung für die Gehirngesundheit wichtig ist
Viele Demenzformen, darunter Alzheimer und frontotemporale Demenz, zeigen Ablagerungen eines Proteins namens Tau in Gehirnzellen. Klinisch korreliert abnormes Tau stark mit Gedächtnis- und Denkstörungen, doch wie Tau genau fehlreguliert wird — und was das für junge, sich noch entwickelnde Nervenzellen bedeutet — blieb unklar. Diese Studie fokussiert auf eine vererbte Tau-Mutation, die mit frontotemporaler Demenz verknüpft ist, und stellt eine einfache, aber zentrale Frage: Was geschieht in Neuronen lange bevor Symptome auftreten?
Ein genauerer Blick auf eine riskante Tau-Variante
Die Forschenden konzentrierten sich auf eine einzelne genetische Veränderung, V337M, im MAPT-Gen, das die Bauanleitung für Tau liefert. Träger dieser Mutation entwickeln fast sicher eine frontotemporale Demenz, oft im mittleren Lebensalter. Um frühe Effekte zu untersuchen, nutzte das Team humane induzierte pluripotente Stammzellen — ausgereifte Zellen, die zurückprogrammiert wurden, um embryonale Eigenschaften zu zeigen — und differenzierten sie im Labor zu Neuronen. Sie verglichen Neuronen mit normalem Tau, Neuronen mit einer oder zwei Kopien der V337M-Mutation und Neuronen, in denen die Tau-Spiegel gezielt reduziert worden waren.
Viele molekulare Hinweise gleichzeitig verfolgen
Statt nur ein Signal zu verfolgen, nahmen die Wissenschaftler eine „multi-omische“ Perspektive ein: Sie maßen Genaktivität (RNA-Sequenzierung), die Zugänglichkeit von DNA-Regionen, die Gene steuern (ATAC-seq), sowie Tausende Proteine und deren chemische Anhänge (Proteomik und Phosphoproteomik). Über diese Ebenen hinweg zeichnete sich eine konsistente Botschaft ab. In Neuronen mit der V337M-Mutation und in Neuronen mit reduziertem Tau betrafen die stärksten Veränderungen Gene und Proteine, die Axone aufbauen und formen — die langen, kabelartigen Ausläufer, die Signale zu anderen Zellen leiten. Diese Veränderungen traten früh auf, innerhalb der ersten Entwicklungswochen der Neuronen, bevor es erkennbare Zeichen von Zelltod oder Proteinaggregation gab.
Junge Neuronen wachsen kürzer, nicht stärker
Um zu prüfen, ob diese molekularen Veränderungen die Zellform beeinflussen, beobachtete das Team junge Neuronen in Kultur. Sie markierten Zellmembranen mit einem fluoreszierenden Marker und verfolgten die Axone über mehrere Tage, während sie über die Platte hinauswuchsen. Neuronen mit der V337M-Mutation und Neuronen mit reduziertem Tau zeigten deutlich kürzere Hauptaxone und weniger Gesamtwachstum, obwohl die Zahl kleiner Seitentriebe nicht dramatisch verändert war. Anders gesagt: der zentrale „Draht“ der Nervenzelle erreichte nicht so weit wie erwartet. Das deutet auf einen Verlust der normalen Unterstützungsfunktion von Tau für die Axonverlängerung hin, statt auf einen offensichtlichen toxischen Effekt, der Zellen direkt tötet.
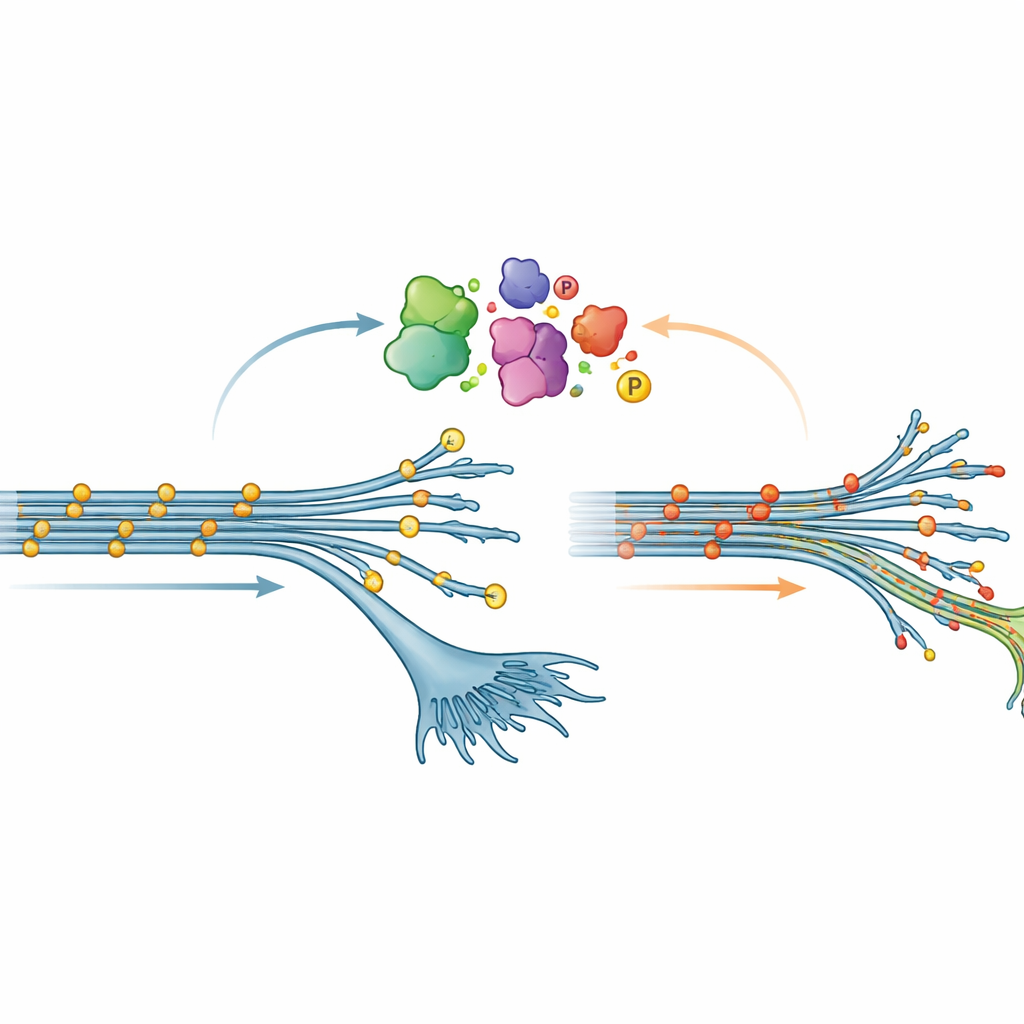
Ein unerwartetes Muster der Tau-Chemie
Einer der überraschendsten Befunde betraf die Phosphorylierung, eine verbreitete chemische Modifikation, bei der winzige Phosphatgruppen an Proteine angehängt werden. In vielen Gehirnerkrankungen ist Tau stark phosphoryliert; das wird oft als schädliche Veränderung angesehen, die die Bildung von Tau-Fibrillen fördert. Hier zeigten Neuronen im frühen Stadium mit der V337M-Mutation jedoch das Gegenteil: Tau war an vielen Stellen weniger phosphoryliert als normal. Diese „Hypophosphorylierung“ verschwand allmählich mit der Reifung der Neuronen, war aber ausreichend robust, um sowohl durch Massenspektrometrie als auch durch Standardproteintests bestätigt zu werden. Als das Team V337M-Tau künstlich überexprimierte in Neuronen, deren eigenes Tau heruntergeregelt worden war, trat derselbe niedrige Phosphorylierungszustand wieder auf — ein Hinweis darauf, dass die Mutation selbst die intrazelluläre Modifikation von Tau verändert.
Signalwege, die Axone und Tau umgestalten
Um zu verstehen, was diese Veränderungen antreibt, suchten die Forschenden nach Signalwegen — Kaskaden von Enzymen, die Phosphatgruppen hinzufügen oder entfernen — die in V337M-Neuronen verändert waren. Ihre Phosphoproteomik-Daten wiesen auf Proteine hin, die am Wachstum neuronaler Fortsätze beteiligt sind, und auf bestimmte Kinasenfamilien, darunter den p38-MAP-Kinase-Weg, der für das Neuritenwachstum bekannt ist. Anschließend führten sie groß angelegte CRISPR-Screens durch und veränderten tausende Gene, um zu sehen, welche das Niveau einer wichtigen phosphorylierten Tau-Form beeinflussen. Viele Treffer waren Gene, die das zelluläre Innengerüst und die Axonstruktur organisieren; mehrere Komponenten des p38-Wegs beeinflussten speziell die Tau-Phosphorylierung in V337M-Neuronen. Das legt eine enge Verbindung nahe zwischen der Maschinerie, die Axone aufbaut, und der Maschinerie, die den chemischen Zustand von Tau einstellt.
Was das für das Verständnis des Demenzrisikos bedeutet
In der Summe deuten die Ergebnisse darauf hin, dass die V337M-Tau-Mutation Tau nicht einfach im klassischen Sinne toxischer macht. Stattdessen scheint sie sehr früh die normale Unterstützung von Tau für das Axonwachstum zu dämpfen und die Tau-Phosphorylierung zu verändern — Effekte, die sich mit denen überschneiden, die durch Verringerung oder Verlust von Tau entstehen. Subtile Verdrahtungsfehler in der Entwicklung oder im frühen Erwachsenenalter — kombiniert mit anhaltenden Veränderungen in der Tau-Chemie — könnten erklären, weshalb Träger von MAPT-Mutationen jahrzehntelang kognitive Unterschiede zeigen, bevor eindeutige Demenz einsetzt. Die Arbeit macht deutlich, dass Therapien, die allgemein auf eine Verringerung von Tau abzielen, die nützlichen Funktionen von Tau in jungen, gesunden Neuronen berücksichtigen sollten, und dass ein fein abgestimmtes Eingreifen — statt bloßes Blockieren — entscheidend sein könnte, um das Gehirn ein Leben lang zu schützen.
Zitation: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Schlüsselwörter: Tau-Protein, frontotemporale Demenz, Axonwachstum, neurale Entwicklung, Proteinphosphorylierung