Clear Sky Science · pl
Wieloomiczne fenotypowanie neuronów z wariantem MAPT V337M ujawnia wczesne zmiany w aksonogenezie i fosforylacji tau
Dlaczego te badania mają znaczenie dla zdrowia mózgu
Wiele postaci demencji, w tym choroba Alzheimera i otępienie czołowo-skroniowe, wiąże się z nagromadzeniami białka tau wewnątrz komórek mózgu. Lekarze obserwują, że nieprawidłowe tau silnie koreluje z zaburzeniami pamięci i funkcji poznawczych, ale dokładny mechanizm, w jaki tau ulega zmianom — i co robi młodym, nadal rozwijającym się komórkom nerwowym — pozostawał niejasny. To badanie skupia się na dziedzicznym wariancie tau powiązanym z otępieniem czołowo-skroniowym i stawia proste, lecz istotne pytanie: co dzieje się z neuronami dużo wcześniej, zanim pojawią się objawy?
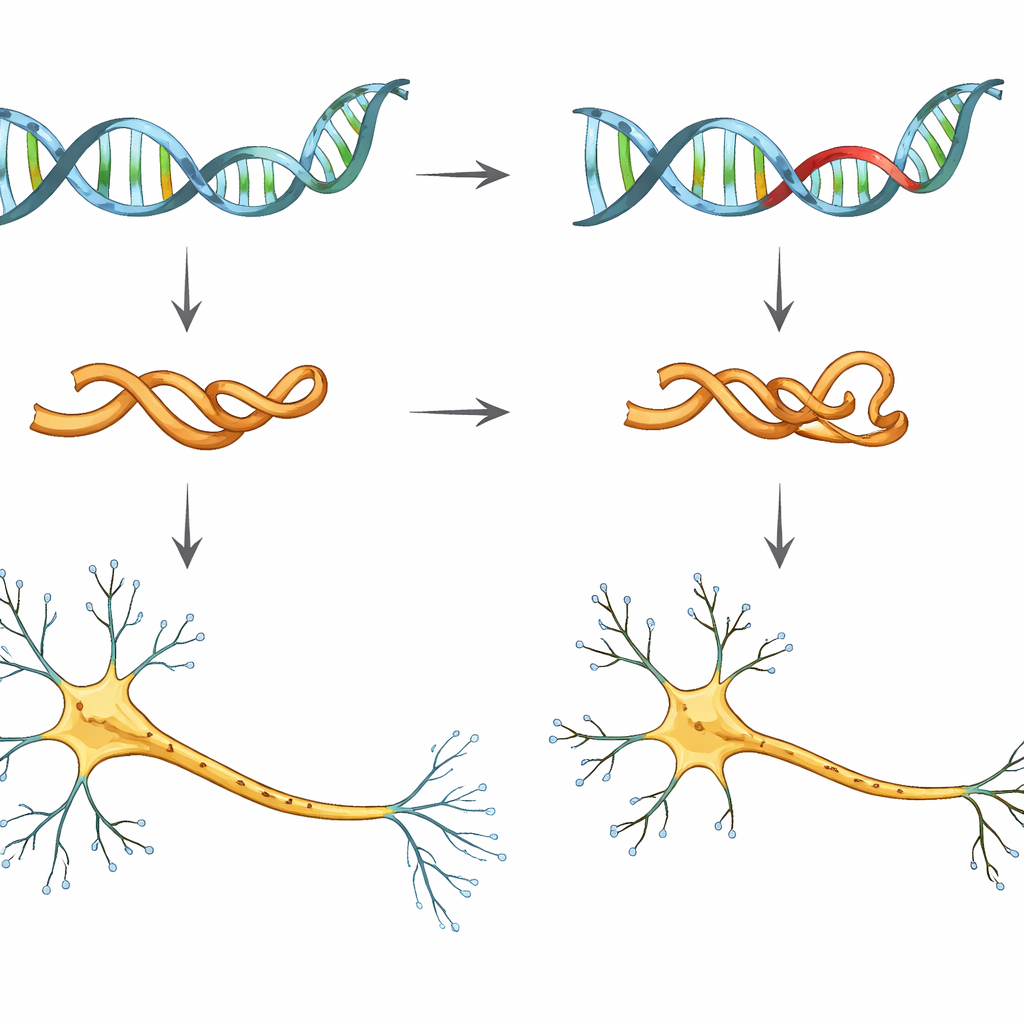
Bliższe spojrzenie na ryzykowną wersję tau
Naukowcy skoncentrowali się na pojedynczej zmianie genetycznej, zwanej V337M, w genie MAPT, który koduje tau. Osoby noszące tę mutację są niemal pewne rozwoju otępienia czołowo-skroniowego, często w średnim wieku. Aby zbadać jej wczesne skutki, zespół użył ludzkich indukowanych pluripotencjalnych komórek macierzystych — komórek dorosłych przeprogramowanych do stanu przypominającego embrionalny — i przekształcił je w neurony w laboratorium. Porównali neurony z normalnym tau, neurony z jedną lub dwiema kopią wariantu V337M oraz neurony, w których poziomy tau zostały celowo obniżone.
Śledzenie wielu molekularnych wskazówek naraz
Zamiast obserwować tylko jeden sygnał, naukowcy przyjęli „wieloomiczny” punkt widzenia: mierzyli aktywność genów (sekwencjonowanie RNA), dostępność regionów DNA kontrolujących geny (ATAC-seq) oraz tysiące białek i ich chemicznych znaków (proteomika i fosfoproteomika). Na tych różnych poziomach pojawił się spójny komunikat. W neuronach z mutacją V337M oraz w neuronach z obniżonym tau najsilniejsze zmiany dotyczyły genów i białek, które budują i kształtują aksony — długie, przypominające kable wypustki, które przekazują sygnały do innych komórek. Zmiany te pojawiały się wcześnie, w ciągu pierwszych tygodni rozwoju neuronów, przed jakimikolwiek widocznymi oznakami śmierci komórek czy agregacji białek.
Młode neurony rosną krócej, nie mocniej
Aby sprawdzić, czy te molekularne zmiany rzeczywiście wpływają na kształt komórek, zespół obserwował rozwój młodych neuronów w hodowlach. Oznaczyli błony komórkowe znacznikiem fluorescencyjnym i przez kilka dni śledzili aksony, gdy wydłużały się po płytce. Neurony z mutacją V337M oraz neurony z obniżonym tau wytwarzały wyraźnie krótsze główne aksony i mniejsze całkowite wydłużenie, chociaż liczba drobnych bocznych gałązek nie ulegała znacznym zmianom. Innymi słowy, centralny „przewód” neuronu nie sięgał tak daleko, jak powinien. Wskazuje to na osłabienie normalnej wspierającej roli tau w wydłużaniu aksonu, a nie na oczywisty efekt toksyczny prowadzący bezpośrednio do śmierci komórek.
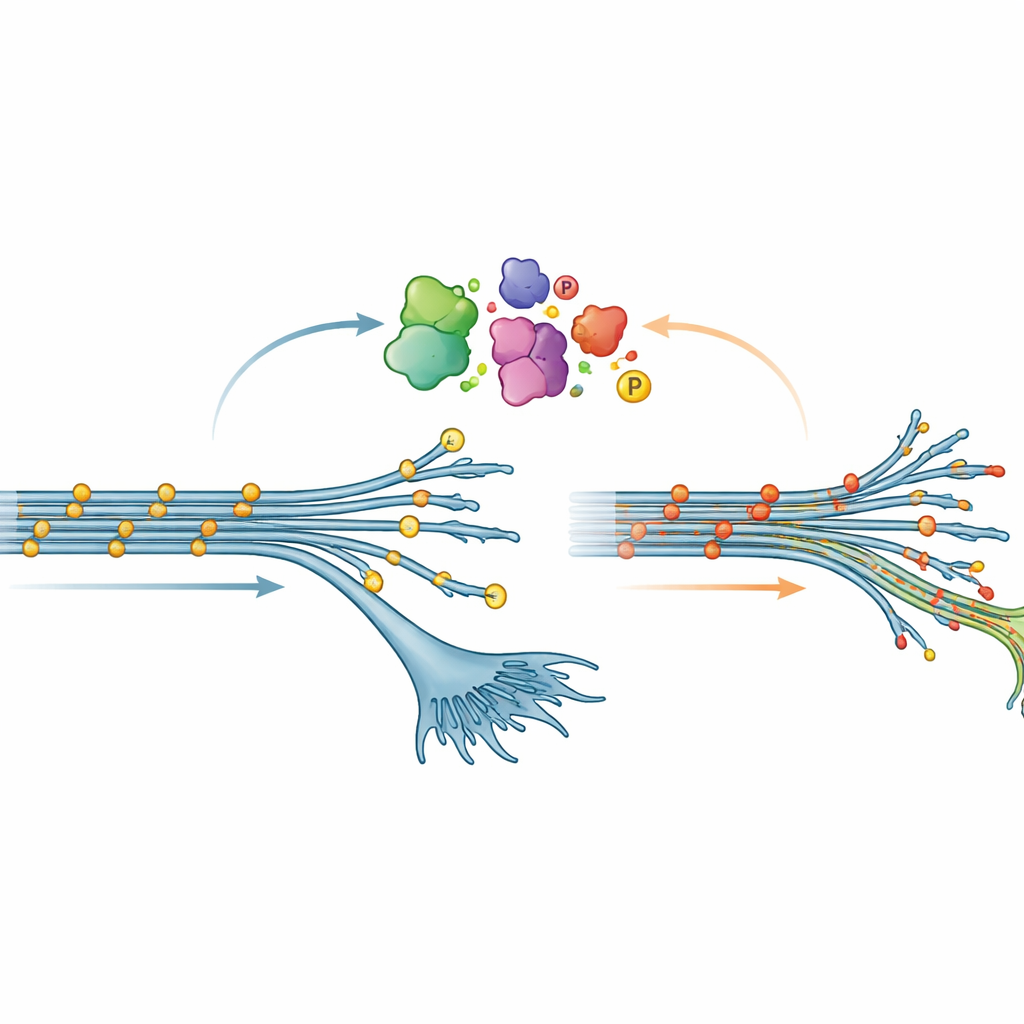
Niespodziewany wzorzec chemii tau
Jednym z najbardziej zaskakujących odkryć była fosforylacja — powszechna modyfikacja chemiczna, w której małe grupy fosforanowe przyłączają się do białek. W wielu chorobach mózgu tau staje się mocno sfosforylowane; często uważa się to za zmianę szkodliwą sprzyjającą tworzeniu splotów. Tu jednak we wczesnych neuronach z mutacją V337M zaobserwowano odwrotny wzorzec: tau był mniej sfosforylowany w wielu miejscach niż normalnie. Ta „hipofosforylacja” stopniowo zanikała wraz z dojrzewaniem neuronów, ale była na tyle wyraźna, że potwierdzono ją zarówno metodą spektrometrii mas, jak i standardowymi testami białkowymi. Gdy zespół sztucznie nadprodukowal wariant V337M w neuronach, których własne tau zostało zredukowane, pojawiał się ten sam stan niskiej fosforylacji, co sugeruje, że sama mutacja przekształca sposób, w jaki tau jest modyfikowane wewnątrz komórek.
Szlaki sygnałowe przekształcające aksony i tau
Aby zrozumieć, co napędza te zmiany, badacze szukali szlaków sygnałowych — łańcuchów enzymów dodających lub usuwających grupy fosforanowe — które były zmienione w neuronach V337M. Dane z fosfoproteomiki wskazały na białka zaangażowane w wzrost wypustek nerwowych oraz na konkretne rodziny kinaz, w tym szlak kinazy p38 MAP, znany z wpływu na wzrost neurytów. Następnie przeprowadzili szerokozakresowe ekrany CRISPR, zwiększając lub obniżając aktywność tysięcy genów, by sprawdzić, które z nich zmieniają poziom kluczowej sfosforylowanej formy tau. Wiele trafień stanowiły geny organizujące wewnętrzny szkielet komórki i strukturę aksonu, a kilka składników szlaku p38 wpływało na fosforylację tau w sposób specyficzny dla neuronów V337M. Sugeruje to bliskie powiązanie między maszynerią budującą aksony a maszynerią regulującą stan chemiczny tau.
Co to oznacza dla zrozumienia ryzyka demencji
W sumie wyniki sugerują, że mutacja V337M w tau nie po prostu sprawia, że tau staje się bardziej toksyczne w klasycznym sensie. Zamiast tego we wczesnym okresie życia wydaje się osłabiać zwykłą rolę tau we wspieraniu wzrostu aksonów i zmieniać sposób jego fosforylacji, w sposób pokrywający się z efektami obserwowanymi przy obniżeniu lub utracie tau. Subtelne defekty okablowania podczas rozwoju lub we wczesnej dorosłości — w połączeniu z trwającymi zmianami chemicznymi tau — mogą pomóc wyjaśnić, dlaczego osoby noszące mutacje w MAPT wykazują różnice poznawcze dekady przed wyraźnym pojawieniem się demencji. Praca ta podkreśla, że terapie mające na celu szerokie obniżanie poziomu tau powinny uwzględniać pomocnicze funkcje tau w młodych i zdrowych neuronach, a precyzyjne dostrojenie, zamiast prostego zablokowania, szlaków związanych z tau może być kluczowe dla ochrony mózgu przez całe życie.
Cytowanie: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Słowa kluczowe: białko tau, otępienie czołowo-skroniowe, wzrost aksonów, rozwój neuronów, fosforylacja białek