Clear Sky Science · he
פנוטייפינג רב-אומי של נוירונים עם MAPT V337M חושף שינויים מוקדמים באקסונוגנזה ובפוספורילציה של טאו
מדוע המחקר הזה חשוב לבריאות המוח
צורות רבות של דמנציה, כולל מחלת האלצהיימר ודמנציה פרונטו-טמפורלית, כרוכות בצברים של חלבון בשם טאו בתוך תאי מוח. רופאים רואים שקיום טאו בלתי תקין מקושר חזק ללקויות בזיכרון ובחשיבה, אבל איך בדיוק טאו משתבש — ומה זה עושה לתאי עצב צעירים שעדיין בהתפתחות — נותר לא בגדר וודאות. מחקר זה מתמקד במוטציה תורשתית בטאו המקושרת לדמנציה פרונטו-טמפורלית ושואל שאלה פשוטה אך קריטית: מה קורה לנוירונים הרבה לפני שהסימפטומים מופיעים?
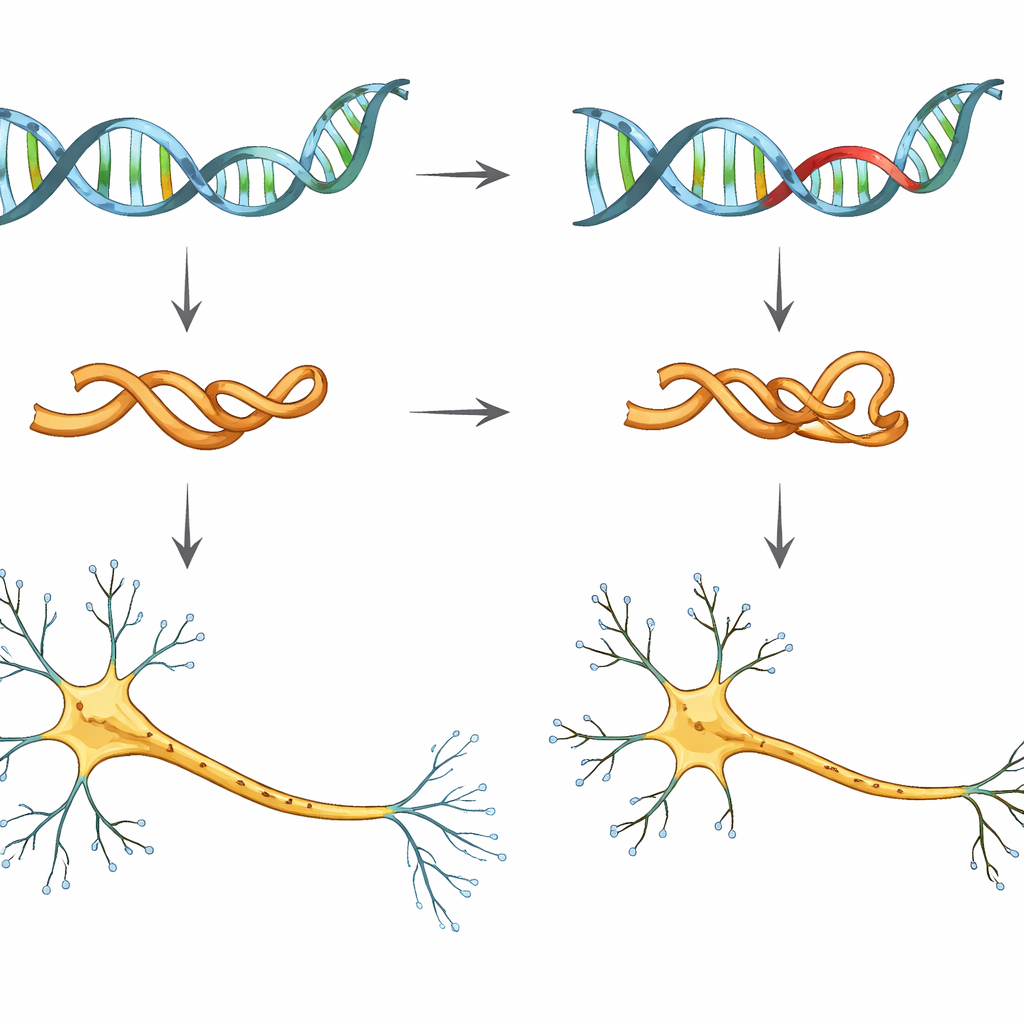
מבט מקרוב על גרסה מסוכנת של טאו
החוקרים התמקדו בשינוי גנטי יחיד, שנקרא V337M, בגן MAPT שמספק את התבנית לטאו. אנשים הנושאים את המוטציה הזו כמעט בטוחים שיפתחו דמנציה פרונטו-טמפורלית, לעתים באמצע החיים. כדי לחקור את ההשפעות המוקדמות שלה, הקבוצה השתמשה בתאים פרוטיפיים מוחשיים (iPSC) אנושיים — תאים בוגרים שתוכנתו מחדש להתנהג כמו תאי עובר — והפכו אותם לנוירונים במעבדה. הם השוו בין נוירונים עם טאו רגיל, נוירונים הנושאים עותק או שניים של מוטציית V337M, ולבין נוירונים שבהם רמות הטאו צומצמו במכוון.
מעקב אחר רמזים מולקולריים רבים בו-זמנית
במקום לעקוב אחרי אות יחיד, המדענים נקטו בגישה "רב-אומית": הם מדדו פעילות גנים (ריצוף RNA), פתיחות של אזורי DNA ששולטים על גנים (ATAC-seq), ואת אלפי החלבונים ותוויותיהם הכימיות (פרוטאומיקה ופוספו-פרוטאומיקה). בין השכבות השונות נשמע מסר עקבי. בנוירונים עם מוטציית V337M, ובנוירונים שבהם טאו הוקטן, השינויים החזקים ביותר נגעו לגנים ולחלבונים בונים ומעצבים אקסונים — ההארכות הארוכות בדמוי כבל שמעבירות אותות לתאים אחרים. שינויים אלה הופיעו מוקדם, בתוך השבועות הראשונים של התפתחות הנוירונים, לפני כל סימנים ברורים של מוות תאי או הצטברות חלבונים.
נוירונים צעירים צומחים קצרים יותר, לא חזקים יותר
כדי לבדוק האם השינויים המולקולריים הללו משפיעים בפועל על צורת התא, הקבוצה צפתה בנוירונים צעירים צומחים במצלחות תרבות. הם תימתו את ממברנות התאים בסמן פלואורסצנטי ועקבו אחר האקסונים על פני מספר ימים כשהם מתארכים על הגליל. נוירונים עם המוטציה V337M ונוירונים עם טאו מופחת הציגו אקסונים ראשיים קצרים באופן ניכר ופחות יציאה כוללת, אף על פי שמספר הסניפים הצדדיים הקטנים לא השתנה דרמטית. במילים אחרות, ה"חוט" המרכזי של הנוירון לא הגיע עד היעד שאמור היה להגיע. זה מצביע על אובדן של התפקיד התומך הטבוע של טאו בהארכת אקסונים, ולא על אפקט רעיל ברור ההורג תאים באופן מלא.
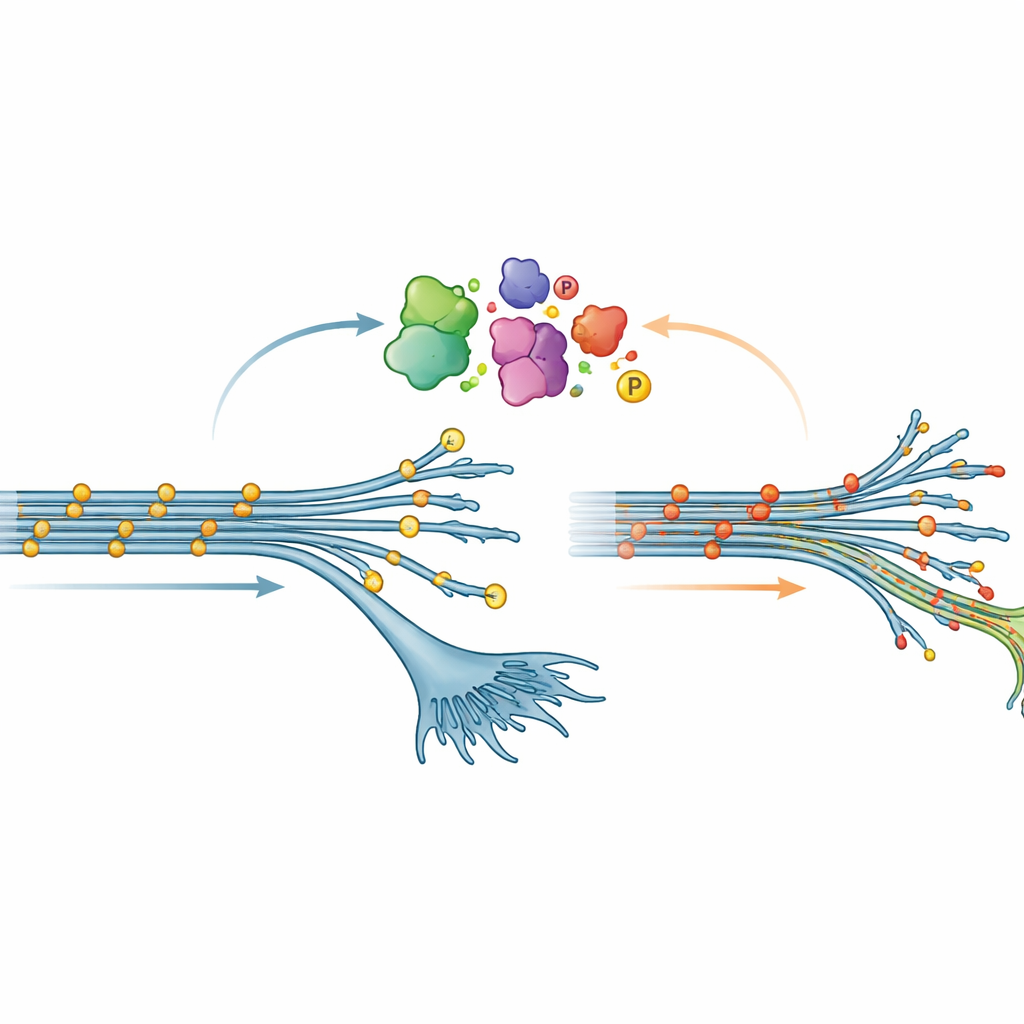
תבנית בלתי צפויה בכימיה של טאו
אחת התגליות המפתיעות ביותר נגעה לפוספורילציה, שינוי כימי נפוץ שבו קבוצות זרחן זעירות מצורפות לחלבונים. במחלות מוח רבות טאו הופך להיות מאוד מפוספורל; שינוי זה נתפס לעתים כתהליך מזיק שמעודד את טאו ליצור קשרים מסולסלים. כאן, עם זאת, נוירונים בשלבי התפתחות מוקדמים הנושאים את V337M הראו את הדפוס ההפוך: טאו היה פחות מפוספורל באתרים רבים לעומת הנורמה. ה"היפופוספורילציה" הזו התפוגגה בהדרגה כשהנוירונים הבשילו, אך היא הייתה חזקה מספיק לאשרור גם באמצעות ספקטרומטריית מסה ובדיקות חלבון סטנדרטיות. כאשר הקבוצה ייצרה באופן מלאכותי עודפי טאו V337M בנוירונים שלגביהם טאו מקומי הורד, אותה תמצית של פוספורילציה נמוכה חזרה והופיעה שוב, מה שמעיד שהמוטציה עצמה מעצבת מחדש את האופן שבו טאו מותאם בתוך התאים.
מסלולי איתות שמעצבים אקסונים וטאו
כדי להבין מה דוחף את השינויים האלה, החוקרים חיפשו מסלולי איתות — שרשרות של אנזימים שמוסיפים או מסירים קבוצות זרחן — שהשתנו בנוירוני V337M. נתוני הפוספו-פרוטאומיקה הצביעו על חלבונים המעורבים בצמיחת שלוחות עצביות ועל משפחות קינאזות ספציפיות, כולל מסלול p38 MAP קינאז, הידוע בכך שהוא משפיע על יציאת נויריטים. לאחר מכן הם ביצעו מסכי CRISPR רחבי היקף, כשהפעילו או כיבו אלפי גנים כדי לראות אילו מהם משנים את רמת צורת הטאו המפוספורלת המרכזית. רבים מהממצאים היו גנים שמארגנים את השלד הפנימי של התא ואת מבנה האקסון, וכמה רכיבים של מסלול p38 השפיעו ספציפית על פוספורילציית טאו בנוירוני V337M. זה מציע קשר הדוק בין המכאניזם שבונה אקסונים לזה שמכוון את המצב הכימי של טאו.
מה משמעות הדבר להבנת סיכון לדמנציה
לסיכום, הממצאים מרמזים שמוטציית טאו V337M אינה פשוטה כ"הפיכת טאו לרעיל" במובן הקלאסי. במקום זאת, בשלב מוקדם מאוד בחיים היא נראית כמחלישה את התמיכה הרגילה של טאו בצמיחת אקסונים ומשנה את אופן הפוספורילציה של טאו, בדרכים החופפות לאלו שמתרחשות כאשר טאו מופחת או אובד. פגמים עדינים בחיווט במהלך ההתפתחות או בתחילת הבגרות — בשילוב עם שינויים מתמשכים בכימיית הטאו — עשויים להסביר מדוע נשאי מוטציות MAPT מראים הבדלים קוגניטיביים עשורים לפני שדמנציה ברורה מתפתחת. עבודה זו מדגישה שטיפולים שמטרתם להוריד טאו באופן נרחב עשויים להצטרך לקחת בחשבון את תפקידי הסיוע של טאו בתאים צעירים ובריאים, וכי כוונון מדויק, ולא חסימה מוחלטת, של מסלולי טאו עשוי להיות המפתח להגנה על המוח לאורך החיים.
ציטוט: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
מילות מפתח: חלבון טאו, דמנציה פרונטו-טמפורלית, צמיחת אקסון, התפתחות עצבית, פוספורילציה של חלבונים