Clear Sky Science · ar
التوصيف متعدد الأوميكس لخلايا عصبية حاملة طفرة MAPT V337M يكشف تغيّرات مبكرة في تكون المحوار وفوسفORYlation التاو
لماذا يهم هذا البحث لصحة الدماغ
تتضمن أشكال متعددة من الخرف، بما في ذلك مرض الزهايمر وخرف الفص الجبهي الصدغي، تكوّن تجمعات من بروتين يُسمى تاو داخل الخلايا العصبية. يُظهر الأطباء أن تغيرات تاو غير الطبيعية ترتبط بشدة بمشكلات الذاكرة والتفكير، لكن كيف يخطئ تاو بالضبط—وما الذي يفعله للخلايا العصبية الشابة والمتطورة—ظل غير واضح. تركز هذه الدراسة على طفرة موروثة في تاو مرتبطة بالخرف الفصّي الصدغي وتطرح سؤالاً بسيطاً لكنه حاسم: ماذا يحدث للخلايا العصبية وقت طويل قبل ظهور الأعراض؟
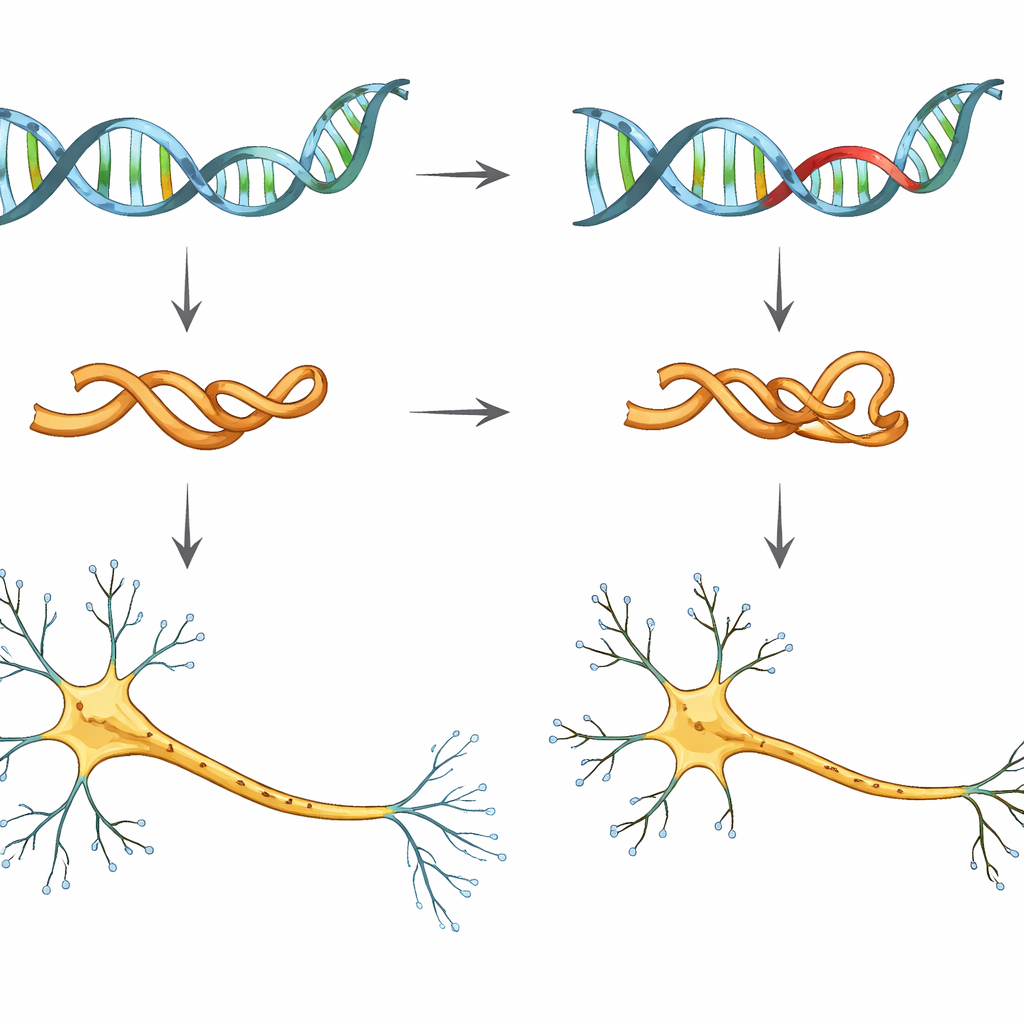
نظرة أقرب إلى نسخة تاو ذات الخطر
ركّز الباحثون على تغيير جيني واحد، يُسمى V337M، في جين MAPT الذي يحدد الشيفرة لبروتين تاو. الأشخاص الحاملون لهذه الطفرة يكاد يكونون متأكدين من الإصابة بخرف الفص الجبهي الصدغي، وغالباً في منتصف العمر. لدراسة تأثيراتها المبكرة، استخدم الفريق خلايا جذعية حِثّها الإنسان (خلايا بالغة أعيد برمجتها لتتصرف كخلايا جنينية) وحولها إلى خلايا عصبية في المختبر. قارنوا خلايا عصبية بها تاو طبيعي، بخلايا تحمل نسخة أو نسختين من طفرة V337M، وبخلايا عصبية تم خفض مستوى تاو فيها عمداً.
متابعة دلائل جزيئية متعددة في آن واحد
بدلاً من تتبّع إشارة واحدة فقط، اتبع العلماء منهجية «متعددة الأوميكس»: قاسوا نشاط الجينات (تسلسل الحمض النووي الريبي)، وانفتاح مناطق الحمض النووي التي تتحكم في الجينات (ATAC-seq)، وآلاف البروتينات وعلاماتها الكيميائية (بروتيوميات وفوسفوبروتيوميات). عبر هذه الطبقات المختلفة، برزت رسالة متسقة. في الخلايا العصبية الحاملة لطفرة V337M، وكذلك في الخلايا التي نُقص فيها تاو، كانت أقوى التغيرات متعلقة بالجينات والبروتينات التي تبني وتشكل المحاور—الامتدادات الطويلة الشبيهة بالكابلات التي تنقل الإشارات إلى خلايا أخرى. ظهرت هذه التغيرات مبكراً، خلال الأسابيع الأولى من تطور الخلايا العصبية، قبل أي بوادر واضحة لموت الخلايا أو تجمعات البروتين.
الخلايا العصبية الشابة تنمو أقصر، لا أقوى
لمعرفة ما إذا كانت هذه التغيرات الجزيئية تؤثر فعلاً على شكل الخلايا، راقب الفريق نمو الخلايا العصبية الشابة في أطباق الزرع. وسموا أغشية الخلايا بعلامة فلورية وتتبعوا المحاور لعدة أيام أثناء امتدادها عبر اللوحة. أنتجت الخلايا الحاملة لطفرة V337M والخلايا ذات تاو المخفّض محاور رئيسية أقصر ونمو إجمالي أقل قابلية للقياس، على الرغم من أن عدد الفروع الجانبية الصغيرة لم يتغير بشكل كبير. بعبارة أخرى، فشل «السلك» المركزي للخلية العصبية في الوصول إلى ما ينبغي عليه الوصول إليه. يشير هذا إلى فقدان دور تاو الداعم الطبيعي في امتداد المحوار، بدلاً من تأثير سام واضح يقتل الخلايا مباشرة.
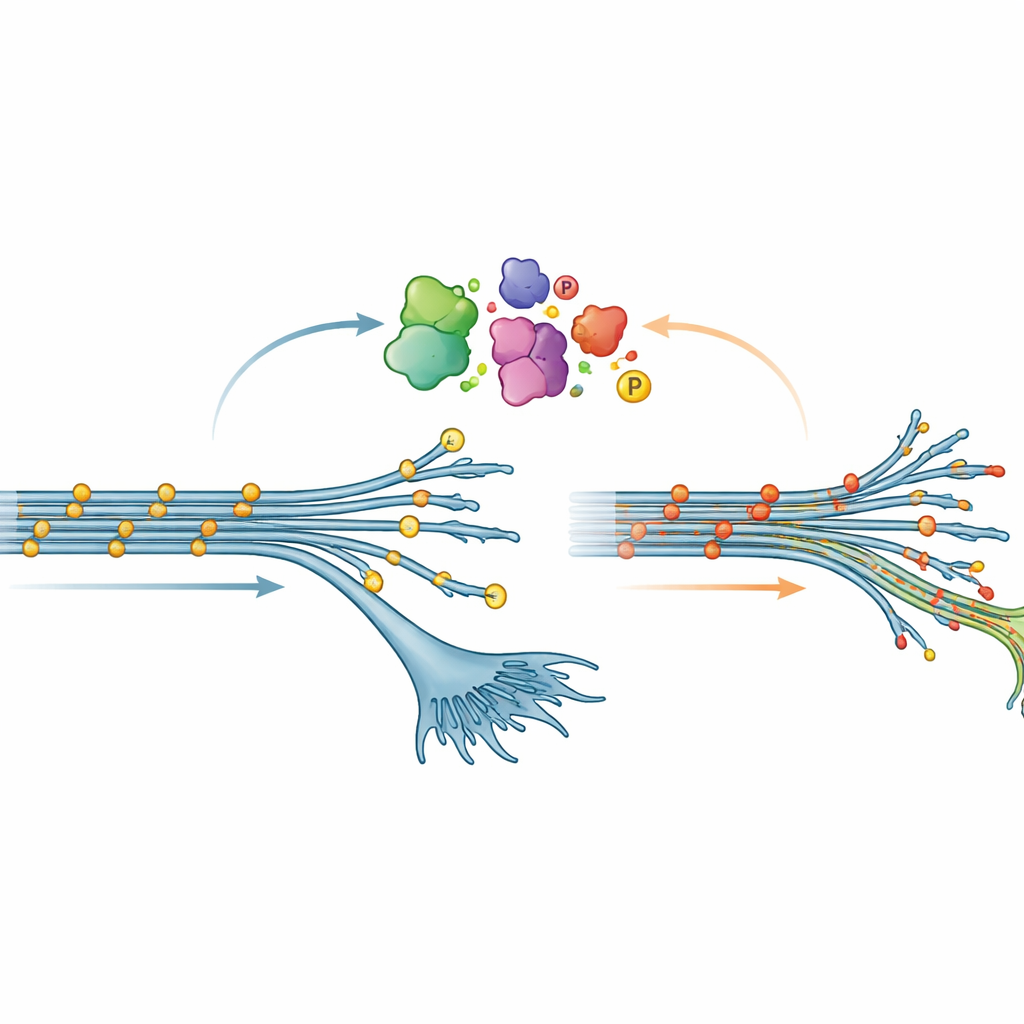
نمط غير متوقع لكيمياء تاو
كان أحد أكثر الاكتشافات مفاجأة يتعلق بالفوسفرة، التعديل الكيميائي الشائع حيث تُلحق مجموعات فوسفات صغيرة بالبروتينات. في العديد من أمراض الدماغ، يصبح تاو شديد الفوسفرة؛ وغالباً ما يُنظر إلى ذلك كتغير ضار يشجع تاو على تشكيل تشابكات. هنا، مع ذلك، أظهرت الخلايا العصبية المبكرة الحاملة لطفرة V337M النمط المعاكس: كان تاو أقل فوسفرة في العديد من المواقع مقارنةً بالطبيعي. تلاشى هذا «النقص في الفوسفرة» تدريجياً مع نضوج الخلايا العصبية، لكنه كان قوياً بما يكفي لأن يؤكدته كل من قياسات مطيافية الكتلة والاختبارات البروتينية التقليدية. عندما زاد الفريق اصطناع تاو V337M في خلايا عصبية تم خفض تاو فيها، عاد نفس الوضع منخفض الفوسفرة، مما يوحي بأن الطفرة نفسها تعيد تشكيل كيفية تعديل تاو داخل الخلايا.
مسارات إشارية تعيد تشكيل المحاور وتاو
لفهم ما يقود هذه التغيرات، بحث الباحثون عن مسارات إشارية—سلاسل من الإنزيمات التي تضيف أو تزيل مجموعات الفوسفات—التي تغيرت في خلايا V337M. أشارت بيانات الفوسفوبروتيوميات إلى بروتينات مشاركة في نمو امتدادات الخلايا العصبية وإلى عائلات كينازات محددة، بما في ذلك مسار كيناز p38 MAP المعروف بتأثيره على نمو الزوائد العصبية. ثم أجروا شاشات CRISPR واسعة النطاق، فعّلوا أو أخمدوا آلاف الجينات لمعرفة أيها يغيّر مستوى شكل تاو المُفَسفر الأساسي. كانت العديد من النتائج جينات تنظم الهيكل الخلوي الداخلي وبنية المحوار، وأثرت عدة مكونات من مسار p38 على فوسفرة تاو بشكل خاص في خلايا V337M. يشير هذا إلى ارتباط وثيق بين آلية بناء المحاور وآلية ضبط الحالة الكيميائية لتاو.
ما الذي يعنيه هذا لفهم خطر الخرف
عامةً، تشير النتائج إلى أن طفرة تاو V337M لا تجعل تاو أكثر سمية بالمعنى الكلاسيكي فحسب. بدلاً من ذلك، في المراحل المبكرة من الحياة يبدو أنها تضعف الدعم الطبيعي لتاو في نمو المحاور وتغيّر كيفية فوسفرة تاو، بطرق تتداخل مع ما يحدث عند تقليل أو فقدان تاو. قد تفسر عيوب التوصيل العصبي الطفيفة أثناء التطور أو البلوغ المبكر—مرافقةً بتغيرات مستمرة في كيمياء تاو—سبب ظهور فروق معرفية لدى حاملي طفرات MAPT قبل عقود من بروز الخرف الواضح. يبرز هذا العمل أن العلاجات المصممة لخفض تاو على نطاق واسع قد تحتاج إلى مراعاة الأدوار المفيدة لتاو في الخلايا العصبية الشابة والسليمة، وأن الضبط الدقيق بدلاً من الحجب البسيط لمسارات تاو قد يكون مفتاحاً لحماية الدماغ مدى الحياة.
الاستشهاد: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
الكلمات المفتاحية: بروتين تاو, خرف الفص الجبهي الصدغي, نمو المحوار, تطور عصبي, فوسفرة البروتين