Clear Sky Science · nl
Multi-omische fenotypering van MAPT V337M-neuronen onthult vroege veranderingen in axonogenese en tau-fosforylering
Waarom dit onderzoek belangrijk is voor de gezondheid van de hersenen
Veel vormen van dementie, waaronder de ziekte van Alzheimer en frontotemporale dementie, gaan gepaard met ophopingen van een eiwit genaamd tau binnen zenuwcellen. Artsen zien dat abnormaal tau sterk samenhangt met geheugen- en denkproblemen, maar precies hoe tau fout gaat — en wat het doet met jonge, nog in ontwikkeling zijnde neuronen — bleef onduidelijk. Deze studie zoomt in op een erfelijke tau-mutatie die gekoppeld is aan frontotemporale dementie en stelt een eenvoudige maar cruciale vraag: wat gebeurt er met neuronen lang voordat symptomen zichtbaar worden?
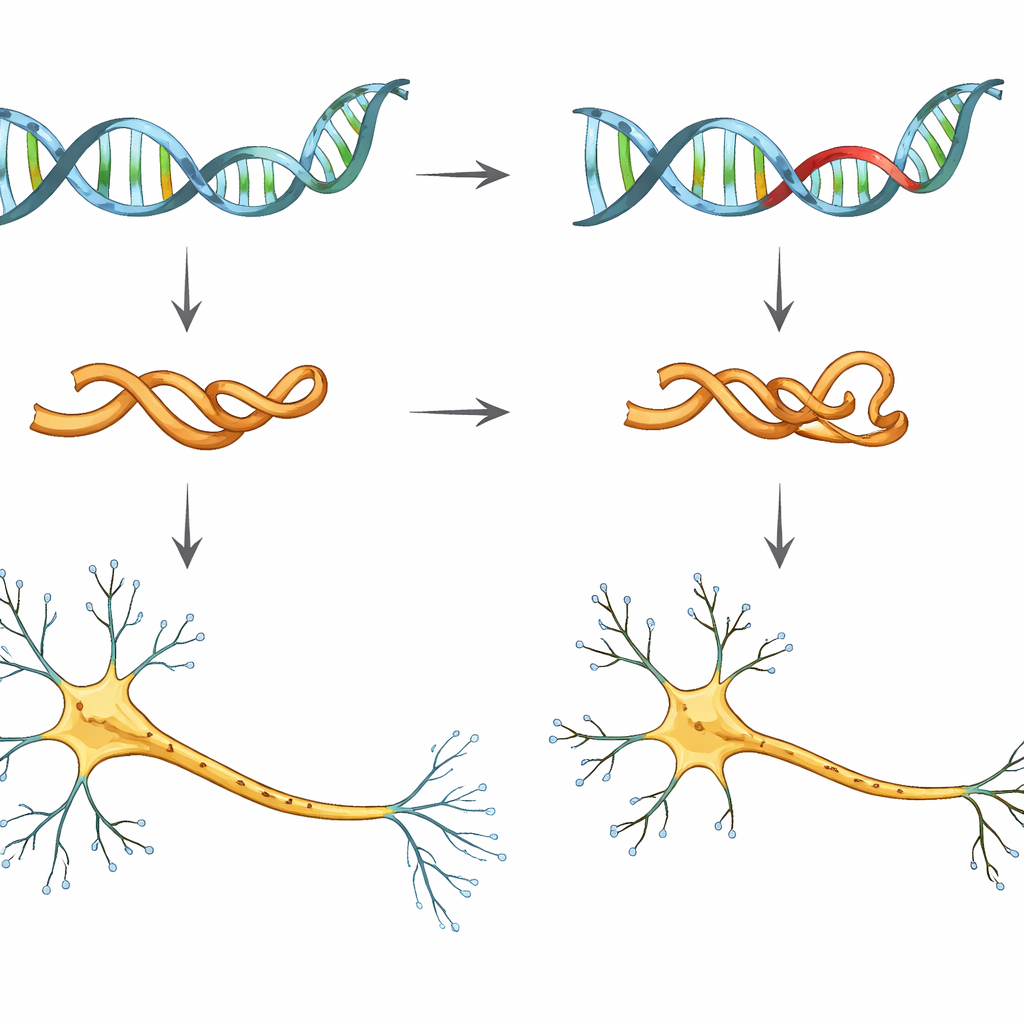
Een nadere blik op een risicovolle variant van tau
De onderzoekers richtten zich op één genetische verandering, V337M genoemd, in het MAPT-gen, dat de blauwdruk voor tau bevat. Mensen die deze mutatie dragen, zullen vrijwel zeker frontotemporale dementie ontwikkelen, vaak in de middelbare leeftijd. Om de vroege effecten te bestuderen, gebruikte het team humane geïnduceerde pluripotente stamcellen — volwassen cellen die opnieuw geprogrammeerd zijn om zich als embryonale cellen te gedragen — en differentieerde die in neuronen in het laboratorium. Ze vergeleken neuronen met normaal tau, neuronen met één of twee kopieën van de V337M-mutatie, en neuronen waarbij de tau-niveaus opzettelijk verlaagd waren.
Verschillende moleculaire aanwijzingen tegelijk volgen
In plaats van slechts één signaal te volgen, namen de wetenschappers een “multi-omische” benadering: ze maten genactiviteit (RNA-sequencing), de toegankelijkheid van DNA-regio’s die genen reguleren (ATAC-seq), en duizenden eiwitten en hun chemische labels (proteomica en fosfoproteomica). Over deze lagen heen kwam een consistent beeld naar voren. In neuronen met de V337M-mutatie, en in neuronen waar tau was verlaagd, betroffen de sterkste veranderingen genen en eiwitten die axonen opbouwen en vormgeven — de lange, kabelachtige uitlopers die signalen naar andere cellen dragen. Deze veranderingen traden vroeg op, binnen de eerste weken van neuronale ontwikkeling, voordat er duidelijke tekenen van celdood of eiwitophopingen waren.
Jonge neuronen groeien korter, niet sterker
Om te zien of deze moleculaire veranderingen daadwerkelijk de celvorm beïnvloedden, volgde het team jonge neuronen in kweekschalen. Ze markeerden celmembranen met een fluorescent label en tekenden axonen over meerdere dagen terwijl die zich over de plaat uitstrekten. Neuronen met de V337M-mutatie en neuronen met verlaagd tau produceerden beide duidelijk kortere hoofdaxonen en minder totale uitgroei, hoewel het aantal kleine zijtakken niet dramatisch veranderde. Met andere woorden, de centrale “geleider” van de neuron reikte niet zo ver als zou moeten. Dit wijst op een verlies van de normale ondersteunende rol van tau bij axonuitbreiding, eerder dan op een duidelijke toxische werking die cellen direct doet afsterven.
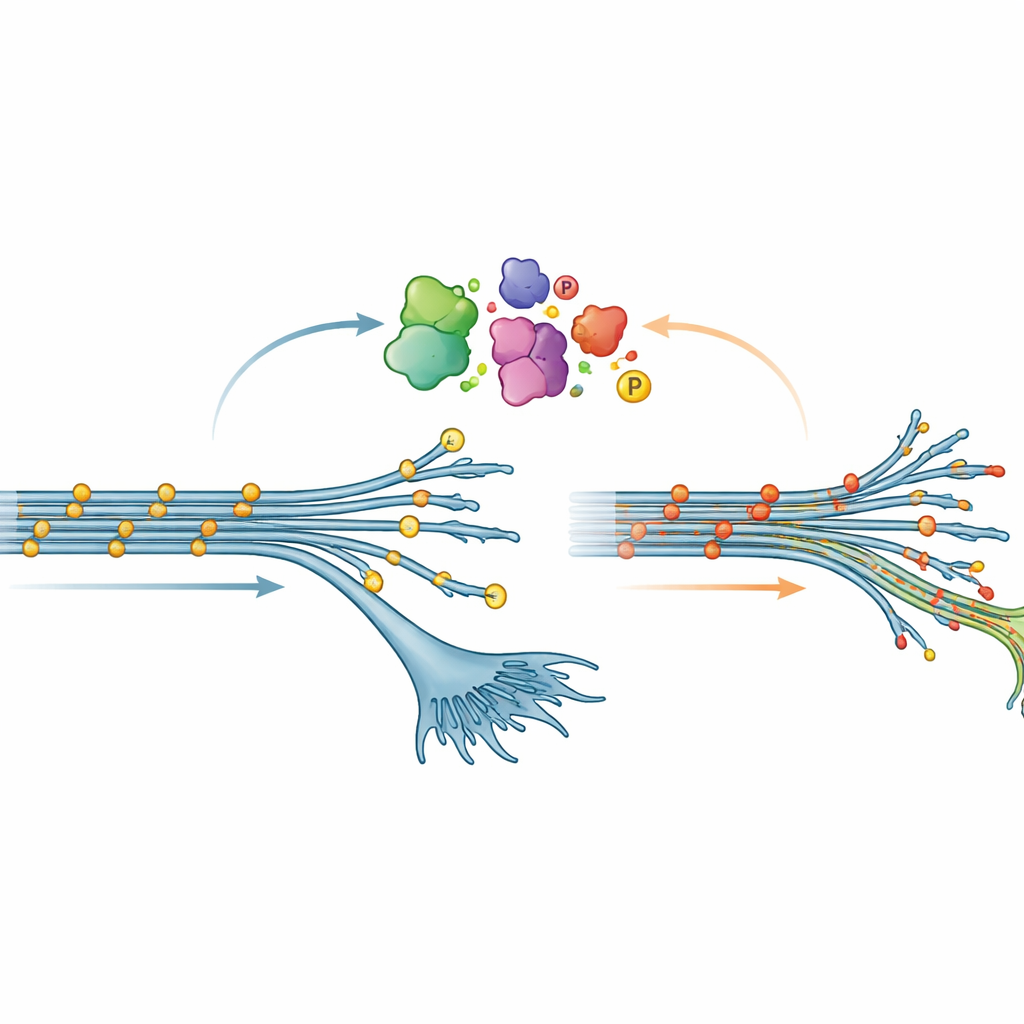
Een onverwacht patroon in tau-chemie
Een van de meest verrassende ontdekkingen had te maken met fosforylering, een veelvoorkomende chemische modificatie waarbij kleine fosfaatgroepen aan eiwitten worden gehecht. In veel hersenziekten wordt tau zwaar gefosforyleerd; dat wordt vaak gezien als een schadelijke verandering die de vorming van kluwens bevordert. Hier lieten vroege neuronen met de V337M-mutatie echter het tegenovergestelde zien: tau was op veel plaatsen minder gefosforyleerd dan normaal. Deze “hypofosforylering” vervaagde geleidelijk naarmate de neuronen rijpten, maar was stevig genoeg om bevestigd te worden met zowel massaspectrometrie als standaard eiwitanalyses. Toen het team de V337M-tau kunstmatig overproduceerde in neuronen waarvan het eigen tau was teruggeschroefd, verscheen dezelfde laag-fosforyleringsstatus opnieuw, wat suggereert dat de mutatie zelf verandert hoe tau binnen cellen wordt gemodificeerd.
Signaalroutes die axonen en tau hervormen
Om te begrijpen wat deze veranderingen aandrijft, zochten de onderzoekers naar signaalroutes — ketens van enzymen die fosfaatgroepen toevoegen of verwijderen — die in V337M-neuronen veranderd waren. Hun fosfoproteomica-gegevens wezen op eiwitten betrokken bij de uitgroei van neuronale uitlopers en op specifieke kinasefamilies, waaronder de p38 MAP-kinase-route, die bekendstaat om invloed op neurietgroei. Vervolgens voerden ze grootschalige CRISPR-screens uit, waarbij ze duizenden genen hoger of lager zetten om te zien welke het niveau van een belangrijke gefosforyleerde vorm van tau veranderden. Veel hits waren genen die het interne skelet en de axonstructuur van de cel organiseren, en verschillende componenten van het p38-pad beïnvloedden tau-fosforylering specifiek in V337M-neuronen. Dit suggereert een nauwe koppeling tussen het apparaat dat axonen bouwt en het apparaat dat de chemische staat van tau afstemt.
Wat dit betekent voor het begrijpen van dementierisico
Samengevoegd suggereren de bevindingen dat de V337M-taumutatie niet simpelweg tau toxischer maakt in de klassieke zin. In een zeer vroeg stadium lijkt ze eerder tau’s normale ondersteuning van axonuitgroei te verzwakken en verandert ze hoe tau gefosforyleerd wordt, op manieren die overlappen met wat er gebeurt wanneer tau verminderd of verloren is. Subtiele bedradingstekorten tijdens de ontwikkeling of vroege volwassenheid — gecombineerd met aanhoudende veranderingen in tau-chemie — kunnen helpen verklaren waarom mensen met MAPT-mutaties cognitieve verschillen vertonen decennia voordat duidelijke dementie optreedt. Dit werk benadrukt dat therapieën die gericht zijn op brede verlaging van tau mogelijk rekening moeten houden met de nuttige rollen van tau in jonge en gezonde neuronen, en dat zorgvuldige aanpassing, eerder dan simpelweg blokkeren, van tau-gerelateerde paden cruciaal kan zijn om de hersenen levenslang te beschermen.
Bronvermelding: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Trefwoorden: tau-eiwit, frontotemporale dementie, axon-groei, neurale ontwikkeling, eiwitfosforylering