Clear Sky Science · ja
MAPT V337Mニューロンのマルチオミクス表現型解析が明らかにした軸索形成とタウのリン酸化の早期変化
なぜこの研究が脳の健康に重要なのか
アルツハイマー病や前頭側頭型認知症など多くの認知症では、タウと呼ばれるタンパク質が脳細胞内に凝集して見られます。臨床では異常なタウと記憶・認知障害が強く関連することがわかっていますが、タウがどのように変調し、若く発達途上にある神経細胞に何をもたらすのかははっきりしていません。本研究は、前頭側頭型認知症に関連する遺伝性のタウ変異に焦点を当て、症状が出るずっと前の段階でニューロンに何が起きるかという単純だが重要な問いを投げかけます。
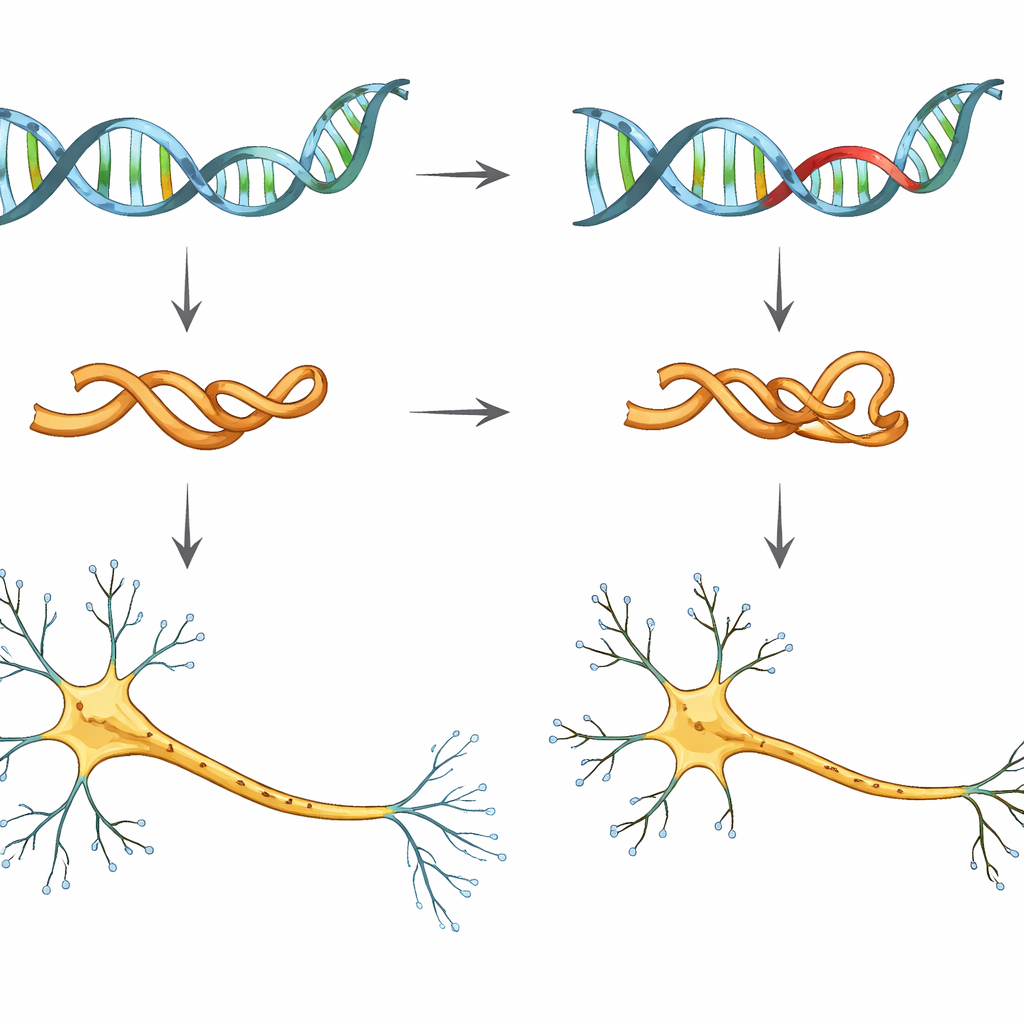
リスクのあるタウ変異を詳しく見る
研究者らはタウの設計図を与えるMAPT遺伝子の単一の変化、V337Mに注目しました。この変異を持つ人は多くの場合、しばしば中年に前頭側頭型認知症を発症します。早期の影響を調べるため、チームはヒトの誘導多能性幹細胞(成体細胞を胚様の性質にリプログラミングした細胞)を用いて実験室でニューロンに分化させました。正常なタウを持つニューロン、V337M変異を片方あるいは両方に持つニューロン、そしてタウの量を意図的に減らしたニューロンを比較しました。
複数の分子手がかりを同時に追う
単一の指標だけを追うのではなく、研究者らは「マルチオミクス」的な見方を採りました:遺伝子発現(RNAシーケンシング)、遺伝子を制御するDNA領域の開放性(ATAC-seq)、そして数千種類のタンパク質とその化学修飾(プロテオミクスおよびリン酸化プロテオミクス)を測定しました。これら異なる層を横断して、一貫したメッセージが浮かび上がりました。V337M変異を持つニューロンとタウが低下したニューロンで最も顕著に変化していたのは、信号を他細胞に伝える長いケーブル状の突起である軸索を作り形づくる遺伝子やタンパク質でした。これらの変化は、細胞死やタンパク質凝集の明白な兆候が出る前の、ニューロン発生の最初の数週間のうちに現れました。
若いニューロンは短く伸びる、強くはならない
これらの分子変化が実際に細胞形態に影響するかを確かめるため、チームは培養皿内で若いニューロンの成長を観察しました。細胞膜を蛍光マーカーで標識し、軸索がプレート上に伸びる様子を数日間追跡しました。V337M変異を持つニューロンとタウが減らされたニューロンは、主要な軸索が著しく短く、総伸長量も少なかったのです。一方で小さな側枝の数は劇的には変わりませんでした。言い換えれば、ニューロンの中心的な“配線”が本来届くべきところまで到達していませんでした。これは、細胞を即座に死に至らしめるような明らかな毒性ではなく、軸索伸展におけるタウの通常の支持役割の喪失を示唆します。
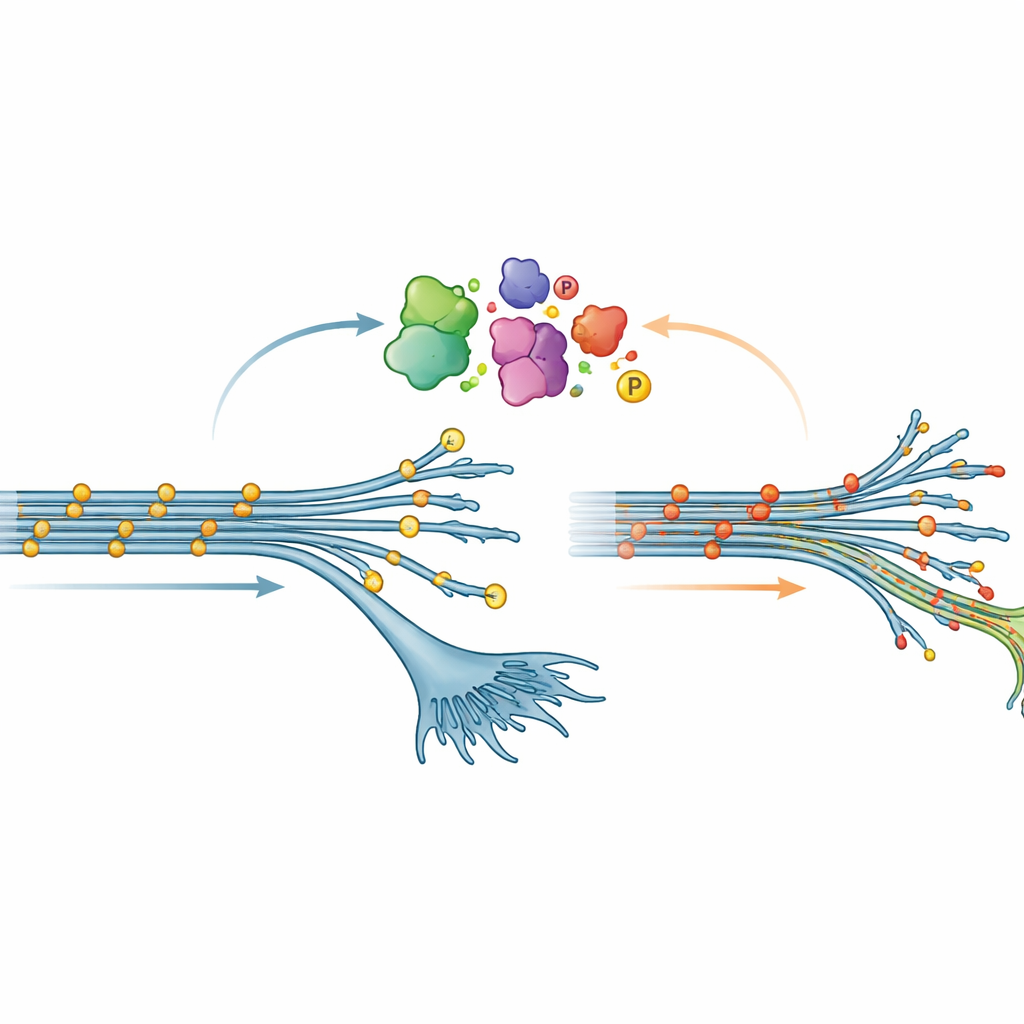
予想外のタウの化学的パターン
最も驚きだった発見の一つはリン酸化に関するものでした。リン酸化は小さなリン酸基がタンパク質に付加される一般的な化学修飾です。多くの脳疾患ではタウが過度にリン酸化されることがあり、これがタウの凝集を促す有害な変化と見なされることが多いです。しかし本研究では、V337M変異を持つ初期段階のニューロンは逆のパターンを示しました:タウは多くの部位で通常よりもむしろリン酸化が少ない(低リン酸化)状態でした。この“低リン酸化”はニューロンが成熟するにつれて次第に薄れていきましたが、質量分析と標準的なタンパク質検査の両方で確認されるほど頑健でした。さらに、チームが自身のタウを抑えたニューロンでV337Mタウを人工的に過剰発現させると、同じ低リン酸化状態が再現され、変異そのものが細胞内でタウの修飾のされ方を変えていることを示唆しました。
軸索とタウを形づくるシグナル経路
これらの変化を引き起こす要因を理解するため、研究者らはリン酸基を付加または除去する酵素の連鎖であるシグナル経路を探索しました。リン酸化プロテオミクスのデータは、ニューロンの突起成長に関与するタンパク質や、ニューロット伸展に影響を与えることが知られるp38 MAPキナーゼ経路を含む特定のキナーゼファミリーを示しました。続いて、数千の遺伝子を大規模CRISPRスクリーニングで上げ下げし、タウの重要なリン酸化形態の量を変えるものを同定しました。多くのヒットは細胞内骨格や軸索構造を組織する遺伝子であり、いくつかのp38経路の構成要素は特にV337Mニューロンにおけるタウのリン酸化に影響を及ぼしました。これは軸索を組み立てる機構とタウの化学的状態を調節する機構との密接な結びつきを示唆します。
認知症リスクの理解にとっての意味
総じて、これらの所見はV337Mタウ変異が古典的な意味でタウを単純により有毒にするわけではないことを示唆します。むしろ、非常に早期の段階でタウが軸索成長を支える通常の役割を弱め、タウのリン酸化のされ方を変えるように見えます。これはタウが減少または喪失した場合に起きる変化と重なる部分があります。発達期や若年成人期における微妙な配線の欠陥とタウ化学の持続的変化が組み合わさることで、MAPT変異を持つ人々が明白な認知症が出現する何十年も前から認知の違いを示す理由の一端を説明し得ます。本研究は、タウを幅広く低下させることを目的とした療法が若く健康なニューロンにおけるタウの有用な役割を考慮する必要があること、そしてタウ関連経路を単に遮断するのではなく慎重に調整することが一生涯にわたって脳を保護する鍵になりうることを強調します。
引用: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
キーワード: タウタンパク質, 前頭側頭型認知症, 軸索成長, 神経発達, タンパク質のリン酸化