Clear Sky Science · tr
MAPT V337M nöronlarının çok-omik fenotiplemesi aksonogenez ve tau fosforilasyonunda erken değişiklikleri ortaya koyuyor
Bu araştırma beyin sağlığı açısından neden önemli
Alzheimer hastalığı ve frontotemporal demans dahil birçok demans türünde, tau adı verilen bir proteinin beyin hücreleri içinde kümeler oluşturduğu görülür. Doktorlar anormal tau ile hafıza ve düşünme sorunlarının güçlü bir ilişki gösterdiğini biliyor, ancak tau’nun nasıl bozulduğu ve genç, hâlâ gelişmekte olan sinir hücrelerine ne yaptığı tam olarak net değildi. Bu çalışma, frontotemporal demansla ilişkilendirilen kalıtsal bir tau mutasyonuna odaklanıyor ve basit ama kritik bir soruyu soruyor: belirtiler ortaya çıkmadan çok önce nöronlara ne oluyor?
Riskli bir tau varyantına daha yakından bakış
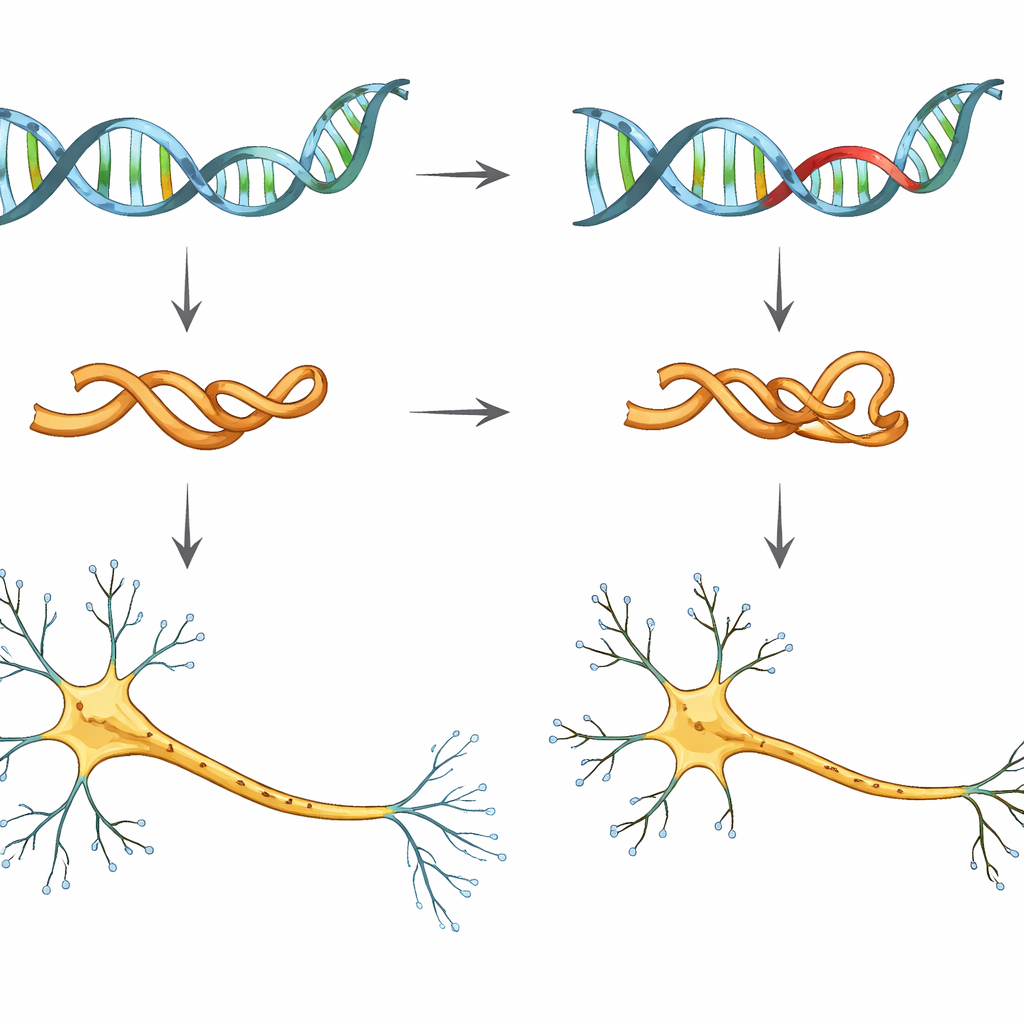
Araştırmacılar, tau için şablonu sağlayan MAPT genindeki V337M adlı tek bir genetik değişime odaklandı. Bu mutasyonu taşıyan kişiler genellikle orta yaşta frontotemporal demans geliştirir. Erken etkilerini incelemek için ekip, insan indüklenmiş pluripotent kök hücrelerini—erişkin hücrelerin embriyonik hücre gibi davranacak şekilde yeniden programlanması—nöronlara dönüştürdü. Normal tau taşıyan nöronları, bir veya iki kopya V337M mutasyonu taşıyan nöronları ve tau düzeylerinin kasten azaltıldığı nöronları karşılaştırdılar.
Birden çok moleküler ipucunu aynı anda izlemek
Sadece tek bir işareti takip etmek yerine bilim insanları “çok-omik” bir bakış benimsedi: gen aktivitesini (RNA dizilemesi), genleri kontrol eden DNA bölgelerinin açıklığını (ATAC-seq) ve binlerce protein ile onların kimyasal işaretlerini (proteomik ve fosfoproteomik) ölçtüler. Bu farklı katmanlar boyunca tutarlı bir mesaj ortaya çıktı. V337M mutasyonlu nöronlarda ve tau azaltılmış nöronlarda en güçlü değişiklikler aksonları—diğer hücrelere sinyal taşıyan uzun, kablo benzeri uzantıları—oluşturan ve şekillendiren genler ve proteinlerle ilgiliydi. Bu değişiklikler, hücre ölümü veya protein kümelenmesi gibi belirgin belirtilerden önce, nöronal gelişimin ilk haftaları içinde ortaya çıktı.
Genç nöronlar daha kısa, daha güçlü değil
Bu moleküler değişikliklerin hücre şeklini gerçekten etkileyip etkilemediğini görmek için ekip genç nöronların kültür kaplarında büyümesini izledi. Hücre zarlarını floresan bir işaretleyiciyle etiketleyip aksonları birkaç gün boyunca plak boyunca uzarken takip ettiler. V337M mutasyonlu nöronlar ve tau’su azaltılmış nöronlar, küçük yan dalların sayısı önemli ölçüde değişmemiş olsa da, belirgin şekilde daha kısa ana aksonlar ve daha az toplam uzantı üretti. Başka bir deyişle, nöronun merkezi “teli” gerektiği kadar uzaklaşamadı. Bu, hücreleri doğrudan öldüren belirgin toksik bir etkiden ziyade akson uzamasında tau’nun normal destek rolünün kaybuna işaret ediyor.
Beklenmedik bir tau kimyası deseni
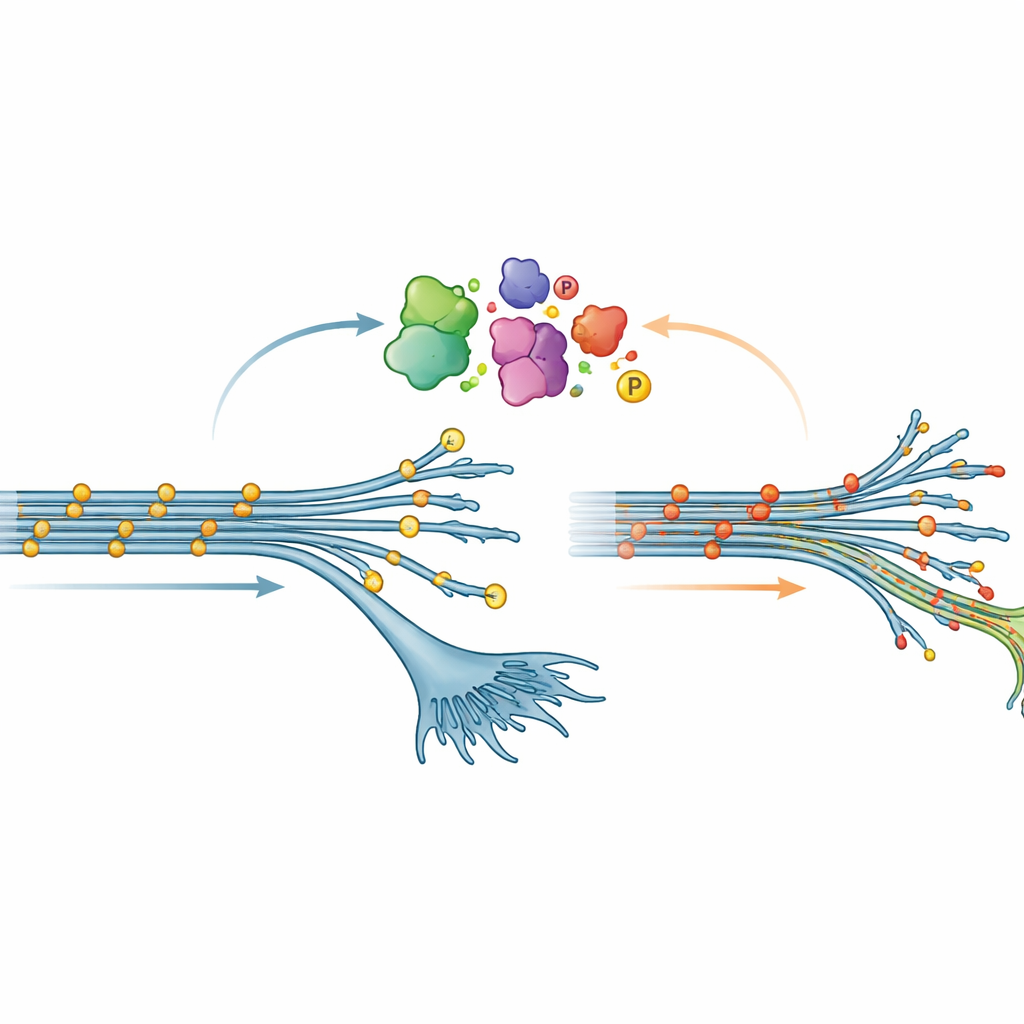
En şaşırtıcı keşiflerden biri fosforilasyonla ilgiliydi; bu, küçük fosfat gruplarının proteinlere eklenmesiyle gerçekleşen yaygın bir kimyasal değişiklik. Birçok beyin hastalığında tau yoğun olarak fosforile olur; bu genellikle tau’nun yumaklar oluşturmasını teşvik eden zararlı bir değişiklik olarak görülür. Oysa burada, erken evre V337M mutasyonlu nöronlar ters bir desen gösterdi: tau birçok bölgede normalden daha az fosforile olmuştu. Bu “hipofosforilasyon” nöronlar olgunlaştıkça yavaşça azaldı, ancak kütle spektrometrisi ve standart protein testleriyle doğrulanacak kadar güçlüydü. Ekip, kendi tau’su azaltılmış nöronlarda V337M tau’yu yapay olarak fazla ürettiğinde aynı düşük fosforilasyon durumu yeniden ortaya çıktı; bu da mutasyonun tau’nun hücre içindeki modifikasyon biçimini doğrudan yeniden şekillendirdiğini düşündürüyor.
Aksonları ve tau’yu yeniden şekillendiren sinyal yolları
Bu değişiklikleri neyin tetiklediğini anlamak için araştırmacılar, V337M nöronlarında değişmiş olan sinyal yollarını—fosfat gruplarını ekleyen veya çıkaran enzim zincirlerini—aramaya koyuldu. Fosfoproteomik verileri nöron projeksiyon büyümesiyle ilişkili proteinleri ve nörit büyümesini etkilediği bilinen p38 MAP kinaz yolu da dahil olmak üzere belirli kinaz ailelerini işaret etti. Ardından binlerce geni açıp kapatarak tau’nun ana fosforile formunun düzeyini değiştirenleri bulmak için geniş ölçekli CRISPR taramaları yaptılar. Çok sayıda sonuç, hücrenin iç iskeletini ve akson yapısını organize eden genlerdi ve birkaç p38 yolu bileşeni özellikle V337M nöronlarında tau fosforilasyonunu etkiledi. Bu, akson inşasını sağlayan mekanizma ile tau’nun kimyasal durumunu ayarlayan mekanizma arasında yakın bir bağ olduğunu öne sürüyor.
Bu bulgular demans riskini anlamak için ne anlama geliyor
Bir araya getirildiğinde, bulgular V337M tau mutasyonunun tau’yu klasik anlamda basitçe daha toksik hale getirmediğini gösteriyor. Bunun yerine, çok erken dönemde tau’nun akson büyümesini destekleyen normal işlevini zayıflatıyor ve tau’nun fosforilasyon şeklini değiştiriyor; bu etkiler tau azaltıldığında veya kaybedildiğinde görülenlerle örtüşüyor. Gelişim veya erken yetişkinlik sırasında oluşan ince devre kusurları—tau kimyasındaki süregelen değişimlerle birleştiğinde—MAPT mutasyonlarını taşıyan kişilerin açık demans ortaya çıkmadan onlarca yıl önce bilişsel farklılıklar göstermesini açıklamaya yardımcı olabilir. Bu çalışma, tau’yu genel olarak düşürmeyi hedefleyen tedavilerin genç ve sağlıklı nöronlardaki tau’nun yararlı rollerini dikkate alması gerektiğini ve tau ilişkili yolların basitçe engellenmesi yerine dikkatli bir ayarın, ömür boyu beyni korumak için anahtar olabileceğini vurguluyor.
Atıf: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Anahtar kelimeler: tau proteini, frontotemporal demans, akson büyümesi, nöronal gelişim, protein fosforilasyonu