Clear Sky Science · pt
Fenotipagem multiômica de neurônios MAPT V337M revela alterações iniciais em axonogênese e fosforilação da tau
Por que esta pesquisa importa para a saúde do cérebro
Muitas formas de demência, incluindo a doença de Alzheimer e a demência frontotemporal, envolvem aglomerados de uma proteína chamada tau dentro das células cerebrais. Os médicos observam que a tau anormal se correlaciona fortemente com problemas de memória e cognição, mas exatamente como a tau se altera — e o que isso faz a neurônios jovens ainda em desenvolvimento — permaneceu obscuro. Este estudo se concentra em uma mutação herdada da tau ligada à demência frontotemporal e faz uma pergunta simples, porém crucial: o que acontece aos neurônios muito antes do aparecimento dos sintomas?
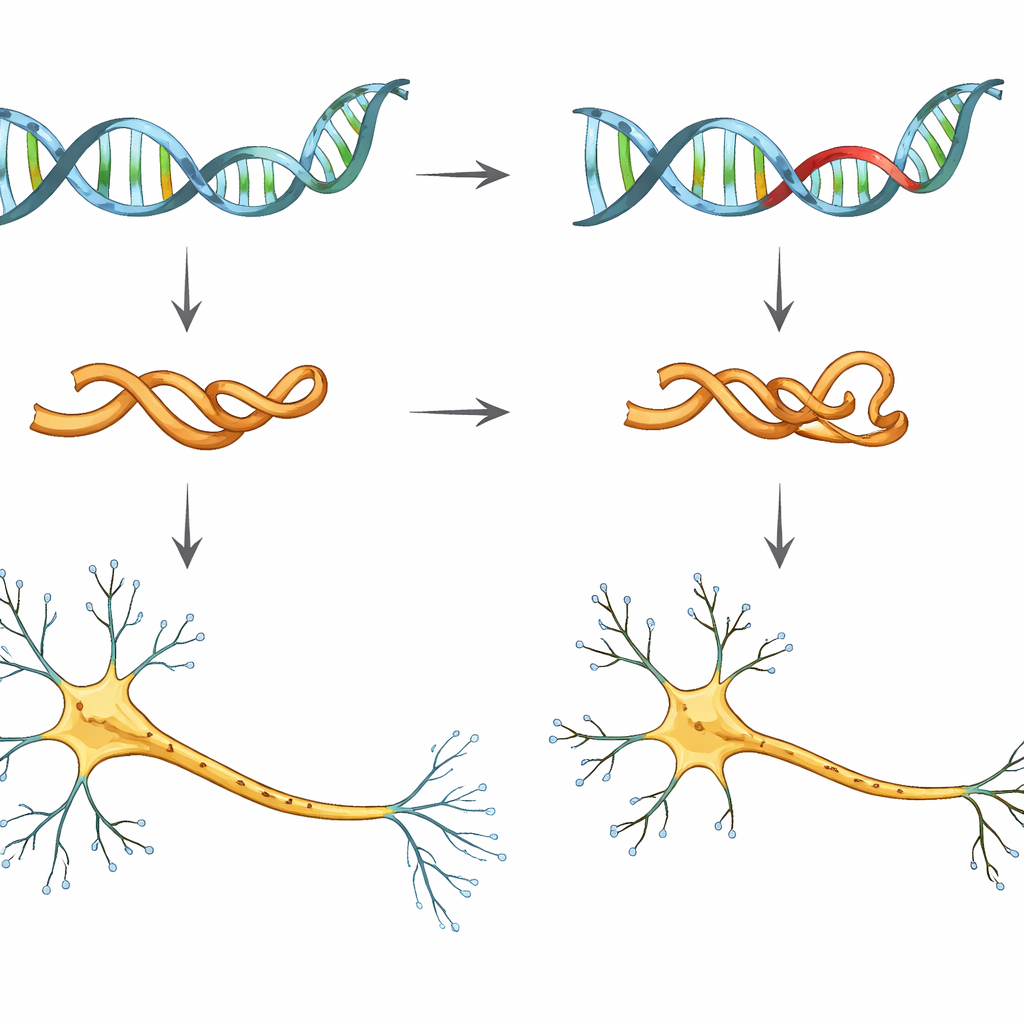
Um olhar mais atento sobre uma versão de risco da tau
Os pesquisadores focalizaram uma única alteração genética, chamada V337M, no gene MAPT, que fornece o projeto para a tau. Pessoas que carregam essa mutação têm quase certeza de desenvolver demência frontotemporal, frequentemente na meia-idade. Para estudar seus efeitos iniciais, a equipe usou células-tronco pluripotentes induzidas humanas — células adultas reprogramadas para se comportarem como células embrionárias — e as transformou em neurônios no laboratório. Eles compararam neurônios com tau normal, neurônios portadores de uma ou duas cópias da mutação V337M e neurônios nos quais os níveis de tau foram deliberadamente reduzidos.
Acompanhando várias pistas moleculares ao mesmo tempo
Em vez de acompanhar apenas um sinal, os cientistas adotaram uma visão “multiômica”: mediram a atividade gênica (sequenciamento de RNA), a acessibilidade de regiões do DNA que controlam genes (ATAC-seq) e milhares de proteínas e suas marcas químicas (proteômica e fosfoproteômica). Através dessas camadas diferentes, emergiu uma mensagem consistente. Em neurônios com a mutação V337M, e em neurônios com tau reduzida, as maiores alterações envolveram genes e proteínas que constroem e moldam os axônios — as longas projeções semelhantes a cabos que transmitem sinais para outras células. Essas mudanças surgiram cedo, nas primeiras semanas do desenvolvimento neuronal, antes de quaisquer sinais óbvios de morte celular ou aglomeração de proteínas.
Neurônios jovens crescem mais curtos, não mais fortes
Para verificar se essas mudanças moleculares realmente afetavam a forma celular, a equipe observou neurônios jovens crescendo em placas de cultura. Eles marcaram as membranas celulares com um marcador fluorescente e traçaram os axônios por vários dias enquanto se estendiam pela placa. Neurônios com a mutação V337M e neurônios com tau reduzida produziram axônios principais visivelmente mais curtos e menor crescimento total, apesar de o número de pequenos ramos laterais não ter sido dramaticamente alterado. Em outras palavras, o “fio” central do neurônio não alcançou a extensão esperada. Isso aponta para uma perda do papel de suporte normal da tau na extensão do axônio, em vez de um efeito tóxico óbvio que mata as células diretamente.
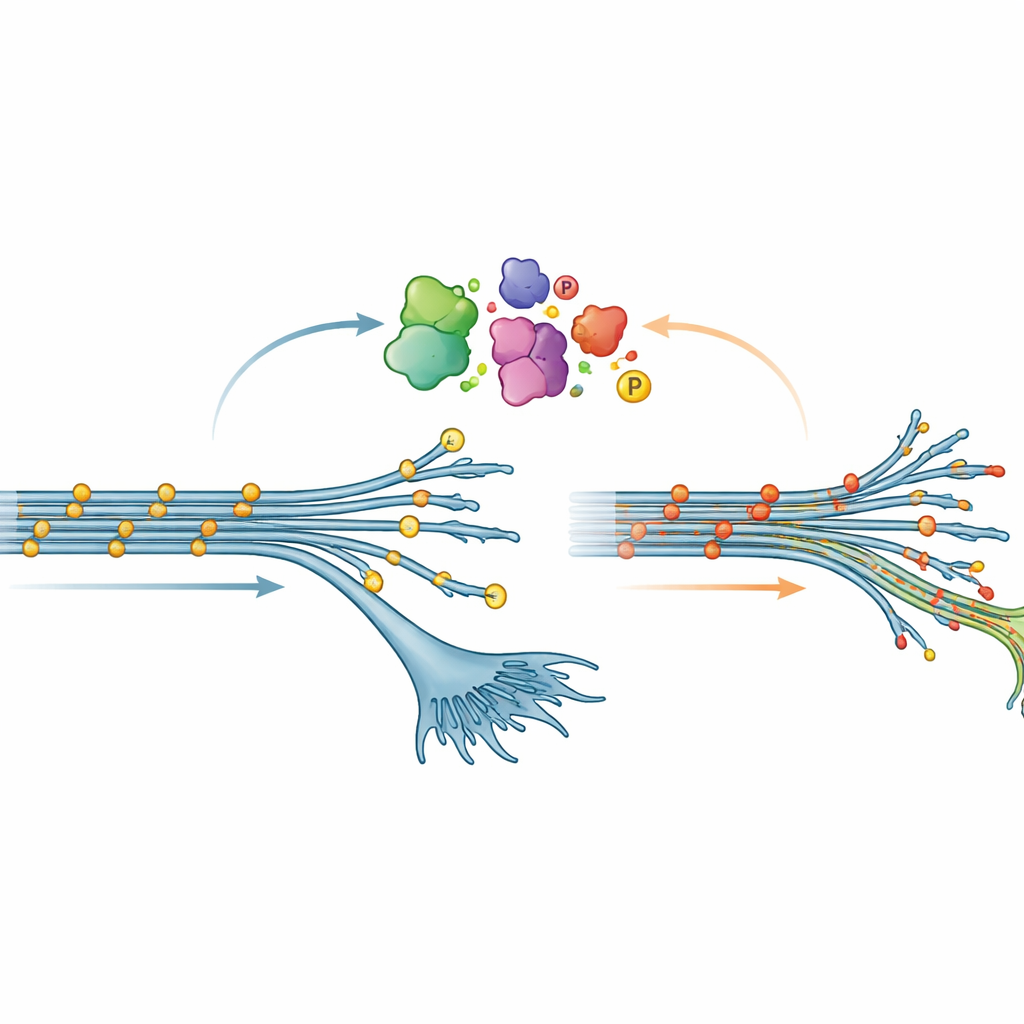
Um padrão inesperado na química da tau
Uma das descobertas mais surpreendentes diz respeito à fosforilação, uma modificação química comum em que pequenos grupos fosfato são anexados às proteínas. Em muitas doenças cerebrais, a tau se torna altamente fosforilada; isso costuma ser visto como uma alteração prejudicial que incentiva a formação de emaranhados. Aqui, porém, neurônios em estágio inicial portadores da mutação V337M mostraram o padrão oposto: a tau estava menos fosforilada em muitos sítios do que o normal. Essa “hipofosforilação” gradualmente diminuiu à medida que os neurônios amadureciam, mas foi consistente o suficiente para ser confirmada tanto por espectrometria de massa quanto por testes padrão de proteína. Quando a equipe superproduziu artificialmente a tau V337M em neurônios cuja tau endógena havia sido reduzida, o mesmo estado de baixa fosforilação reapareceu, sugerindo que a mutação por si só remodela como a tau é modificada dentro das células.
Cascatas de sinalização que remodelam axônios e a tau
Para entender o que impulsiona essas mudanças, os pesquisadores procuraram por vias de sinalização — cadeias de enzimas que adicionam ou removem grupos fosfato — que estavam alteradas em neurônios V337M. Seus dados de fosfoproteômica indicaram proteínas envolvidas no crescimento de projeções neuronais e famílias de quinases específicas, incluindo a via da MAP quinase p38, conhecida por influenciar o crescimento de neuritos. Em seguida, realizaram triagens CRISPR em larga escala, ativando ou desativando milhares de genes para ver quais mudavam o nível de uma forma fosforilada-chave da tau. Muitos alvos foram genes que organizam o esqueleto interno da célula e a estrutura do axônio, e vários componentes da via p38 afetaram a fosforilação da tau especificamente em neurônios V337M. Isso sugere uma ligação íntima entre a maquinaria que constrói axônios e a que ajusta o estado químico da tau.
O que isso significa para entender o risco de demência
Em conjunto, os achados sugerem que a mutação V337M na tau não simplesmente torna a tau mais tóxica no sentido clássico. Em vez disso, em estágios muito iniciais da vida parece reduzir o papel habitual da tau no suporte ao crescimento do axônio e altera como a tau é fosforilada, de maneiras que se sobrepõem ao que acontece quando a tau é reduzida ou perdida. Defeitos sutis de fiação durante o desenvolvimento ou início da idade adulta — combinados com mudanças contínuas na química da tau — podem ajudar a explicar por que pessoas portadoras de mutações no MAPT apresentam diferenças cognitivas décadas antes do surgimento claro da demência. Este trabalho ressalta que terapias visando reduzir amplamente a tau podem precisar considerar os papéis benéficos da tau em neurônios jovens e saudáveis, e que ajustar cuidadosamente, em vez de simplesmente bloquear, as vias relacionadas à tau pode ser a chave para proteger o cérebro ao longo da vida.
Citação: Mohl, G.A., Dixon, G., Marzette, E. et al. Multi-omic phenotyping of MAPT V337M neurons reveals early changes in axonogenesis and tau phosphorylation. npj Dement. 2, 24 (2026). https://doi.org/10.1038/s44400-026-00076-w
Palavras-chave: proteína tau, demência frontotemporal, crescimento do axônio, desenvolvimento neuronal, fosforilação de proteínas