Clear Sky Science · zh
压力下的细菌命运:脂质重塑与抗微生物肽攻击
这对抗击感染为何重要
随着越来越多细菌对我们现有的最佳抗生素产生耐药性,科学家们正转向天然防御分子——抗微生物肽,这类分子在从蜜蜂到人类的生物体内均有发现。但细菌并非被动靶标:它们可以重塑包裹细胞的油性膜,从而可能躲避这些新型药物。本研究提出了一个具有重大意义的实际问题:在细菌在压力下改变其膜脂质时,两种著名的抗微生物肽——来自蜜蜂毒液的melittin和人源的LL-37——还能否杀死它们,且具体通过何种方式实现?
处于压力下的细菌
细菌持续面临恶劣环境:温度或盐度变化、免疫攻击以及抗生素暴露。为应对这些挑战,它们会重新配置构成外界边界的脂肪分子(即脂质),调整膜的厚度、流动性和表面电荷等性质。一个关键的脂质构件——磷脂酸(phosphatidic acid),在正常情况下含量很低,但当其它带负电的脂质被耗尽时会积累。那些带负电的脂质通常是带正电的抗微生物肽的主要结合位点。作者使用了模式细菌大肠杆菌(Escherichia coli)及一株在很大程度上缺失两种主要阴性(带负电)脂质、由更多磷脂酸替代的突变株,以模拟药物压力下可能发生的膜脂质重塑。
两种肽,两种攻击风格
研究团队集中研究了melittin和LL-37,这两种经典的膜活性肽都具有螺旋形状,但亲水与疏水区的排列不同。利用结构预测工具和模型膜实验,他们发现两种肽不仅能与常见的阴性脂质结合,也能与磷脂酸结合,插入这些被改变的膜并扰乱其组织结构。melittin在使模型大肠杆菌膜发生泄漏方面表现得尤其强烈,而在相同条件下LL-37引起的直接泄漏较弱,暗示LL-37可能依赖于比简单在膜上打孔更为广泛的作用机制。
实时观察细胞死亡
为将膜损伤与实际细菌死亡联系起来,研究者并行运行了六种互补的检测方法。这些方法追踪肽与细胞表面的结合程度、外膜和内膜是否变得可渗透、内膜跨膜电位是否崩溃,以及细胞能量(ATP)和代谢酶活性如何变化。关键是,他们在正常大肠杆菌和脂质重塑突变株中同时测量这些效应,并计算仍能形成菌落的细胞数量。这产生了详细的“谱谱档”,显示哪些事件在什么肽浓度和时间下上升与饱和,有效地绘制出从首次接触到细胞死亡的路径图。
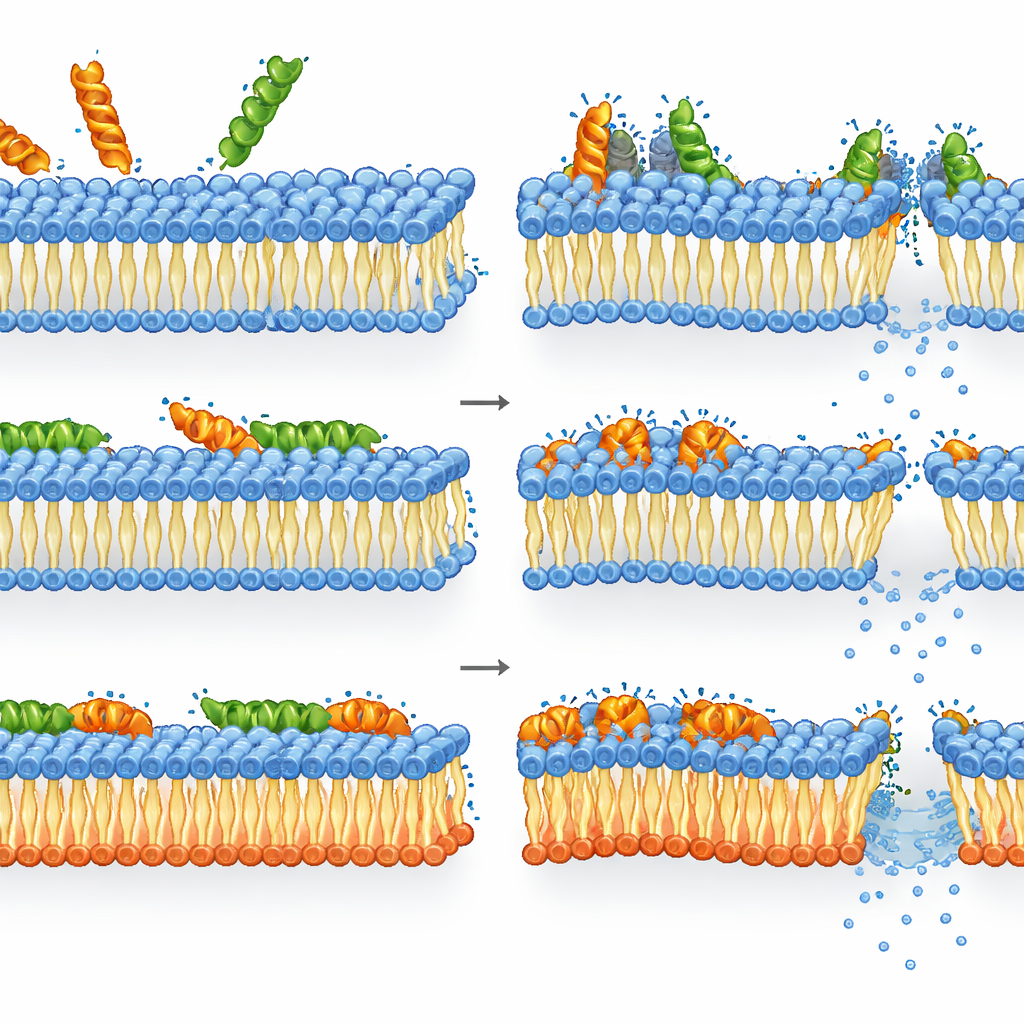
melittin和LL-37如何应对重塑后的膜
结果显示,melittin对缺乏常见阴性脂质的突变株甚至更具致死性。在突变株中,膜完整性的丧失、能量水平下降与存活能力丧失紧密相关:一旦melittin破坏了重塑后的膜,细胞便迅速死亡。然而在野生型中,情况更为复杂。膜通透性和去极化在某些浓度已达到饱和,但ATP与酶活性仍相对较高。换言之,许多细胞膜已严重受损但仍有代谢活性,无法形成菌落——这表明melittin的杀伤力来自于严重、可能是短暂的膜损伤,细胞无法完全恢复,即便其内部机器短时间内仍在运行。
更强韧、更具多面性的人人类肽
LL-37的表现则不同。它能中和表面电荷并在野生型与突变株中以几乎相同的程度损伤内外膜,表明其作用在很大程度上不依赖于阴性脂质的具体组合。在内外膜已被严重破坏的浓度下,许多细胞仍显示出可测的代谢活性,ATP水平也并不总是降为零。这种时序差距暗示,LL-37的最终致死作用可能涉及膜以外的靶点——例如干扰能量产生、触发氧化应激,或通过与DNA和核糖体结合使细胞质变得僵硬——一旦它进入细胞内部即可发挥这些作用。
对未来抗微生物剂的启示
总体而言,这项研究表明,膜脂质重塑——即便是从常见阴性脂质向磷脂酸发生剧烈转变——也不能使细菌逃脱melittin或LL-37的杀伤。两种肽都能适应新的脂质环境,继续结合、插入并最终致死。详细的检测谱谱显示,细菌死亡并非在膜被穿透瞬间的简单开关,而是一系列重叠事件的网络,这些事件可以在所有代谢信号消失之前就使细胞受损并失去生长能力。通过将具体的膜和存活标志与实际杀伤联系起来,这项工作为如何评估和比较新型抗微生物肽提供了蓝图,并表明仅靠改变膜脂质组成,细菌难以轻易躲避这些强效、多面向的分子。
引用: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
关键词: 抗微生物肽, 细菌膜, 脂质重塑, 抗生素耐药性, LL-37 与蜜蜂毒素肽(melittin)