Clear Sky Science · ru
Судьба бактериальной клетки при стрессе: перестройка липидов и атака антимикробных пептидов
Почему это важно в борьбе с инфекциями
По мере того как всё больше бактерий становятся устойчивыми к нашим лучшим антибиотикам, учёные обращают внимание на природные молекулы защиты — антимикробные пептиды, встречающиеся у организмов от пчёл до человека. Но бактерии не являются пассивными мишенями: они могут перестраивать маслянистую мембрану вокруг своих клеток и тем самым потенциально ускользать от этих новых препаратов. В этой работе поставлен практический вопрос с серьёзными последствиями: когда бактерии меняют липиды мембраны под стрессом, могут ли два хорошо изученных антимикробных пептида — мелиттин из яда медоносной пчелы и человеческий LL-37 — по-прежнему их убивать, и как именно это происходит?
Бактерии под давлением
Бактерии постоянно сталкиваются с жесткими условиями: изменениями температуры или солёности, атаками иммунной системы и воздействием антибиотиков. Чтобы справиться, они перенастраивают жирные молекулы, или липиды, формирующие их внешний барьер, регулируя такие свойства, как толщина, текучесть и заряд поверхности. Ключевой строительный блок липидов — фосфатидная кислота — при нормальных условиях присутствует лишь в следовых количествах, но может накапливаться, когда другие анионные (отрицательно заряженные) липиды истощаются. Эти заряженные липиды обычно служат основными точками притяжения для положительно заряженных антимикробных пептидов. Авторы использовали модельную бактерию Escherichia coli и мутантный штамм, практически лишённый двух основных анионных липидов и заменивший их повышенным содержанием фосфатидной кислоты, чтобы смоделировать перестройку мембраны, которая может происходить под давлением препаратов.
Два пептида, два стиля атаки
Команда сосредоточилась на мелиттине и LL-37 — классических мембраноактивных пептидах, которые имеют спиральную структуру, но отличаются расположением гидрофильных и гидрофобных областей. С помощью инструментов предсказания структуры и модельных мембран они показали, что оба пептида могут связываться не только с обычными анионными липидами, но и с фосфатидной кислотой, внедряться в эти изменённые мембраны и нарушать их организацию. Мелиттин оказался особенно эффективным в создании проницаемости в модельных мембранах E. coli, тогда как LL-37 при тех же условиях вызывал более слабую прямую утечку, что наводит на мысль о том, что он может опираться на более широкий набор механизмов, чем простое проделывание дырок в мембране.
Наблюдая гибель клеток в реальном времени
Чтобы связать повреждение мембраны с реальной гибелью бактерий, исследователи провели шесть взаимодополняющих тестов параллельно. Они отслеживали, насколько хорошо пептиды связываются с поверхностью клетки, становятся ли проницаемыми внешняя и внутренняя мембраны, не обрушился ли электрический потенциал через внутреннюю мембрану и как меняются уровень энергии (АТФ) и активность метаболических ферментов. Важно, что эти эффекты измерялись как для нормальной E. coli, так и для мутанта с перестроенными липидами, параллельно подсчитывая число клеток, способных образовывать колонии. Это позволило получить детализированные «профили», показывающие, какие события возникают и насыщаются при каких концентрациях пептидов и во времени, фактически картируя путь от первого контакта до гибели клетки.
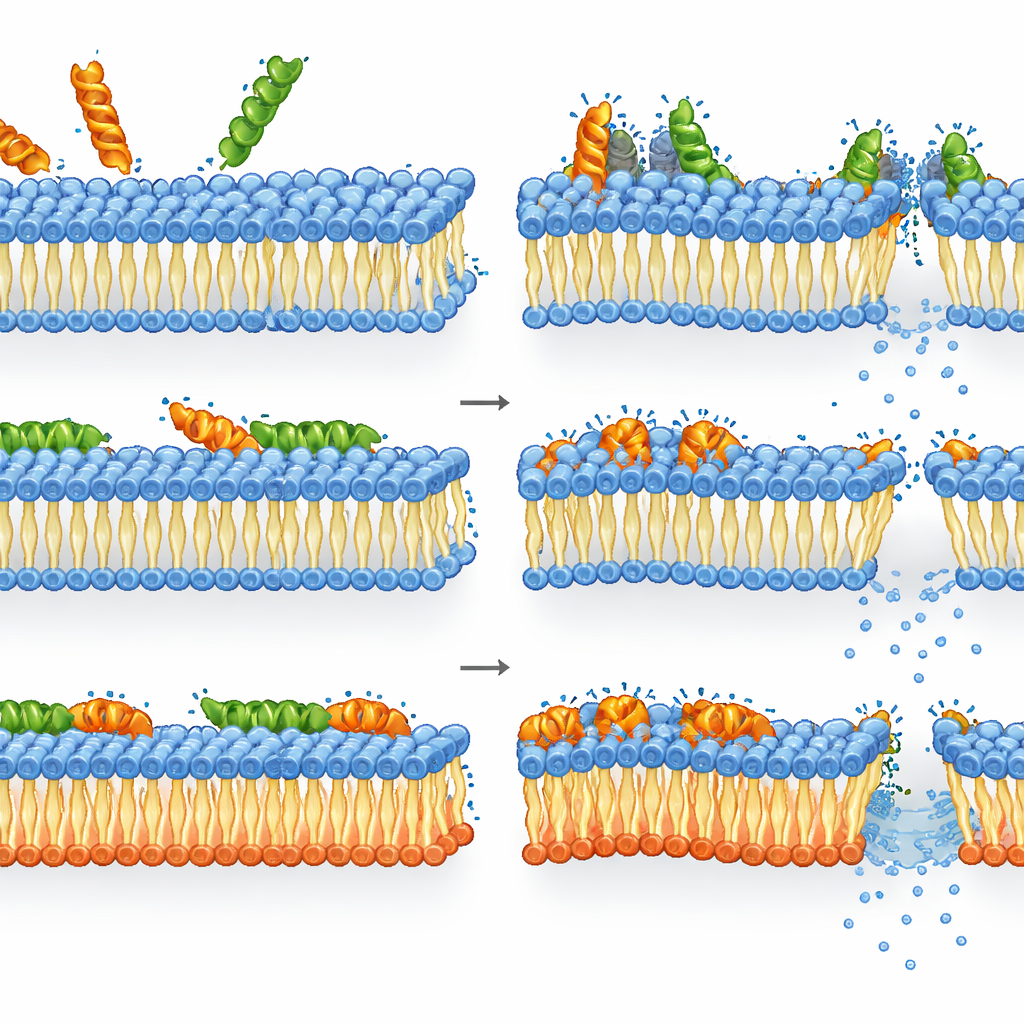
Как мелиттин и LL-37 справляются с перестроенными мембранами
Мелиттин оказался ещё более летальным для бактерий, лишённых обычных анионных липидов, чем для дикого штамма. У мутанта потеря целостности мембраны, снижение энергетического состояния и утрата жизнеспособности были тесно связаны: как только мелиттин нарушал перестроенную мембрану, клетки быстро умирали. У дикого штамма картина была более сложной. Проницаемость мембраны и деполяризация уже достигали насыщения при концентрациях, при которых уровни АТФ и активность ферментов оставались относительно высокими. Иными словами, многие клетки имели серьёзно повреждённые мембраны, но всё ещё были метаболически активны, хотя не могли образовывать колонии — что предполагает, что убивающая сила мелиттина связана с тяжёлым, возможно временным повреждением мембраны, от которого клетки не в состоянии полностью восстановиться, даже если их внутренняя «машинерия» на короткое время продолжает работать.
Более выносливый и универсальный человеческий пептид
LL-37 вёл себя иначе. Он нейтрализовал поверхностный заряд и повреждал обе мембраны у дикого типа и у мутанта практически в одинаковой степени, что указывает на то, что его действие в значительной степени не зависит от точного состава анионных липидов. При концентрациях, когда внутренняя и внешняя мембраны уже были сильно скомпрометированы, многие клетки по-прежнему показывали измеримую метаболическую активность, и уровни АТФ не всегда падали до нуля. Этот разрыв во времени подразумевает, что окончательный удар LL-37, скорее всего, включает мишени за пределами самой мембраны — например, нарушение генерации энергии, вызов окислительного стресса или уплотнение цитоплазмы за счёт связывания с ДНК и рибосомами — когда он уже проник в клеточную внутренность.
Что это значит для будущих антимикробных средств
В целом исследование показывает, что перестройка мембраны — даже радикальные сдвиги от обычных анионных липидов в сторону фосфатидной кислоты — не спасает бактерии от мелиттина или LL-37. Оба пептида адаптируются к новому липидному ландшафту, всё ещё связываются, внедряются и в конечном счёте убивают. Детализированные профили тестов показывают, что гибель бактерий не является простым выключателем в момент пробития мембраны, а представляет собой сеть перекрывающихся событий, которые могут оставить клетки повреждёнными и неспособными к росту задолго до того, как все метаболические сигналы исчезнут. Связывая конкретные маркеры мембраны и жизнеспособности с фактическим убийством, эта работа даёт шаблон для оценки и сравнения новых антимикробных пептидов и говорит о том, что простая смена состава липидов мембраны вряд ли станет лёгким путём ухода для бактерий, столкнувшихся с этими мощными, многосоставными молекулами.
Цитирование: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Ключевые слова: антимикробные пептиды, бактериальные мембраны, перестройка липидов, антибиотикорезистентность, LL-37 и мелиттин