Clear Sky Science · tr
Stres altında bakteriyel hücre kaderi: lipid yeniden düzenlenmesi ve antimikrobiyal peptit saldırısı
Neden enfeksiyonlarla mücadelede önemli
Daha fazla bakteri en iyi antibiyotiklerimize direnç kazandıkça, bilim insanları arıdan insana kadar çeşitli canlılarda bulunan doğal savunma molekülleri olan antimikrobiyal peptitlere yöneliyor. Ancak bakteriler pasif hedefler değil: hücrelerini çevreleyen yağlı zarı yeniden düzenleyerek bu yeni ilaçlardan kaçabilirler. Bu çalışma pratik ve geniş etkileri olan bir soruyu gündeme getiriyor: bakteriler strese yanıt olarak zar lipidlerini değiştirdiklerinde, iki iyi bilinen antimikrobiyal peptit—bal arısı zehrinden melittin ve insan LL-37—hala onları öldürebiliyor mu ve bunu tam olarak nasıl yapıyorlar?
Baskı altındaki bakteriler
Bakteriler sürekli olarak zorlu koşullarla karşılaşıyor: sıcaklık veya tuz değişimleri, bağışıklık saldırıları ve antibiyotik maruziyeti. Başa çıkmak için dış sınırlarını oluşturan yağ moleküllerini, yani lipidleri yeniden yapılandırır; kalınlık, akışkanlık ve yüzey yükü gibi özellikleri ayarlarlar. Anahtar bir lipid yapı taşı olan fosfatidik asit, normalde çok az miktarda bulunurken, diğer negatif yüklü lipidler tükenince birikebilir. Bu yüklü lipidler genellikle pozitif yüklü antimikrobiyal peptitlerin öncelikli bağlanma bölgeleridir. Yazarlar, model bakteri Escherichia coli ve iki ana anyonik (negatif yüklü) lipidten büyük ölçüde yoksun olan, bunların yerine daha fazla fosfatidik asit içeren bir mutant suş kullandılar; bu, ilaç baskısı altında meydana gelebilecek türde zar yeniden düzenlenmesini taklit ediyor.
İki peptit, iki saldırı tarzı
Çalışma ekibi melittin ve LL-37’ye odaklandı; her ikisi de heliks biçimli klasik membran-aktif peptitler ancak suyu seven ve yağı seven bölgelerinin düzenlenişi farklı. Yapı tahmin araçları ve model zarlar kullanarak her iki peptidin sadece olağan anyonik lipidlere değil aynı zamanda fosfatidik asite de bağlanabildiğini, bu değişmiş zarların içine yerleşerek organizasyonlarını bozduğunu gösterdiler. Melittin, model E. coli zarlarını sızıntılı hâle getirmede özellikle güçlü olduğunu kanıtladı; LL-37 ise aynı koşullar altında daha zayıf doğrudan sızıntı gösterdi ve bunun membranda basit delik açmaktan daha geniş bir etki repertuarına dayanabileceğine işaret etti.
Hücrelerin gerçek zamanlı ölmesini izlemek
Membran hasarını gerçek bakteriyel ölümle ilişkilendirmek için araştırmacılar altı tamamlayıcı testi yan yana çalıştırdı. Bunlar peptitlerin hücre yüzeyine ne kadar bağlandığını, dış ve iç zarların geçirgen hale gelip gelmediğini, iç zar üzerindeki elektriksel potansiyelin çöküp çökmediğini ve hücrelerin enerji (ATP) ile metabolik enzim faaliyetinin nasıl değiştiğini izledi. Kritik olarak, bu etkileri hem normal E. coli’de hem de lipidleri yeniden düzenlenmiş mutantta ölçtular ve aynı zamanda kaç hücrenin hâlâ koloni oluşturabildiğini saydılar. Bu, hangi olayların hangi peptit konsantrasyonlarında ve zamanlarda arttığını ve doyuma ulaştığını gösteren ayrıntılı “profil”ler üretti; böylece ilk temasdan hücre ölümüne giden yol haritalandı.
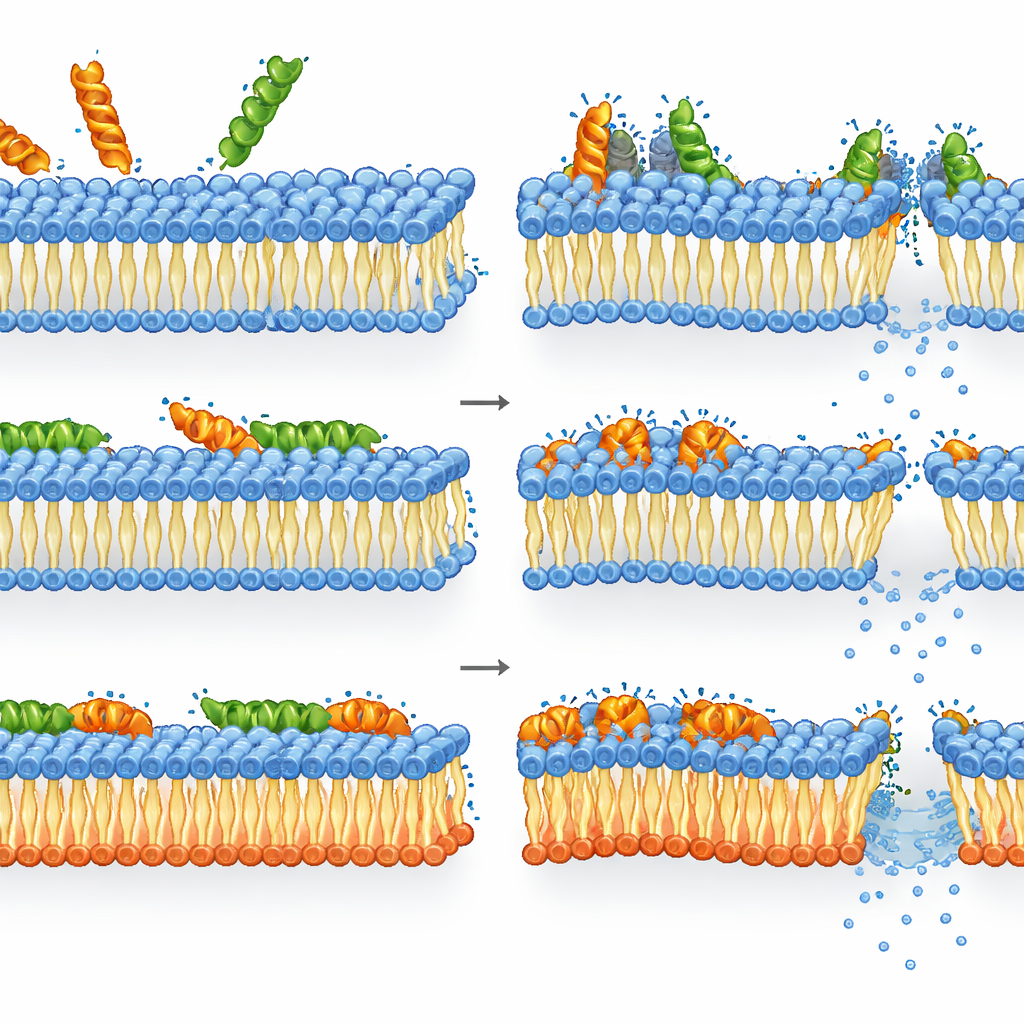
Melittin ve LL-37’nin yeniden düzenlenmiş zarlarla başa çıkma biçimi
Melittin, olağan anyonik lipidlere sahip olmayan bakterilere karşı vahşi tipe göre daha ölümcül çıktı. Mutantta, zar bütünlüğünün yitirilmesi, enerji düzeylerinin düşmesi ve canlılığın kaybı sıkı bir şekilde bağlantılıydı: melittin yeniden düzenlenmiş zarı bozduğunda hücreler hızla öldü. Ancak vahşi tipte durum daha nüanslıydı. Membran geçirgenliği ve depolarizasyon, ATP ve enzim aktivitesinin hâlâ nispeten yüksek kaldığı konsantrasyonlarda bile doygunluğa ulaşmıştı. Başka bir deyişle, birçok hücre ciddi şekilde zarar görmüş zarlara rağmen hâlâ metabolik olarak aktifti fakat koloni oluşturamıyordu—bu, melittin’in öldürücü gücünün hücrelerin tamamen toparlanamayacağı şiddetli, muhtemelen geçici membran hasarından kaynaklandığını; iç makineler kısa süreli çalışmaya devam etse bile geri döndürülemez zarar verdiğini düşündürüyor.
Daha zorlu, daha çok yönlü bir insan peptidi
LL-37 farklı davrandı. Yüzey yükünü nötralize etti ve hem vahşi tip hem de mutant hücrelerde iki zara neredeyse aynı ölçüde zarar verdi; bu da etkinliğinin belirli anyonik lipid karışımından büyük ölçüde bağımsız olduğunu gösteriyor. İç ve dış zarların zaten ağır şekilde zarar gördüğü konsantrasyonlarda bile birçok hücre ölçülebilir metabolik aktivite gösterdi ve ATP düzeyleri her zaman sıfıra inmiyordu. Bu zamanlama farkı, LL-37’nin son öldürücü darbesinin muhtemelen zarın ötesinde hedefleri içerdiğini ima ediyor—örneğin enerji üretimini bozmak, oksidatif stresi tetiklemek veya DNA ve ribozomlara bağlanarak sitoplazmayı sertleştirmek gibi—peptid hücre içine eriştikten sonra ortaya çıkan etkiler.
Gelecekteki antimikrobiyaller için anlamı
Genel olarak, çalışma gösteriyor ki zar yeniden düzenlenmesi—olağan anyonik lipitlerden fosfatidik asite doğru yapılan köklü kaymalar bile—bakterileri melittin veya LL-37’den kurtarmıyor. Her iki peptit de yeni lipid manzarasına uyum sağlıyor, bağlanıyor, giriyor ve nihayetinde öldürüyor. Ayrıntılı test profilleri, bakteriyel ölümün zar delinmesi anındaki basit bir açık-kapalı anahtar olmadığını, metabolik sinyaller tamamen yok olmadan çok önce hücreleri hasarlı ve büyümeyen hâle getirebilen örtüşen olaylar ağı olduğunu ortaya koyuyor. Belirli membran ve canlılık belirteçlerini gerçek öldürme ile ilişkilendirerek, bu çalışma yeni antimikrobiyal peptitleri değerlendirmek ve karşılaştırmak için bir kılavuz sunuyor ve yalnızca zar lipid bileşimini değiştirmeyi, bu güçlü, çok yönlü moleküllerle karşılaşan bakteriler için kolay bir kaçış yolu olarak görmenin muhtemelen yanlış olduğunu öne sürüyor.
Atıf: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Anahtar kelimeler: antimikrobiyal peptitler, bakteriyel zarlar, lipid yeniden düzenlenmesi, antibiyotik direnci, LL-37 ve melittin