Clear Sky Science · ja
ストレス下の細菌の運命:脂質のリモデリングと抗菌ペプチドの攻撃
感染症対策でなぜ重要か
多くの細菌が主要な抗生物質に対して耐性を獲得する中で、研究者はミツバチから人間までの生物に見られる天然の防御分子、抗菌ペプチドに注目しています。しかし細菌は受動的な標的ではなく、細胞を包む脂質の膜をリモデリングしてこれらの新しい薬剤を回避する可能性があります。本研究は実用的かつ重要な問いを投げかけます:細菌がストレス下で膜脂質を変化させたとき、ミツバチ毒由来のメリチンとヒト由来のLL-37という二つのよく知られた抗菌ペプチドは依然として殺菌できるのか、そしてその具体的な作用機序は何か?
圧力にさらされる細菌
細菌は常に厳しい環境に直面しています:温度や塩濃度の変化、免疫の攻撃、抗生物質への暴露。対処するために、彼らは外側の境界を構成する脂肪分子(脂質)を再構成し、膜の厚さ、流動性、表面電荷といった性質を調整します。主要な脂質の前駆体であるホスファチジン酸は通常ごく少量しか存在しませんが、他の負に帯電した脂質が減少すると蓄積することがあります。これらの負電荷を持つ脂質は通常、陽イオン性の抗菌ペプチドの主要な結合部位です。著者らはモデル細菌の大腸菌と、二種類の主要な陰イオン性脂質をほとんど欠く変異株を用い、それらをホスファチジン酸で置き換えることで、薬剤圧によって起こり得る膜のリモデリングを模倣しました。
二つのペプチド、二通りの攻め方
研究チームはメリチンとLL-37に着目しました。これらはどちらもヘリカルな形状を持つ典型的な膜作用性ペプチドですが、親水性領域と疎水性領域の配置に違いがあります。構造予測ツールとモデル膜を用いて、両ペプチドが通常の陰イオン性脂質に結合するだけでなくホスファチジン酸にも結合し、これら変化した膜に挿入して膜の秩序を乱すことを示しました。メリチンはモデルの大腸菌膜を漏れやすくする点で特に強力でしたが、同じ条件下でLL-37は直接的な漏洩作用が弱く、単純な膜の穴開け以上に幅広い作用を頼る可能性を示唆しました。
細胞が死ぬ過程をリアルタイムで観察
膜損傷と実際の細菌死を結び付けるために、研究者らは六つの補完的なアッセイを並行して実施しました。これらはペプチドがどれだけ細胞表面に結合するか、外膜と内膜が透過性を帯びるか、内膜の電位が崩れるか、細胞のエネルギー(ATP)や代謝酵素活性がどう変化するかを追跡します。重要なのは、これらの効果を通常型大腸菌と脂質リモデリング変異株の双方で測定し、同時にコロニー形成可能な細胞数も数えた点です。こうして、どの事象がどのペプチド濃度・時間で上昇し飽和するかを示す詳細な“プロファイル”が得られ、初接触から細胞死に至る道筋がマッピングされました。
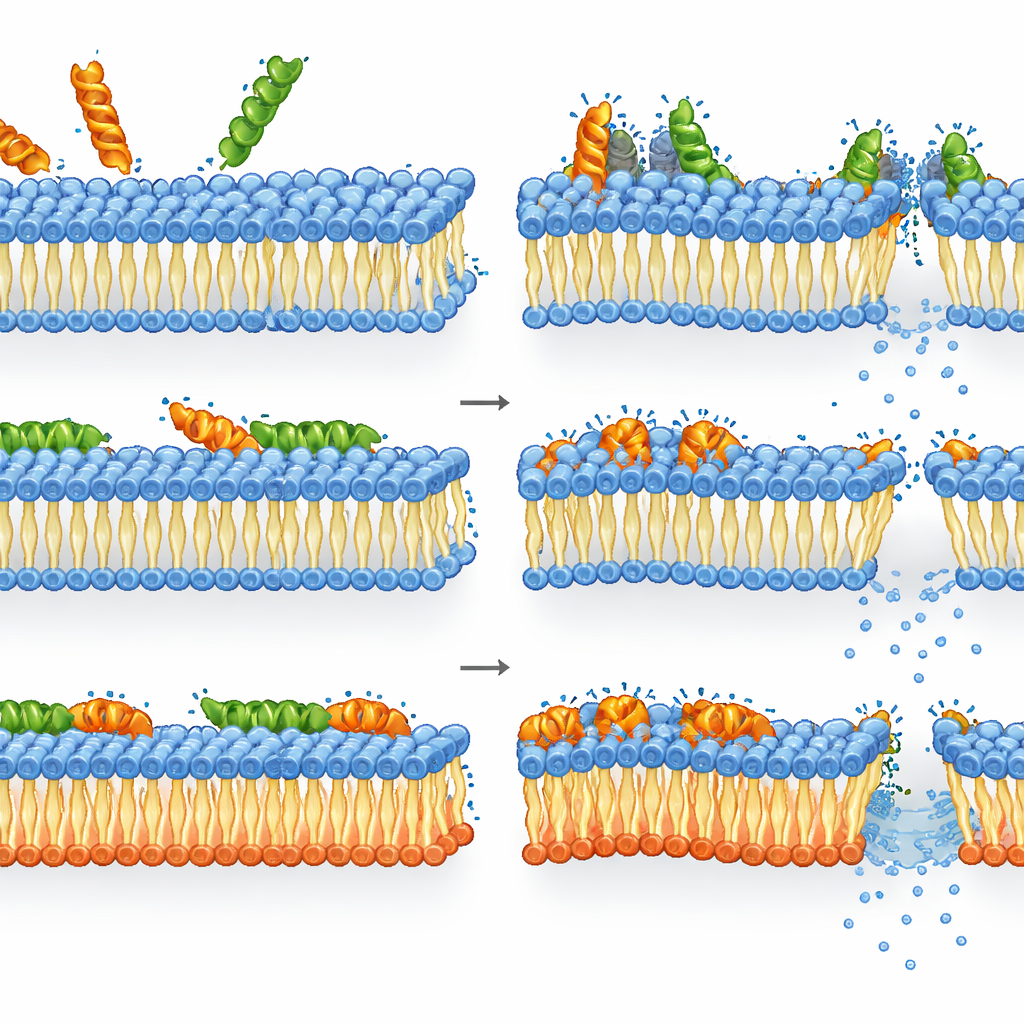
リモデリング膜に対するメリチンとLL-37の振る舞い
メリチンは、通常の陰イオン性脂質を欠く変異株に対してむしろ強い致死性を示しました。変異株では膜の一体性喪失、エネルギー低下、失活が密接に結び付いており、メリチンがリモデリングされた膜を破壊すると細胞は急速に死に至りました。一方で野生株では状況はより複雑でした。膜の透過性や脱分極は既に飽和している濃度でも、ATPや酵素活性は比較的高いままでした。つまり、多くの細胞は膜が大きく損傷しているにもかかわらず代謝的にはまだ活動的であり、コロニー形成ができない—これはメリチンの殺菌効果が細胞が完全に回復できないような深刻でおそらく一過性の膜損傷に由来し、内部の機能は短時間ならまだ動き続ける可能性があることを示唆します。
より手強く多才なヒト由来ペプチド
LL-37は異なる振る舞いを示しました。表面電荷を中和し、野生株と変異株の両方で外膜と内膜の損傷をほぼ同程度に引き起こし、その作用が陰イオン性脂質の正確な組成に大きく依存しないことを示しました。内外膜が既に大きく損なわれている濃度でも、多くの細胞は測定可能な代謝活性を示し、ATPレベルが常にゼロに落ちるわけではありませんでした。このタイミングのずれは、LL-37の最終的な致死作用が膜以外の標的—例えばエネルギー産生の攪乱、酸化ストレスの誘導、DNAやリボソームへの結合による細胞質の硬化—などを含む可能性が高いことを示唆しています。一度細胞内に到達すると、これらの追加標的が致命的な役割を果たすと考えられます。
将来の抗菌剤にとっての意味
総じて、本研究は膜のリモデリング—通常の陰イオン性脂質からホスファチジン酸への大きなシフトであっても—がメリチンやLL-37から細菌を救うことはないことを示しています。両ペプチドは新しい脂質環境に適応し、依然として結合・挿入し、最終的に細胞を殺します。詳細なアッセイプロファイルは、細菌死が膜が破られた瞬間の単純なオン/オフではなく、代謝信号が消えるよりずっと前に細胞を損傷し増殖不能にする重なり合う一連の事象であることを明らかにします。特定の膜指標と生存性指標を実際の殺菌と結びつけることで、この研究は新しい抗菌ペプチドを評価・比較するための設計図を提供しており、膜脂質組成の単純な変化がこれら強力で多面的な分子に対する細菌の容易な逃避経路にはならないことを示唆しています。
引用: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
キーワード: 抗菌ペプチド, 細菌膜, 脂質リモデリング, 抗生物質耐性, LL-37 とメリチン