Clear Sky Science · pt
Destino da célula bacteriana sob estresse: remodelação lipídica e ataque de peptídeos antimicrobianos
Por que isso importa no combate às infecções
À medida que mais bactérias se tornam resistentes aos nossos melhores antibióticos, cientistas recorrem a moléculas naturais de defesa chamadas peptídeos antimicrobianos, encontradas em organismos que vão de abelhas a humanos. Mas as bactérias não são alvos passivos: elas podem remodelar a camada oleosa que envolve suas células, potencialmente escapando desses novos fármacos. Este estudo faz uma pergunta prática com grandes implicações: quando as bactérias alteram seus lipídios de membrana sob estresse, dois peptídeos antimicrobianos bem conhecidos — melittina do veneno da abelha e LL-37 humano — ainda conseguem matá-las, e como exatamente fazem isso?
Bactérias sob pressão
As bactérias enfrentam constantemente condições adversas: variações de temperatura ou salinidade, ataques do sistema imune e exposição a antibióticos. Para sobreviver, elas reconfiguram as moléculas gordurosas, ou lipídios, que formam sua fronteira externa, ajustando propriedades como espessura, fluidez e carga de superfície. Um bloco lipídico chave, o ácido fosfatídico, normalmente presente apenas em quantidades pequenas, pode acumular-se quando outros lipídios carregados negativamente são reduzidos. Esses lipídios carregados costumam ser os principais pontos de ancoragem para peptídeos antimicrobianos carregados positivamente. Os autores usaram a bactéria modelo Escherichia coli e uma linhagem mutante que praticamente não contém dois lipídios aniônicos principais, substituindo-os por mais ácido fosfatídico, para imitar o tipo de remodelação de membrana que pode ocorrer sob pressão de drogas.
Dois peptídeos, dois estilos de ataque
A equipe concentrou-se na melittina e no LL-37, peptídeos clássicos que atuam na membrana, que compartilham uma forma helicoidal, mas diferem em como suas regiões hidrofílicas e hidrofóbicas estão organizadas. Usando ferramentas de predição estrutural e membranas modelo, eles mostraram que ambos os peptídeos podem se ligar não apenas aos lipídios aniônicos habituais, mas também ao ácido fosfatídico, inserindo-se nessas membranas alteradas e perturbando sua organização. A melittina mostrou-se especialmente poderosa em tornar as membranas modelo de E. coli permeáveis, enquanto o LL-37 mostrou vazamento direto mais fraco nas mesmas condições, sugerindo que ele pode depender de um conjunto mais amplo de ações além de simplesmente perfurar a membrana.
Observando as células morrerem em tempo real
Para conectar o dano à membrana com a morte bacteriana real, os pesquisadores realizaram seis ensaios complementares lado a lado. Esses ensaios acompanharam quão bem os peptídeos se ligavam à superfície celular, se as membranas externa e interna se tornaram permeáveis, se o potencial elétrico através da membrana interna colapsou e como a energia (ATP) e a atividade de enzimas metabólicas das células mudaram. Crucialmente, mediram esses efeitos tanto em E. coli normal quanto no mutante com membrana remodelada, enquanto também contavam quantas células ainda podiam formar colônias. Isso produziu "perfis" detalhados mostrando quais eventos aumentavam e saturavam em quais concentrações e tempos dos peptídeos, mapeando efetivamente a estrada do primeiro contato até a morte celular.
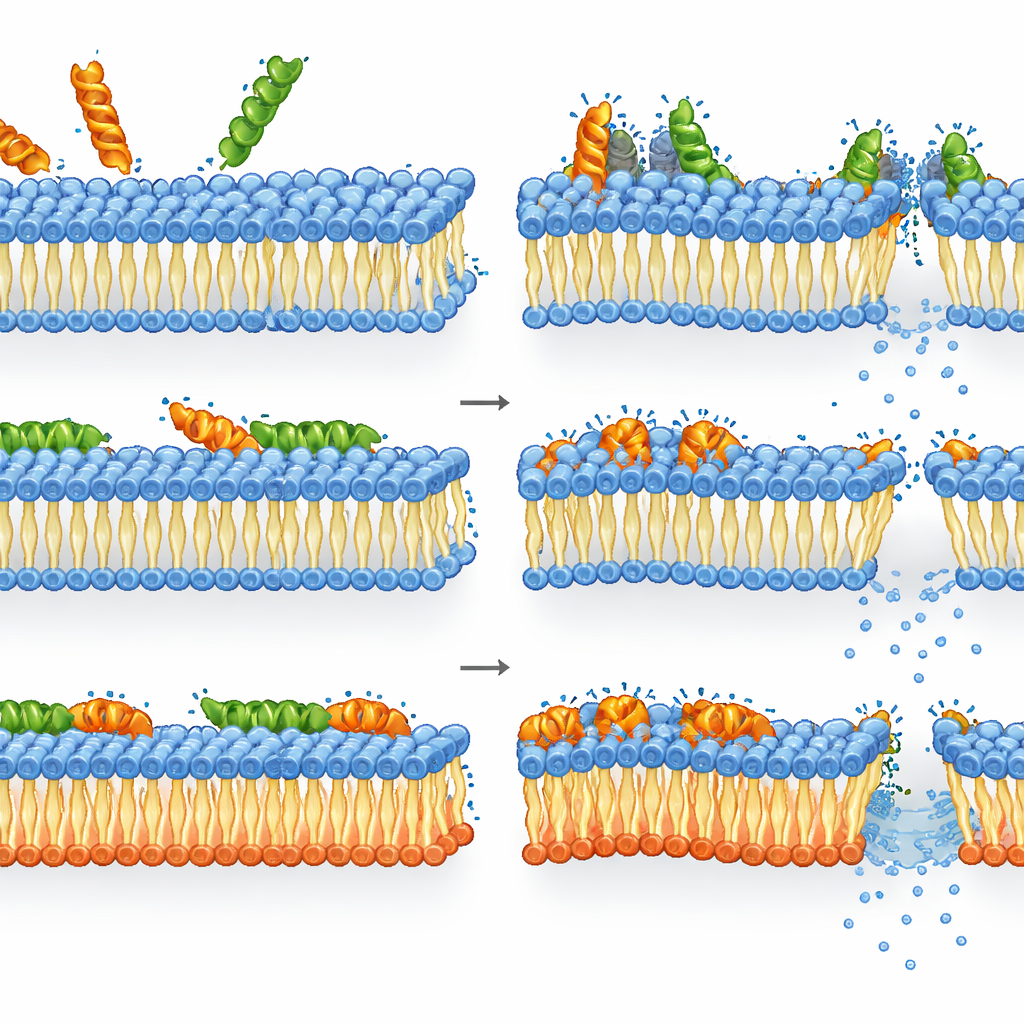
Como melittina e LL-37 lidam com membranas remodeladas
A melittina revelou-se ainda mais letal contra bactérias que não tinham os lipídios aniônicos habituais do que contra o tipo selvagem. No mutante, perda da integridade da membrana, queda dos níveis de energia e perda de viabilidade estavam fortemente ligadas: uma vez que a melittina desorganizou a membrana remodelada, as células morreram rapidamente. No tipo selvagem, contudo, o quadro foi mais nuançado. A permeabilização e a despolarização da membrana já estavam saturadas em concentrações em que ATP e atividade enzimática permaneciam relativamente altas. Em outras palavras, muitas células tinham membranas gravemente danificadas, mas ainda estavam metabolicamente ativas, embora incapazes de formar colônias — sugerindo que o poder letal da melittina vem de um dano severo, possivelmente transitório, à membrana do qual as células não conseguem se recuperar totalmente, mesmo que sua maquinaria interna funcione por um breve período.
Um peptídeo humano mais versátil e resistente
O LL-37 comportou-se de forma diferente. Ele neutralizou a carga de superfície e danificou ambas as membranas em células do tipo selvagem e do mutante em extensão quase igual, indicando que sua ação foi em grande parte independente da mistura precisa de lipídios aniônicos. Em concentrações em que as membranas interna e externa já estavam fortemente comprometidas, muitas células ainda exibiam atividade metabólica mensurável, e os níveis de ATP nem sempre caíam a zero. Essa lacuna de tempo implica que o golpe final do LL-37 provavelmente envolve alvos além da própria membrana — como interromper a geração de energia, desencadear estresse oxidativo ou enrijecer o citoplasma ao se ligar ao DNA e ribossomos — uma vez que ele tenha acessado o interior celular.
O que isso significa para futuros antimicrobianos
No geral, o estudo mostra que a remodelação da membrana — mesmo mudanças drásticas afastando-se dos lipídios aniônicos usuais em direção ao ácido fosfatídico — não salva as bactérias da melittina ou do LL-37. Ambos os peptídeos se adaptam ao novo panorama lipídico, ainda se ligando, inserindo-se e, em última instância, matando. Os perfis detalhados dos ensaios revelam que a morte bacteriana não é um interruptor simples ligado/desligado no momento em que a membrana é perfurada, mas uma teia de eventos sobrepostos que podem deixar as células danificadas e incapazes de crescer muito antes de todos os sinais metabólicos desaparecerem. Ao vincular marcadores específicos de membrana e viabilidade à morte real, este trabalho fornece um roteiro sobre como avaliar e comparar novos peptídeos antimicrobianos, e sugere que a simples mudança na composição lipídica da membrana provavelmente não é uma rota de fuga fácil para bactérias frente a essas moléculas potentes e multifacetadas.
Citação: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Palavras-chave: peptídeos antimicrobianos, membranas bacterianas, remodelação lipídica, resistência a antibióticos, LL-37 e melittina