Clear Sky Science · he
גורל התא החיידקי תחת לחץ: עיצוב מחדש של שומנים והתקפת פפטידים אנטימיקרוביאליים
מדוע זה חשוב במאבק בזיהומים
ככל שיותר חיידקים מפתחים עמידות לאנטיביוטיקה הטובה ביותר שלנו, מדענים פונים למולקולות הגנה טבעיות הנקראות פפטידים אנטימיקרוביאליים, הנמצאות ביצורים מדבורים ועד בני אדם. אך החיידקים אינם מטרות פסיביות: הם יכולים לעצב מחדש את הממברנה השומנית שמקיפה את תאייהם, וכך להימנע אולי מתרופות חדשות אלו. המחקר הזה שואל שאלה מעשית עם השלכות רחבות: כאשר חיידקים משנים את הליפידים בממברנה תחת לחץ, האם שני פפטידים אנטימיקרוביאליים מוכרים — מליטין מהרעל של דבורת הדבש ו-LL-37 האנושי — יכולים עדיין להרוג אותם, ובאיזו דרך בדיוק הם עושים זאת?
חיידקים תחת לחץ
חיידקים ניצבים כל הזמן בתנאים קשים: שינויים בטמפרטורה או במליחות, התקפות חיסוניות וחשיפה לאנטיביוטיקה. כדי להתמודד, הם משנים את המולקולות השומניות, או הליפידים, שמרכיבות את הגבול החיצוני שלהם, ומכווננים תכונות כמו עובי, נזילות וטעינת פני השטח. אבני בניין ליפידיות חשובות, פוספטידית חומצה, שנמצאת בדרך כלל בכמויות זעירות, עלולה להצטבר כאשר ליפידים מטעים שליליים אחרים נדמים. הליפידים המטעים הללו הם בדרך כלל אתרי עגינה עיקריים לפפטידים אנטימיקרוביאליים בעלי מטען חיובי. המחברים השתמשו בחיידק המודל Escherichia coli ובשבט מוטנטי שחסר במידה רבה שני ליפידים אניוניים עיקריים, שהוחלפו בפוספטידית חומצה, כדי לחקות את סוג העיצוב מחדש של הממברנה שעשוי להתרחש תחת לחץ תרופתי.
שני פפטידים, שני סגנונות התקפה
הצוות התמקד במליטין ו-LL-37, פפטידים קלאסיים הפועלים על הממברנה שמשתפים צורת סליל אך נבדלים בסידור האזורים הידרופיליים וההידרופוביים שלהם. באמצעות כלים לחיזוי מבנה וממברנות מודל, הם הראו ששני הפפטידים יכולים להיקשר לא רק לליפידים האניוניים הרגילים אלא גם לפוספטידית חומצה, להחדיר את עצמם לממברנות שמשונו ולשבש את ארגונן. המליטין התגלה ככוחי במיוחד ביצירת דליפה בממברנות מודל של E. coli, בעוד של-LL-37 נצפתה דליפה ישירה חלשה יותר בתנאים זהים, מה שמרמז כי הוא עשוי להסתמך על מערך פעולות רחב יותר מאשר רק חור בממברנה.
צפייה במות התאים בזמן אמת
כדי לקשר נזק לממברנה למות חיידקי בפועל, החוקרים ערכו שישה בדיקות משלימות במקביל. אלה עקבו אחר כמה היטב הפפטידים נקשרים לפני שטח התא, האם הממברנה החיצונית והפנימית הפכו חדירות, האם הפוטנציאל החשמלי על פני הממברנה הפנימית קרס, וכיצד השתנו האנרגיה של התאים (ATP) ופעילות אנזימטית מטבולית. באופן קריטי הם מדדו אפקטים אלה גם ב-E. coli רגילה וגם במוטנט עם הממברנה שעוצבה מחדש, תוך ספירה כמה תאים עדיין יכולים ליצור מושבות. זה הניב "פרופילים" מפורטים שהראו אילו אירועים עלו והגיעו לרוויה באילו ריכוזים וזמנים של הפפטיד, ובכך מיפו בפועל את הדרך מהמגע הראשון ועד מות התא.
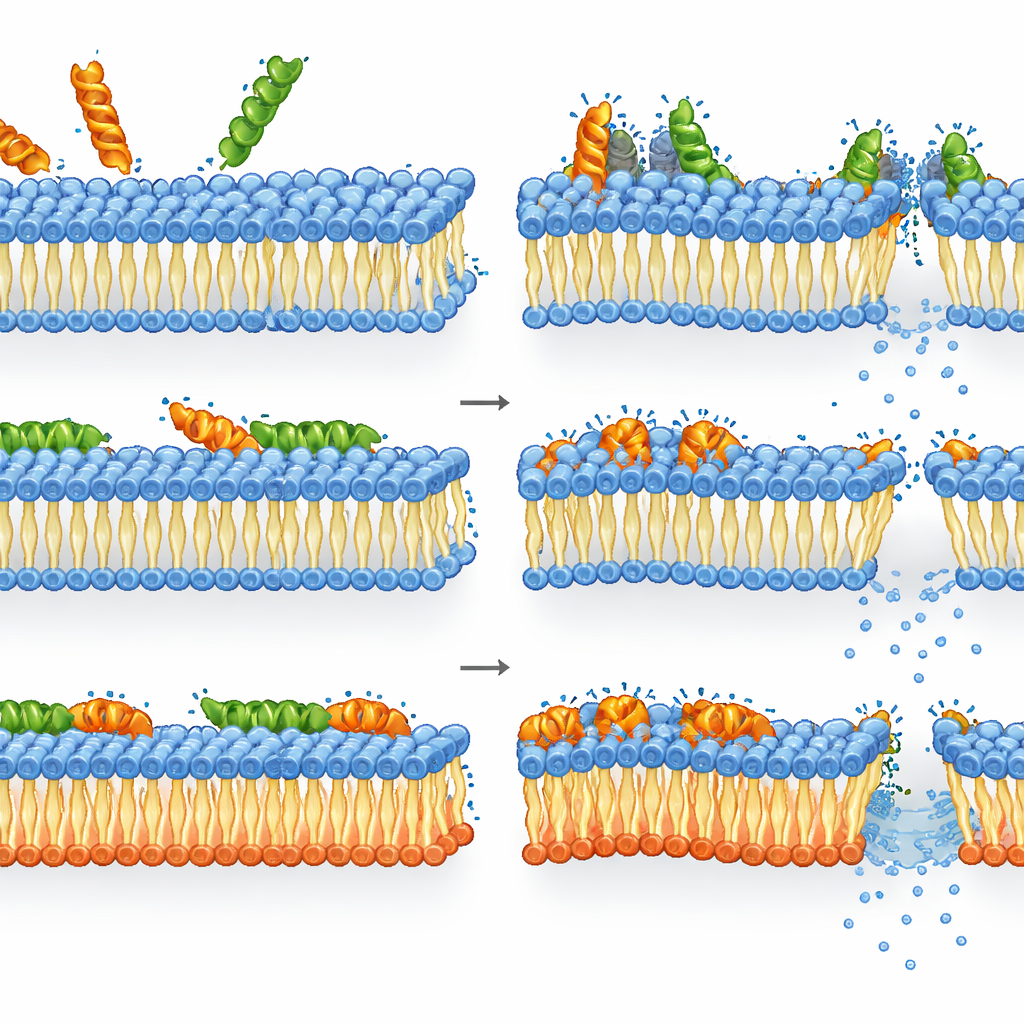
כיצד מליטין ו-LL-37 מתמודדים עם ממברנות שעוצבו מחדש
התברר כי מליטין היה אפילו קטלני יותר נגד חיידקים שחסרו את הליפידים האניוניים הרגילים מאשר נגד הבר-ברירה. במוטנט, אובדן שלמות הממברנה, ירידה ברמות האנרגיה ואובדן החיוניות היו קשורים באופן הדוק: ברגע שמליטין שיבש את הממברנה שעוצבה מחדש, התאים מתו במהירות. בבר-ברירה, לעומת זאת, התמונה הייתה מורכבת יותר. החדירות והדה-פולריזציה של הממברנה כבר היו ברוויה בריכוזים שבהם רמות ה-ATP ופעילות האנזימים נשארו יחסית גבוהות. במילים אחרות, תאים רבים היו בעלי ממברנות שנפגעו קשות אך עדיין פעילים מטבולית ולא יכלו ליצור מושבות — דבר המצביע על כך שההרג של מליטין נובע מנזק חמור, ואולי חולף, לממברנה שהתאים אינם יכולים לשקם לחלוטין, גם אם מכניזם פנימי מסוים ממשיך לפעול לזמן קצר.
פפטיד אנושי קשוח וגמיש יותר
LL-37 התנהג אחרת. הוא נטרל מטען פני השטח ופגע בשתי הממברנות בתאים הבר-ברירה ובמוטנט במידה כמעט זהה, דבר שמעיד על כך שהפעולה שלו הייתה ברובה בלתי תלויה בתמהיל המדויק של הליפידים האניוניים. בריכוזים שבהם הממברנה הפנימית והחיצונית היו כבר פגועות קשות, רבים מהתאים עדיין הظهرו פעילות מטבולית מדידה, ורמות ה-ATP לא תמיד צנחו לאפס. הפער התזמוני הזה מרמז כי המכה ההורגת הסופית של LL-37 סביר שתכלול מטרות שמעבר לממברנה עצמה — כגון שיבוש ייצור האנרגיה, גרימת לחץ חמצוני, או הקשחת הציטופלזמה על ידי קשירה ל-DNA וריבוזומים — ברגע שהוא נכנס לחלל התא הפנימי.
מה משמעות הדבר עבור אנטימיקרוביאלים עתידיים
בסך הכול המחקר מראה שעיצוב מחדש של הממברנה — אפילו שינוי קיצוני מהליפידים האניוניים הרגילים לכיוון פוספטידית חומצה — אינו מציל את החיידקים ממליטין או LL-37. שני הפפטידים מסתגלים לנוף הליפידי החדש, עדיין נקשרים, חודרים ולבסוף הורגים. פרופילי הבדיקות המפורטים מראים שמות החיידקים אינם מתנהלים כמתג פשוט של דליקה/כיבוי ברגע שהממברנה ננקבת, אלא כרשת אירועים חופפים שיכולה להשאיר תאים פגועים ובלתי גדלים זמן רב לפני שכל האותות המטבוליים נעלמים. על ידי קישור סמנים ספציפיים של הממברנה וחיוניות להרג אמיתי, עבודה זו מספקת מתווה לאיך להעריך ולהשוות פפטידים אנטימיקרוביאליים חדשים, ומרמזת ששינוי פשוט בהרכב הליפידים של הממברנה אינו צפוי להיות דרך בריחה קלה לחיידקים מול מולקולות רב-פרונטליות ועזות כאלו.
ציטוט: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
מילות מפתח: פפטידים אנטימיקרוביאליים, ממברנות חיידקים, עיצוב מחדש של ליפידים, עמידות לאנטיביוטיקה, LL-37 ומליטין