Clear Sky Science · sv
Bakteriers öde under stress: lipidombyggnad och angrepp av antimikrobiella peptider
Varför detta spelar roll i kampen mot infektioner
Allteftersom fler bakterier blir resistenta mot våra bästa antibiotika vänder sig forskare till naturliga försvarsmolekyler kallade antimikrobiella peptider, som finns hos allt från bin till människor. Men bakterier är inte passiva måltavlor: de kan ombygga det oljiga membran som omsluter deras celler och därigenom potentiellt undfly dessa nya läkemedel. Denna studie ställer en praktisk fråga med stora konsekvenser: när bakterier ändrar sina membranlipider under stress, kan två välkända antimikrobiella peptider—melittin från honungsbiet och människans LL-37—fortfarande döda dem, och hur går det då till?
Bakterier under tryck
Bakterier utsätts ständigt för hårda förhållanden: temperatur- eller saltförändringar, angrepp från immunförsvaret och exponering för antibiotika. För att hantera detta omkonfigurerar de de fettlika molekylerna, eller lipiderna, som utgör deras yttre gräns och finjusterar egenskaper som tjocklek, fluiditet och ytladdning. En viktig lipidbyggsten, fosfatidsyra, som normalt finns bara i små mängder, kan hopas när andra negativt laddade lipider minskar. Dessa laddade lipider är vanligtvis gynnsamma fästöar för positivt laddade antimikrobiella peptider. Författarna använde modellbakterien Escherichia coli och en mutantstam som i stor utsträckning saknar två stora anjoniska (negativt laddade) lipider och istället har mer fosfatidsyra, för att efterlikna den typ av membranombyggnad som kan uppstå under läkemedelspress.
Två peptider, två angreppssätt
Teamet fokuserade på melittin och LL-37, klassiska membranaktiva peptider som delar en helixform men skiljer sig i hur deras vattenälskande och fettälskande regioner är organiserade. Med hjälp av strukturprediktion och modellmembran visade de att båda peptiderna kan binda inte bara till de vanliga anjoniska lipiderna utan också till fosfatidsyra, att de går in i dessa förändrade membran och stör deras organisation. Melittin visade sig särskilt kraftfullt för att göra modell‑E. coli‑membran läckande, medan LL-37 uppvisade svagare direkt läckage under samma villkor, vilket antyder att dess verkan kan förlita sig på en bredare uppsättning mekanismer än bara att göra hål i membranet.
Att se celler dö i realtid
För att koppla membranskada till faktisk bakteriedöd körde forskarna sex kompletterande assayparalleller sida vid sida. Dessa följde hur väl peptiderna band till cellens yta, om det yttre och inre membranet blev permeabla, om den elektriska potentialen över innermembranet kollapsade och hur cellernas energi (ATP) och metabola enzymaktivitet förändrades. Avgörande var att de mätte dessa effekter både i normal E. coli och i den lipidombyggda mutanten samtidigt som de räknade hur många celler som fortfarande kunde bilda kolonier. Det här gav detaljerade ”profiler” som visar vilka händelser som steg och mättades vid vilka peptidkoncentrationer och tidpunkter, och som i praktiken kartlade vägen från första kontakt till celldöd.
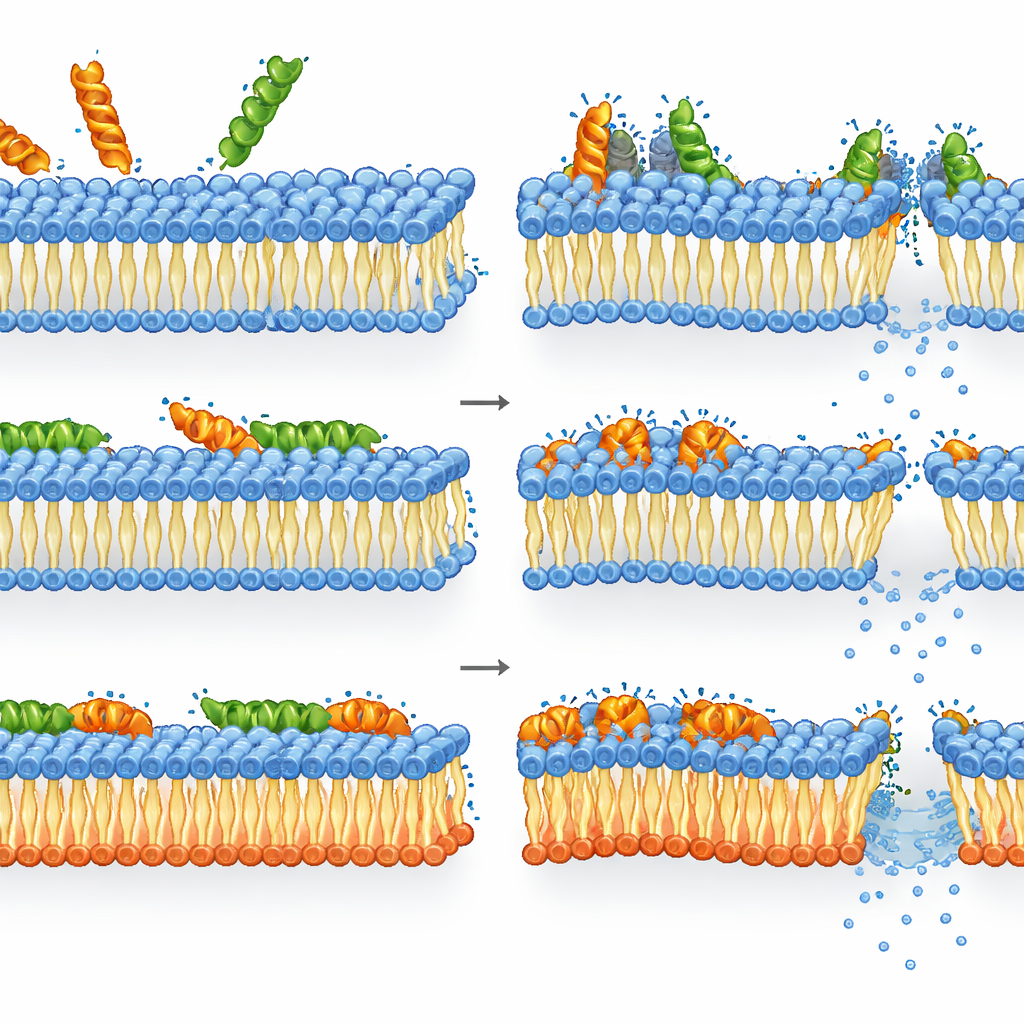
Hur melittin och LL-37 hanterar ombyggda membran
Melittin visade sig vara ännu mer dödligt mot bakterier som saknade de vanliga anjoniska lipiderna än mot vildtypen. I mutanten var förlusten av membranintegritet, sjunkande energinivåer och förlust av livskraft tätt sammankopplade: när melittin störde det ombyggda membranet dog cellerna snabbt. I vildtypen var bilden däremot mer nyanserad. Membranpermeabilisering och depolarisering var redan mättade vid koncentrationer där ATP och enzymaktivitet förblev relativt höga. Med andra ord hade många celler svårt skadade membran men var fortfarande metaboliskt aktiva samtidigt som de inte kunde bilda kolonier — vilket tyder på att melittins dödlighet kommer från allvarlig, möjligen övergående, membranskada som cellerna inte kan återhämta sig fullt från, även om deras inre maskineri kortvarigt fortsätter att fungera.
En tuffare, mer mångsidig human peptid
LL-37 uppträdde annorlunda. Den neutraliserade ytladdningen och skadade båda membranen i både vildtyp och mutanter i nästan samma utsträckning, vilket indikerar att dess verkan till stora delar var oberoende av den exakta blandningen av anjoniska lipider. Vid koncentrationer där inre och yttre membran redan var kraftigt komprometterade visade många celler fortfarande mätbar metabol aktivitet, och ATP-nivåerna föll inte alltid till noll. Detta tidsglapp antyder att LL-37:s slutgiltiga dödande sannolikt involverar mål bortom själva membranet — såsom att störa energiproduktionen, utlösa oxidativ stress eller stelna cytoplasman genom bindning till DNA och ribosomer — när den väl fått tillgång till cellens inre.
Vad detta innebär för framtida antimikrobiella medel
Sammantaget visar studien att membranombyggnad — även drastiska skiften bort från de vanliga anjoniska lipiderna mot fosfatidsyra — inte räddar bakterier från melittin eller LL-37. Båda peptiderna anpassar sig till det nya lipidlandskapet, binder fortfarande, går in och dödar i slutändan. De detaljerade assayprofilerna visar att bakteriedöd inte är en enkel på‑eller‑av‑brytare i ögonblicket då membranet punkteras, utan ett nätverk av överlappande händelser som kan lämna celler skadade och icke‑växande långt innan alla metabola signaler har försvunnit. Genom att koppla specifika membranfynd och livskraftmarkörer till verklig död ger detta arbete en mall för hur nya antimikrobiella peptider kan utvärderas och jämföras, och det antyder att enbart ändrad membranlipidsammansättning sannolikt inte blir en lätt flyktväg för bakterier som ställs inför dessa potenta, flerfacetterade molekyler.
Citering: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Nyckelord: antimikrobiella peptider, bakteriemembran, lipidombyggnad, antibiotikaresistens, LL-37 och melittin