Clear Sky Science · ar
مصير الخلية البكتيرية تحت الضغط: إعادة تشكيل الدهون وهجوم الببتيدات المضادة للميكروبات
لماذا هذا مهم في مكافحة العدوى
مع تزايد مقاومة البكتيريا لأفضل مضاداتنا الحيوية، يتجه العلماء إلى جزيئات دفاعية طبيعية تُسمى الببتيدات المضادة للميكروبات، الموجودة في كائنات من النحل إلى البشر. لكن البكتيريا ليست أهدافًا سلبية: يمكنها إعادة تشكيل الغشاء الزيتي المحيط بخلاياها، مما قد يمكنها من تجنّب هذه الأدوية الجديدة. تطرح هذه الدراسة سؤالًا عمليًا لتبعات كبيرة: عندما تغير البكتيريا دهون غشائها تحت الضغط، هل لا تزال اثنتان من الببتيدات المضادة للميكروبات المعروفة — ميليتين من سم نحل العسل وLL-37 البشري — قادرتين على قتلها، وبأي طريقة بالضبط؟
بكتيريا تحت الضغط
تواجه البكتيريا باستمرار ظروفًا قاسية: تقلبات في الحرارة أو الملح، هجمات جهاز المناعة، والتعرض للمضادات الحيوية. للتعامل مع ذلك، تعيد تكوين الجزيئات الدهنية التي تشكل حدودها الخارجية، مضبوطةً خصائص مثل السمك والسيولة والشحنة السطحية. يمكن لمكوّن دهني رئيسي، الفسفاتيديك أسيد، والذي يوجد عادةً بكميات ضئيلة، أن يتراكم عندما تُنقص الدهون السالبة الأخرى. تلك الدهون المشحونة تكون عادةً مواقع ارتباط رئيسية للببتيدات الإيجابية الشحنة. استخدم المؤلفون بكتيريا نموذجية هي الإشريكية القولونية وسلالة طفيلية تفتقر إلى نظامي دهن سالبة شحنة كبيرين، مستبدلين إياهما بمزيد من الفسفاتيديك أسيد، لمحاكاة نوع إعادة تشكيل الغشاء الذي قد يحدث تحت ضغط الدواء.
ببتيدان، أسلوبان للهجوم
ركز الفريق على الميليتين وLL-37، ببتيدات كلاسيكية النشطة ضد الغشاء تشترك في شكل حلزوني لكنها تختلف في ترتيب مناطقها المحبة للماء والدهون. باستخدام أدوات توقع البنية وغشاء نموذجية، أظهروا أن كلا الببتيدين يمكنهما الارتباط ليس فقط بالدهون السالبة النموذجية بل أيضًا بالفسفاتيديك أسيد، والاندخال في هذه الأغشية المعدلة واضطراب تنظيمها. أثبتت الميليتين أنها فعالة بشكل خاص في جعل أغشية نموذجية للإشريكية القولونية مسربة، بينما أظهر LL-37 تسريبًا مباشرًا أضعف تحت الظروف نفسها، مما يشير إلى أنه قد يعتمد على مجموعة أوسع من الإجراءات بدلًا من مجرد صنع ثقوب في الغشاء.
مراقبة موت الخلايا في الوقت الحقيقي
لربط تلف الغشاء بالموت البكتيري الفعلي، أجرى الباحثون ست تجارب متممة جنبًا إلى جنب. تابعت هذه كيف يرتبط الببتيد بسطح الخلية، وما إذا أصبح غشائي الخلية الخارجي والداخلي منفذين، وما إذا انهار فرق الجهد عبر الغشاء الداخلي، وكيف تغيرت طاقة الخلايا (ATP) ونشاط إنزيماتها الأيضية. والأهم من ذلك، قاموا بقياس هذه التأثيرات في كل من الإشريكية القولونية الطبيعية والسلالة المعاد تشكيل غشائها، مع عدّ عدد الخلايا القادرة على تكوين مستعمرات. أنتج هذا "ملفات تعريف" مفصلة تُظهر أي الأحداث ترتفع وتصل إلى التشبع عند أي تراكيز الببتيد والأزمنة، مجسدةً الطريق من الاتصال الأول إلى الموت الخلوي.
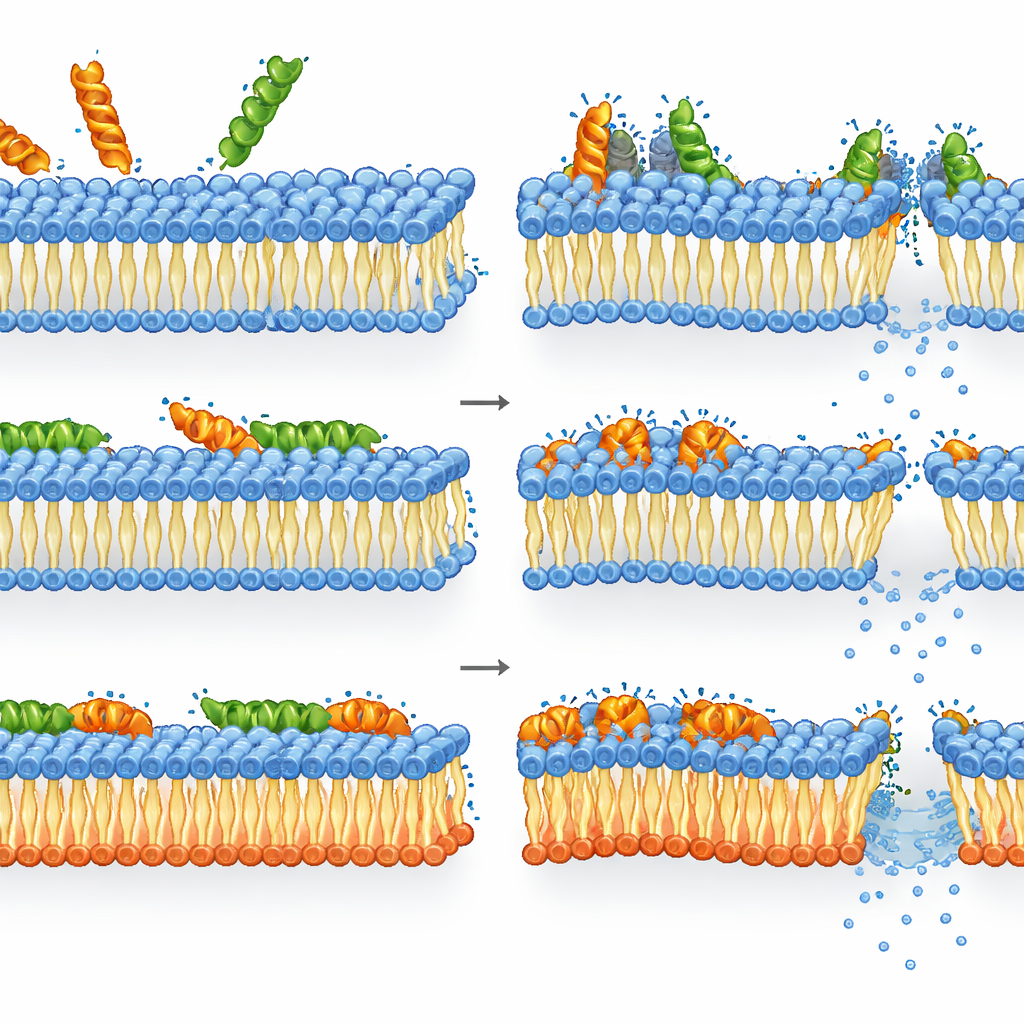
كيف يتعامل الميليتين وLL-37 مع الأغشية المعاد تشكيلها
اتضح أن الميليتين كان أكثر فتكًا ضد البكتيريا التي تفتقر إلى الدهون السالبة المعتادة مقارنةً بالنمط البري. في السلالة الطافرة، ارتبط فقدان سلامة الغشاء، وتراجع مستويات الطاقة، وفقدان القدرة على البقاء ارتباطًا وثيقًا: بمجرد أن أزعج الميليتين الغشاء المعاد تشكيله، ماتت الخلايا بسرعة. في النمط البري، كانت الصورة أكثر تعقيدًا. فقد كانت نفاذية الغشاء وازديالاستقطاب مشبعة بالفعل عند تراكيز لم تنخفض عندها مستويات ATP ونشاط الإنزيمات كثيرًا. بعبارة أخرى، كان لدى العديد من الخلايا أغشية متضررة بشدة لكنها لا تزال نشطة أيضيًا ولكن غير قادرة على تكوين مستعمرات — مما يوحي أن قوة قتل الميليتين تأتي من ضرر غشائي شديد، قد يكون مؤقتًا، لا تستطيع الخلايا التعافي منه بالكامل، حتى لو استمر جهازها الداخلي بالعمل لفترة قصيرة.
ببتيد بشري أكثر صلابة وتعددية
تصرف LL-37 بشكل مختلف. قام بتعادل الشحنة السطحية وتضرر كلا الغشائين في الخلايا النمطية والطافرة إلى حدٍّ متقارب، مما يشير إلى أن تأثيره كان مستقلاً إلى حد كبير عن التركيب الدقيق للدهون السالبة. عند تراكيز كانت فيها الأغشية الداخلية والخارجية متضررة بشدة بالفعل، أظهرت العديد من الخلايا نشاطًا أيضيًا قابلًا للقياس، ولم تنخفض مستويات ATP دائمًا إلى الصفر. يشير هذا الفارق الزمني إلى أن الضربة القاتلة النهائية لـ LL-37 ربما تشمل أهدافًا تتجاوز الغشاء نفسه — مثل تعطيل توليد الطاقة، إثارة الإجهاد التأكسدي، أو تَقَسُّط السيتوبلازم عن طريق الارتباط بالحمض النووي والريبوسومات — بمجرد أن يصل إلى داخل الخلية.
ماذا يعني هذا لمضادات الميكروبات المستقبلية
بشكل عام، تُظهر الدراسة أن إعادة تشكيل الغشاء — حتى تغييرات جذرية بعيدًا عن الدهون السالبة المعتادة نحو الفسفاتيديك أسيد — لا تنقذ البكتيريا من الميليتين أو LL-37. كلا الببتيدين يتكيفان مع المشهد الدهني الجديد، لا يزالان يرتبطان ويقحمان ويقضيان في النهاية. تكشف ملفات الاختبار المفصلة أن موت البكتيريا ليس مفتاح تشغيل/إيقاف بسيطًا عند لحظة اختراق الغشاء، بل هو شبكة من أحداث متداخلة يمكن أن تترك الخلايا متضررة وغير نامية قبل اختفاء جميع إشارات الأيض. من خلال ربط علامات الغشاء والقدرة على البقاء القابلة للقياس بالقتل الفعلي، توفر هذه الدراسة مخططًا لتقييم ومقارنة الببتيدات المضادة للميكروبات الجديدة، وتشير إلى أن تغيير تركيب دهون الغشاء وحده ليس طريقًا سهلاً للهروب أمام البكتيريا في مواجهة هذه الجزيئات القوية متعددة الزوايا.
الاستشهاد: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
الكلمات المفتاحية: الببتيدات المضادة للميكروبات, أغشية البكتيريا, إعادة تشكيل الدهون, مقاومة المضادات الحيوية, LL-37 ومليتين