Clear Sky Science · pl
Losy komórkowe bakterii pod stresem: przebudowa lipidów i atak peptydów przeciwbakteryjnych
Dlaczego ma to znaczenie w walce z infekcjami
W miarę jak coraz więcej bakterii staje się opornych na nasze najlepsze antybiotyki, naukowcy zwracają się ku naturalnym cząsteczkom obronnym zwanym peptydami przeciwbakteryjnymi, występującym u organizmów od pszczół po ludzi. Bakterie jednak nie są biernymi celami: potrafią przebudowywać oleistą błonę otaczającą ich komórki, co może pozwolić im unikać tych nowych leków. W badaniu postawiono praktyczne pytanie o dalekosiężnych konsekwencjach: gdy bakterie zmieniają lipidy błonowe pod wpływem stresu, czy dwa dobrze znane peptydy — melityna z jadu pszczoły miodnej i ludzki LL-37 — nadal potrafią je zabić i w jaki sposób to robią?
Bakterie pod presją
Bakterie nieustannie stykają się z trudnymi warunkami: zmianami temperatury lub zasolenia, atakami układu odpornościowego i ekspozycją na antybiotyki. Aby sobie radzić, rekonfigurują cząsteczki tłuszczowe, czyli lipidy, które tworzą ich zewnętrzną granicę, regulując właściwości takie jak grubość, płynność i ładunek powierzchniowy. Kluczowy element budulcowy lipidów, fosfatydowy kwas (fosfatydowa), zwykle obecny w niewielkich ilościach, może się kumulować, gdy inne ujemnie naładowane lipidy zostaną wyczerpane. Te naładowane lipidy są zwykle głównymi miejscami przyczepu dla dodatnio naładowanych peptydów przeciwbakteryjnych. Autorzy wykorzystali modelową bakterię Escherichia coli oraz mutant pozbawiony w dużej mierze dwóch głównych lipidów anionowych, zastąpionych w większym stopniu fosfatydowym kwasem, aby naśladować przebudowę błony, jaka może zachodzić pod presją leków.
Dwa peptydy, dwa sposoby ataku
Zespół skupił się na melitynie i LL-37, klasycznych peptydach działających na błony, które mają helikalny kształt, ale różnią się układem części hydrofilowych i hydrofobowych. Korzystając z narzędzi do przewidywania struktur i modeli błon, wykazali, że oba peptydy mogą wiązać się nie tylko z typowymi lipidami anionowymi, lecz także z fosfatydowym kwasem, wnikając w te zmienione błony i zaburzając ich organizację. Melityna okazała się szczególnie skuteczna w powodowaniu przecieków w modelowych błonach E. coli, podczas gdy LL-37 wykazywał słabsze bezpośrednie wycieki w tych samych warunkach, co sugeruje, że może polegać na szerszym zestawie działań niż jedynie przebijanie otworów w błonie.
Obserwowanie śmierci komórek w czasie rzeczywistym
Aby powiązać uszkodzenie błony z rzeczywistą śmiercią bakterii, badacze przeprowadzili sześć uzupełniających się testów równolegle. Śledziły one, jak dobrze peptydy wiążą się z powierzchnią komórki, czy błona zewnętrzna i wewnętrzna stają się przepuszczalne, czy potencjał elektryczny przez błonę wewnętrzną się załamuje oraz jak zmienia się energia komórek (ATP) i aktywność enzymów metabolicznych. Co ważne, mierzyli te efekty zarówno w typowej E. coli, jak i w mutantach z przebudowaną lipidom, równocześnie licząc, ile komórek nadal potrafi tworzyć kolonie. To dało szczegółowe „profile” pokazujące, które zdarzenia pojawiają się i osiągają maksimum przy jakich stężeniach peptydów i w jakim czasie, skutecznie mapując drogę od pierwszego kontaktu do śmierci komórki.
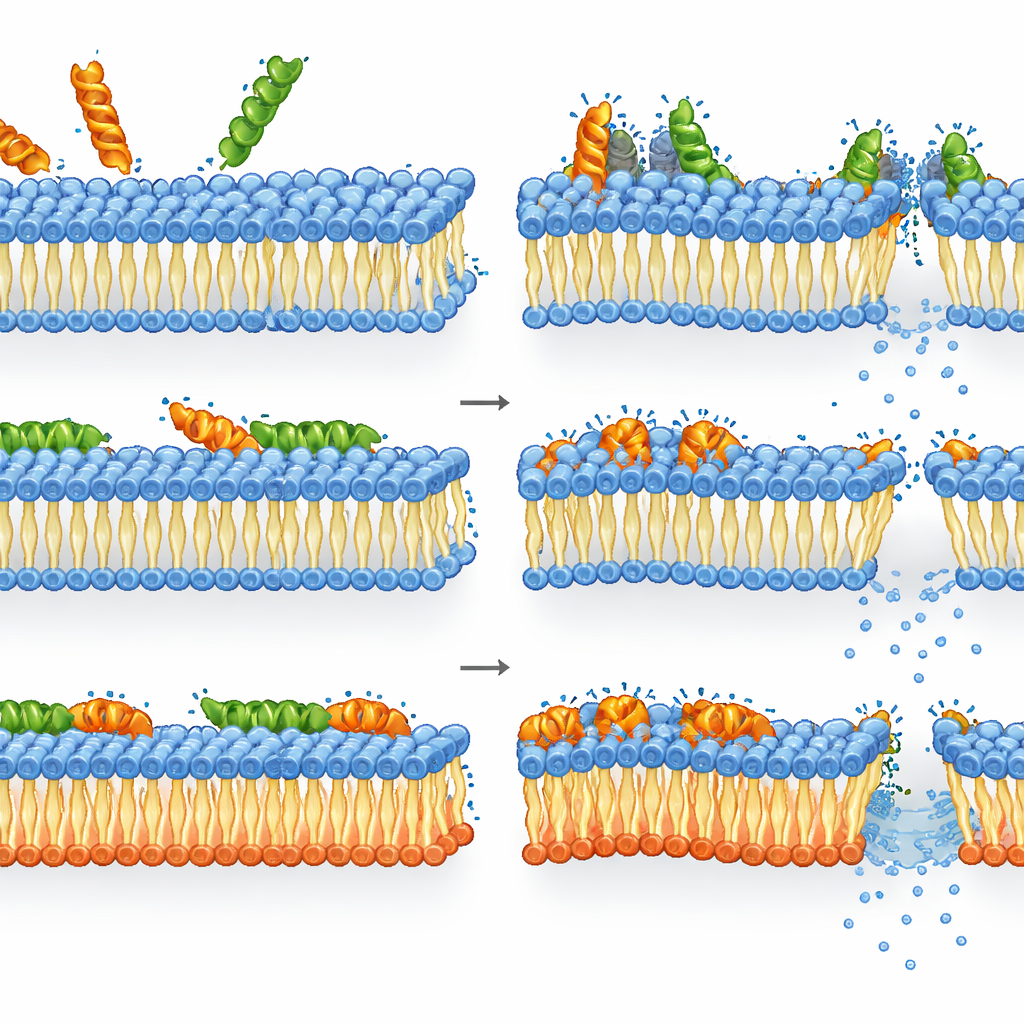
Jak melityna i LL-37 radzą sobie z przebudowanymi błonami
Okazało się, że melityna jest jeszcze bardziej zabójcza wobec bakterii pozbawionych typowych lipidów anionowych niż wobec szczepu dzikiego. W mutancie utrata integralności błony, spadek poziomu energii i utrata żywotności były ściśle powiązane: gdy melityna uszkadzała przebudowaną błonę, komórki szybko ginęły. W szczepie dzikim obraz był jednak bardziej zniuansowany. Przepuszczalność i depolaryzacja błony były już nasycone przy stężeniach, przy których ATP i aktywność enzymów pozostawały stosunkowo wysokie. Innymi słowy, wiele komórek miało poważnie uszkodzone błony, a mimo to było nadal metabolicznie aktywnych, lecz niezdolnych do tworzenia kolonii — co sugeruje, że zabójcza siła melityny wynika z poważnych, być może przejściowych uszkodzeń błony, z których komórki nie potrafią w pełni się odzyskać, nawet jeśli ich wewnętrzne mechanizmy krótko jeszcze działają.
Trudniejszy, bardziej wszechstronny peptyd ludzki
LL-37 zachowywał się inaczej. Neutralizował ładunek powierzchniowy i uszkadzał obie błony w komórkach typu dzikiego i mutantach w prawie takim samym stopniu, co wskazuje, że jego działanie było w dużej mierze niezależne od dokładnego składu lipidów anionowych. Przy stężeniach, przy których wewnętrzne i zewnętrzne błony były już mocno naruszone, wiele komórek nadal wykazywało mierzalną aktywność metaboliczną, a poziomy ATP nie zawsze spadały do zera. Ta rozbieżność czasowa sugeruje, że ostateczny cios zabójczy LL-37 prawdopodobnie obejmuje cele wykraczające poza samą błonę — takie jak zakłócenie wytwarzania energii, wywołanie stresu oksydacyjnego lub usztywnienie cytoplazmy przez wiązanie z DNA i rybosomami — gdy peptyd dostanie się do wnętrza komórki.
Co to oznacza dla przyszłych antybiotyków
Podsumowując, badanie pokazuje, że przebudowa błony — nawet radykalne przesunięcie z typowych lipidów anionowych w kierunku fosfatydowego kwasu — nie ratuje bakterii przed melityną ani LL-37. Oba peptydy dostosowują się do nowego krajobrazu lipidowego, nadal wiążąc się, wnikając i ostatecznie zabijając. Szczegółowe profile testów ujawniają, że śmierć bakterii nie jest prostym przełącznikiem w chwili przebicia błony, lecz siecią nakładających się zdarzeń, które mogą pozostawić komórki uszkodzone i niezdolne do wzrostu na długo zanim znikną wszystkie sygnały metaboliczne. Łącząc konkretne markery błonowe i żywotności z rzeczywistym zabijaniem, praca ta dostarcza planu oceny i porównywania nowych peptydów przeciwbakteryjnych i sugeruje, że samo zmienienie składu lipidów błonowych raczej nie będzie łatwą drogą ucieczki dla bakterii wobec tych silnych, wielotorowych cząsteczek.
Cytowanie: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Słowa kluczowe: peptydy przeciwbakteryjne, błony bakteryjne, przebudowa lipidów, oporność na antybiotyki, LL-37 i melityna