Clear Sky Science · fr
Destin des cellules bactériennes sous stress : remodelage lipidique et attaque par peptides antimicrobiens
Pourquoi cela compte pour lutter contre les infections
À mesure que de plus en plus de bactéries deviennent résistantes à nos meilleurs antibiotiques, les scientifiques se tournent vers des molécules de défense naturelles appelées peptides antimicrobiens, présentes chez des organismes allant des abeilles aux humains. Mais les bactéries ne sont pas des cibles passives : elles peuvent remodeler la couche huileuse qui entoure leurs cellules, échappant potentiellement à ces nouveaux agents. Cette étude pose une question pratique aux grandes implications : lorsque les bactéries modifient leurs lipides membranaires sous stress, deux peptides antimicrobiens bien connus — la mélittine du venin d’abeille et la LL-37 humaine — peuvent-ils encore les tuer, et comment précisément s’y prennent-ils ?
Bactéries sous pression
Les bactéries font constamment face à des conditions rudes : variations de température ou de sel, attaques du système immunitaire et exposition aux antibiotiques. Pour s’adapter, elles reconfigurent les molécules grasses, ou lipides, qui composent leur frontière externe, ajustant des propriétés comme l’épaisseur, la fluidité et la charge de surface. Un élément lipidique clé, l’acide phosphatidique, normalement présent seulement en très petites quantités, peut s’accumuler lorsque d’autres lipides chargés négativement sont épuisés. Ces lipides chargés servent habituellement de cibles privilégiées pour les peptides antimicrobiens chargés positivement. Les auteurs ont utilisé la bactérie modèle Escherichia coli et une souche mutante qui est en grande partie dépourvue de deux lipides anioniques majeurs, les remplaçant par davantage d’acide phosphatidique, pour imiter le type de remodelage membranaire qui pourrait se produire sous pression médicamenteuse.
Deux peptides, deux modes d’attaque
L’équipe s’est concentrée sur la mélittine et la LL-37, des peptides classiques actifs sur la membrane qui partagent une forme hélicoïdale mais diffèrent dans l’arrangement de leurs régions hydrophiles et lipophiles. En utilisant des outils de prédiction de structure et des membranes modèles, ils ont montré que les deux peptides peuvent se lier non seulement aux lipides anioniques habituels mais aussi à l’acide phosphatidique, s’insérant dans ces membranes altérées et perturbant leur organisation. La mélittine s’est révélée particulièrement efficace pour rendre les membranes modèles d’E. coli perméables, tandis que la LL-37 a montré une fuite directe plus faible dans les mêmes conditions, ce qui laisse entendre qu’elle peut s’appuyer sur un ensemble d’actions plus large que la simple perforation de la membrane.
Observer les cellules mourir en temps réel
Pour relier les dommages membraneires à la mort bactérienne réelle, les chercheurs ont exécuté six tests complémentaires côte à côte. Ceux-ci suivaient l’affinité des peptides pour la surface cellulaire, la perméabilité des membranes externe et interne, l’effondrement du potentiel électrique à travers la membrane interne, et l’évolution de l’énergie cellulaire (ATP) et de l’activité des enzymes métaboliques. De manière cruciale, ils ont mesuré ces effets à la fois chez E. coli normale et chez le mutant au remodelage lipidique tout en dénombrant combien de cellules pouvaient encore former des colonies. Cela a produit des « profils » détaillés montrant quels événements augmentent et se saturent à quelles concentrations et quels moments, cartographiant effectivement la route du premier contact à la mort cellulaire.
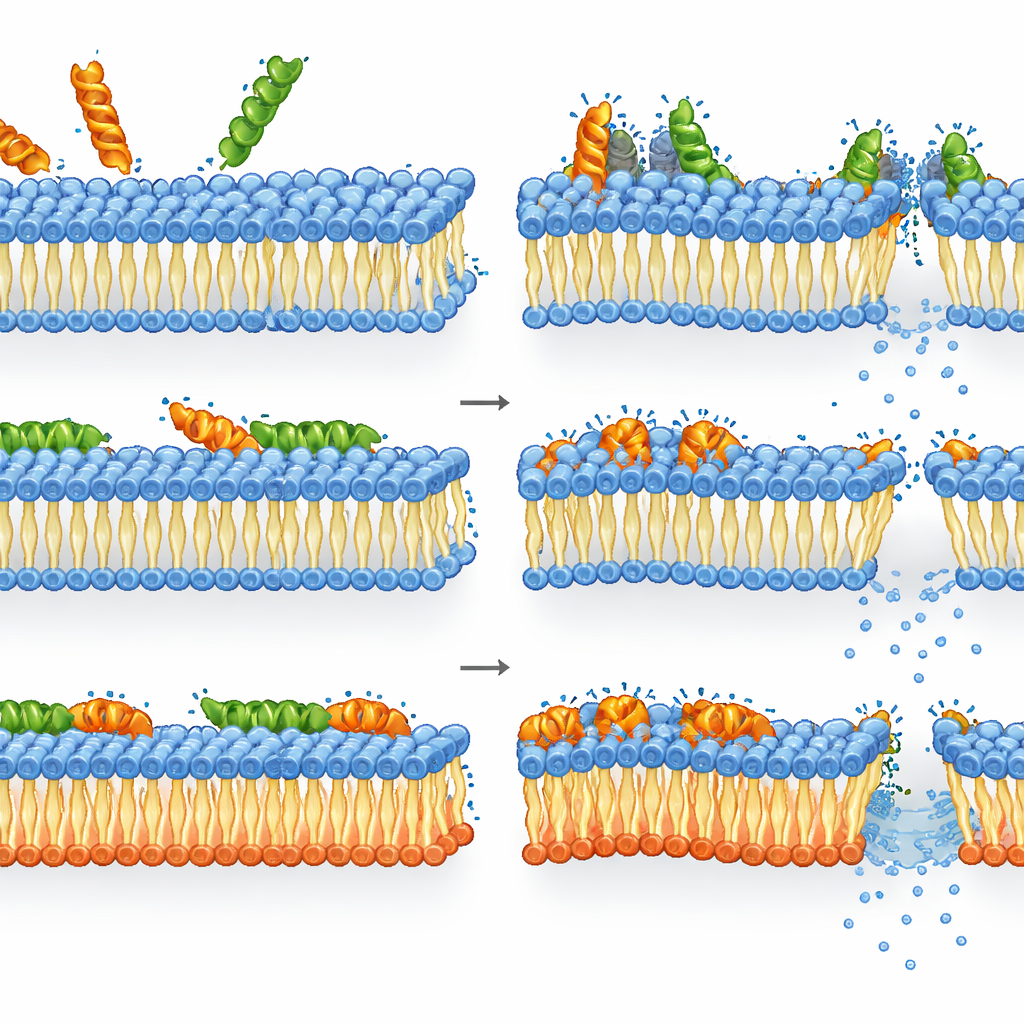
Comment la mélittine et la LL-37 gèrent les membranes remodelées
La mélittine s’est avérée encore plus létale contre les bactéries dépourvues des lipides anioniques habituels que contre le type sauvage. Chez le mutant, la perte d’intégrité membranaire, la chute des niveaux d’énergie et la perte de viabilité étaient étroitement liées : une fois que la mélittine perturbait la membrane remodelée, les cellules mouraient rapidement. Chez le type sauvage, en revanche, le tableau était plus nuancé. La perméabilisation et la dépolarisation membranaires étaient déjà saturées à des concentrations où l’ATP et l’activité enzymatique restaient relativement élevées. Autrement dit, de nombreuses cellules présentaient des membranes gravement endommagées mais restaient encore métaboliquement actives tout en étant incapables de former des colonies — ce qui suggère que le pouvoir létal de la mélittine provient d’un dommage membranaire sévère, possiblement transitoire, dont les cellules ne peuvent pas totalement se remettre, même si leur machinerie interne continue de fonctionner brièvement.
Un peptide humain plus résistant et polyvalent
La LL-37 s’est comportée différemment. Elle neutralisait la charge de surface et endommageait les deux membranes chez les cellules de type sauvage et les mutants de manière presque identique, indiquant que son action dépendait peu de la composition précise en lipides anioniques. À des concentrations où les membranes interne et externe étaient déjà fortement compromises, de nombreuses cellules montraient encore une activité métabolique mesurable, et les niveaux d’ATP ne chutait pas toujours à zéro. Cet écart temporel implique que le coup de grâce final de la LL-37 implique probablement des cibles au-delà de la membrane elle-même — comme la perturbation de la production d’énergie, le déclenchement d’un stress oxydatif, ou le rigidification du cytoplasme par liaison à l’ADN et aux ribosomes — une fois qu’elle a pénétré à l’intérieur de la cellule.
Ce que cela signifie pour les antimicrobiens futurs
Globalement, l’étude montre que le remodelage membranaire — même des basculements drastiques loin des lipides anioniques habituels vers l’acide phosphatidique — ne sauve pas les bactéries de la mélittine ou de la LL-37. Les deux peptides s’adaptent au nouveau paysage lipidique, se lient toujours, s’insèrent et finissent par tuer. Les profils d’essais détaillés révèlent que la mort bactérienne n’est pas un simple interrupteur marche/arrêt au moment où la membrane est perforée, mais un réseau d’événements qui se chevauchent et peuvent laisser les cellules endommagées et incapables de croître bien avant que tous les signaux métaboliques ne disparaissent. En reliant des marqueurs membranaires et de viabilité spécifiques à la mort effective, ce travail fournit une feuille de route pour évaluer et comparer de nouveaux peptides antimicrobiens, et suggère que modifier la composition lipidique de la membrane n’est probablement pas une voie d’évasion facile pour les bactéries face à ces molécules puissantes et multi‑voies.
Citation: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Mots-clés: peptides antimicrobiens, membranes bactériennes, remodelage lipidique, résistance aux antibiotiques, LL-37 et mélittine