Clear Sky Science · nl
Bacteriële celdood onder stress: lipideremodellering en aanval door antimicrobiële peptiden
Waarom dit belangrijk is voor de strijd tegen infecties
Naarmate meer bacteriën resistent worden tegen onze beste antibiotica, wenden wetenschappers zich tot natuurlijke verdedigingsmoleculen genaamd antimicrobiële peptiden, die voorkomen in organismen van bijen tot mensen. Maar bacteriën zijn geen passieve doelen: zij kunnen het vette membraan rond hun cellen herstructureren en zich zo mogelijk onttrekken aan deze nieuwe middelen. Deze studie stelt een praktische vraag met grote implicaties: wanneer bacteriën hun membranefosfolipiden onder stress veranderen, kunnen twee bekende antimicrobiële peptiden — melittine uit honingbijengif en het menselijke LL-37 — hen dan nog doden, en hoe doen ze dat precies?
Bacteriën onder druk
Bacteriën staan voortdurend onder zware omstandigheden: temperatuurschommelingen of zoutveranderingen, immuunaanvallen en blootstelling aan antibiotica. Om hiermee om te gaan herconfigureren ze de vetachtige moleculen, of lipiden, die hun buitengrens vormen, waarbij eigenschappen als dikte, vloeibaarheid en oppervlaktespanning worden bijgesteld. Een belangrijk lipidebouwblok, fosfatidische zuur (phosphatidic acid), dat normaal slechts in kleine hoeveelheden voorkomt, kan zich ophopen wanneer andere negatief geladen lipiden worden uitgeput. Die geladen lipiden zijn gewoonlijk gunstige aanhechtingsplaatsen voor positief geladen antimicrobiële peptiden. De auteurs gebruikten de modelbacterie Escherichia coli en een mutantstam die grotendeels twee belangrijke anionische (negatief geladen) lipiden mist en deze vervangt door meer fosfatidische zuur, om het soort membraneremodellering na te bootsen dat onder medicijndruk kan optreden.
Twee peptiden, twee aanvalsstijlen
Het team richtte zich op melittine en LL-37, klassieke membraan-actieve peptiden die een helixvorm delen maar verschillen in de ordening van hun hydrofiele en hydrofobe regio’s. Met behulp van structuurvoorspellende instrumenten en modelmembranen toonden zij aan dat beide peptiden niet alleen aan de gebruikelijke anionische lipiden kunnen binden, maar ook aan fosfatidische zuur, zich in deze gewijzigde membranen kunnen insereren en hun organisatie verstoren. Melittine bleek bijzonder krachtig in het lek maken van model-E. coli-membranen, terwijl LL-37 onder dezelfde omstandigheden zwakkere directe lekkage veroorzaakte, wat suggereert dat het op een breder spectrum van acties steunt dan louter porevorming in het membraan.
Cellen die in real time sterven bekijken
Om membraanschade te koppelen aan daadwerkelijke bacteriële dood voerden de onderzoekers zes complementaire assays gelijktijdig uit. Deze volgden hoe goed peptiden aan het celoppervlak binden, of het buiten- en binnenmembraan permeabel werden, of het elektrische potentiaal over het binnenmembraan instortte en hoe de energie (ATP) en de activiteit van metabole enzymen van de cellen veranderde. Cruciaal was dat ze deze effecten zowel in normale E. coli als in de lipide-geremodelleerde mutant maten, terwijl ze ook telden hoeveel cellen nog kolonies konden vormen. Dit leverde gedetailleerde ‘profielen’ op die tonen welke gebeurtenissen bij welke peptideconcentraties en tijden oplopen en verzadigen, en zo de weg van eerste contact naar celdood in kaart brengen.
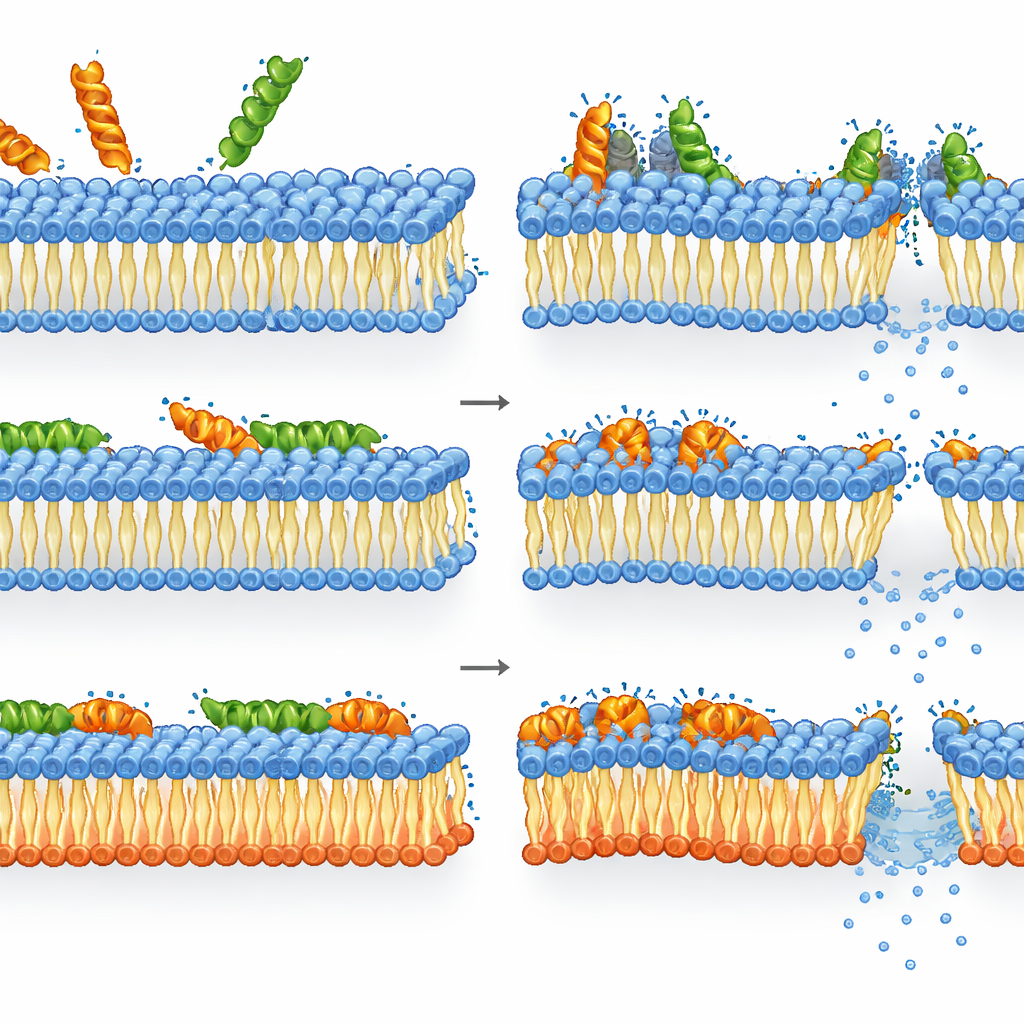
Hoe melittine en LL-37 omgaan met geremodelleerde membranen
Melittine bleek zelfs dodelijker tegen bacteriën die de gebruikelijke anionische lipiden misten dan tegen de wildtype-stam. In de mutant waren verlies van membraanintegriteit, dalende energieniveaus en verlies van levensvatbaarheid nauw met elkaar verbonden: zodra melittine het geremodelleerde membraan verstoorde, stierven de cellen snel. Bij de wildtype-stam was het plaatje echter genuanceerder. Membraanpermeabilisatie en depolarisatie waren al verzadigd bij concentraties waarbij ATP en enzymactiviteit relatief hoog bleven. Met andere woorden, veel cellen hadden sterk beschadigde membranen maar waren nog steeds metabool actief en konden toch geen kolonies vormen — wat suggereert dat melittine’s dodelijke kracht voortkomt uit ernstige, mogelijk tijdelijke, membraanschade waarvan de cellen zich niet volledig kunnen herstellen, zelfs als hun interne machines kort blijven draaien.
Een taaiere, veelzijdigere menselijke peptide
LL-37 gedroeg zich anders. Het neutraliseerde de oppervlakte-lading en beschadigde beide membranen in zowel wildtype- als mutantcellen bijna in gelijke mate, wat aangeeft dat de werking grotendeels onafhankelijk is van de precieze samenstelling van anionische lipiden. Bij concentraties waarbij binnen- en buitenmembraan al zwaar aangetast waren, vertoonden veel cellen nog steeds meetbare metabole activiteit en daalden ATP-niveaus niet altijd tot nul. Deze tijdsverschillen wijzen erop dat LL-37’s definitieve dodelijke effect waarschijnlijk ook doelen buiten het membraan omvat — zoals het verstoren van energieproductie, het opwekken van oxidatieve stress of het verstevigen van het cytoplasma door binden aan DNA en ribosomen — zodra het toegang heeft gekregen tot het celinterieur.
Wat dit betekent voor toekomstige antimicrobiële middelen
Al met al laat de studie zien dat membraneremodellering — zelfs drastische verschuivingen weg van de gebruikelijke anionische lipiden richting fosfatidische zuur — bacteriën niet redt van melittine of LL-37. Beide peptiden passen zich aan het nieuwe lipidenspectrum aan, binden nog steeds, dringen in en doden uiteindelijk. De gedetailleerde assayprofielen tonen aan dat bacteriële dood geen eenvoudige aan/uit-schakelaar is op het moment dat het membraan wordt doorboord, maar een web van overlappende gebeurtenissen die cellen beschadigd en niet-groeiend kunnen achterlaten lang voordat alle metabole signalen verdwenen zijn. Door specifieke membraan- en viabiliteitsmarkers te koppelen aan daadwerkelijke killing biedt dit werk een blauwdruk om nieuwe antimicrobiële peptiden te evalueren en te vergelijken, en het suggereert dat het simpelweg veranderen van membraanlipidesamenstelling geen gemakkelijke ontsnappingsroute zal zijn voor bacteriën die geconfronteerd worden met deze krachtige, veelnoopsmethode moleculen.
Bronvermelding: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Trefwoorden: antimicrobiële peptiden, bacteriële membranen, lipideremodellering, antibioticaresistentie, LL-37 en melittine