Clear Sky Science · es
Destino de las células bacterianas bajo estrés: remodelado lipídico y ataque de péptidos antimicrobianos
Por qué importa para combatir las infecciones
A medida que más bacterias se vuelven resistentes a nuestros mejores antibióticos, los científicos recurren a moléculas de defensa naturales llamadas péptidos antimicrobianos, presentes en organismos desde las abejas hasta los humanos. Pero las bacterias no son objetivos pasivos: pueden remodelar la capa oleosa que rodea sus células y así eludir potencialmente estos nuevos fármacos. Este estudio plantea una pregunta práctica con amplias implicaciones: cuando las bacterias cambian los lípidos de su membrana bajo estrés, ¿pueden dos péptidos antimicrobianos bien conocidos —la melitina del veneno de abeja y la LL-37 humana— seguir matándolas, y cómo lo hacen exactamente?
Bacterias bajo presión
Las bacterias se enfrentan constantemente a condiciones adversas: cambios de temperatura o salinidad, ataques del sistema inmune y exposición a antibióticos. Para sobrevivir, reconfiguran las moléculas grasas, o lípidos, que forman su límite exterior, ajustando propiedades como el espesor, la fluidez y la carga superficial. Un bloque lipídico clave, el ácido fosfatídico, normalmente presente solo en cantidades pequeñas, puede acumularse cuando otros lípidos cargados negativamente se agotan. Esos lípidos cargados suelen ser puntos de unión preferentes para los péptidos antimicrobianos cargados positivamente. Los autores usaron la bacteria modelo Escherichia coli y una cepa mutante que carece en gran medida de dos lípidos aniónicos principales, reemplazándolos por más ácido fosfatídico, para imitar el tipo de remodelado de membrana que podría ocurrir bajo presión por fármacos.
Dos péptidos, dos estilos de ataque
El equipo se centró en la melitina y la LL-37, péptidos clásicos activos sobre membranas que comparten una forma helicoidal pero difieren en la disposición de sus regiones hidrofílicas e hidrofóbicas. Usando herramientas de predicción estructural y membranas modelo, mostraron que ambos péptidos pueden unirse no solo a los lípidos aniónicos habituales, sino también al ácido fosfatídico, insertándose en estas membranas alteradas y alterando su organización. La melitina demostró ser especialmente eficaz en hacer que las membranas modelo de E. coli presentaran fugas, mientras que la LL-37 mostró una capacidad de fuga directa más débil en las mismas condiciones, lo que sugiere que puede apoyarse en un conjunto más amplio de acciones además de perforar la membrana.
Observando la muerte celular en tiempo real
Para conectar el daño en la membrana con la muerte bacteriana real, los investigadores realizaron seis ensayos complementarios en paralelo. Estos siguieron qué tan bien los péptidos se unían a la superficie celular, si la membrana externa e interna se volvían permeables, si el potencial eléctrico a través de la membrana interna colapsaba y cómo cambiaban la energía celular (ATP) y la actividad de enzimas metabólicas. Crucialmente, midieron estos efectos tanto en E. coli normal como en el mutante con membrana remodelada, además de contar cuántas células aún podían formar colonias. Esto produjo “perfiles” detallados que muestran qué eventos se elevaban y se saturaban en qué concentraciones de péptido y tiempos, trazando de forma efectiva el camino desde el primer contacto hasta la muerte celular.
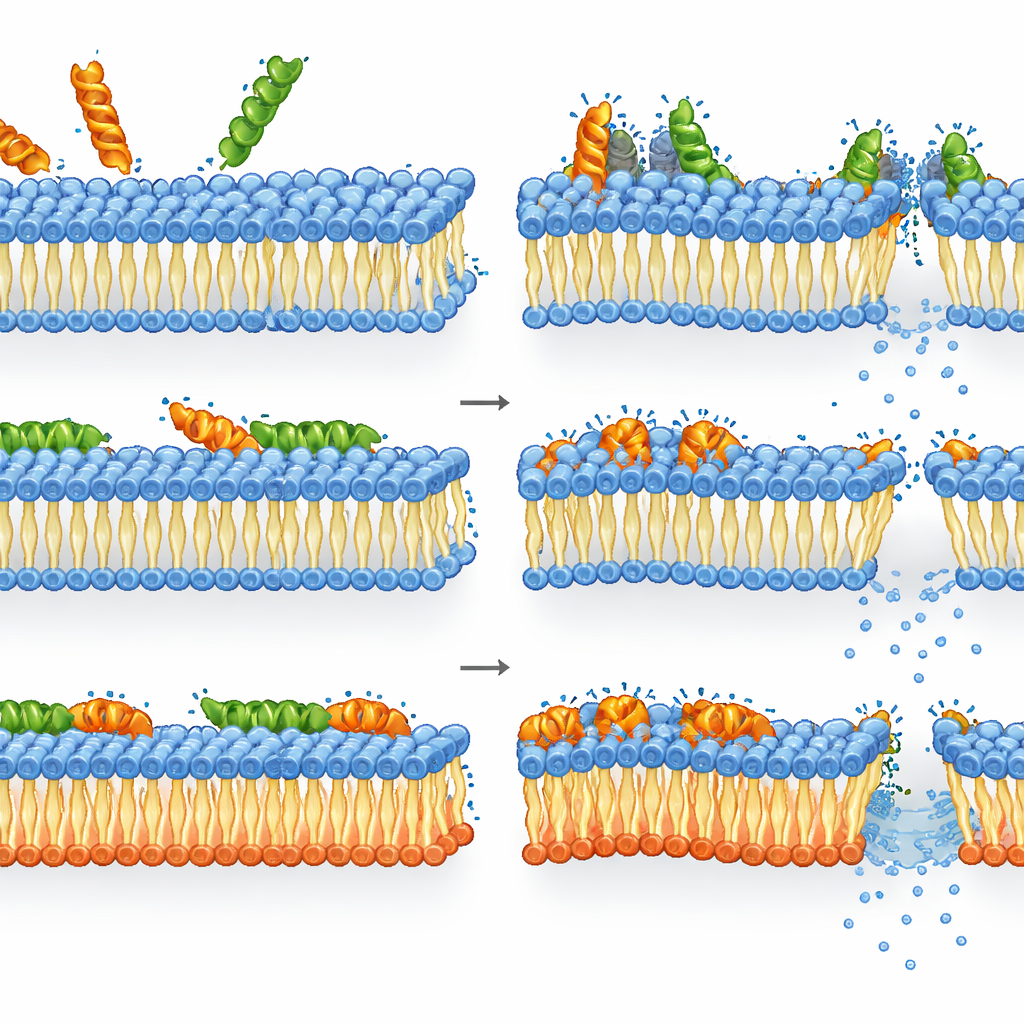
Cómo manejan la membrana remodelada la melitina y la LL-37
La melitina resultó ser incluso más letal contra bacterias que carecían de los lípidos aniónicos habituales que contra el tipo salvaje. En el mutante, la pérdida de integridad de la membrana, el descenso de los niveles de energía y la pérdida de viabilidad estuvieron estrechamente vinculados: una vez que la melitina perturbó la membrana remodelada, las células murieron rápidamente. En el tipo salvaje, sin embargo, el panorama fue más matizado. La permeabilización y la despolarización de la membrana ya estaban saturadas a concentraciones en las que el ATP y la actividad enzimática se mantenían relativamente altas. En otras palabras, muchas células tenían membranas gravemente dañadas pero seguían siendo metabólicamente activas aunque incapaces de formar colonias —lo que sugiere que el poder letal de la melitina proviene de un daño membranoso severo, posiblemente transitorio, del que las células no pueden recuperarse por completo, incluso si su maquinaria interna sigue funcionando brevemente.
Un péptido humano más resistente y versátil
La LL-37 se comportó de manera diferente. Neutralizó la carga superficial y dañó ambas membranas en células de tipo salvaje y mutantes en grado similar, lo que indica que su acción fue en gran medida independiente de la mezcla precisa de lípidos aniónicos. A concentraciones en las que las membranas interna y externa ya estaban muy comprometidas, muchas células aún mostraban actividad metabólica medible y los niveles de ATP no siempre caían a cero. Esta separación temporal implica que el golpe final letal de la LL-37 probablemente involucra objetivos más allá de la membrana —como la alteración de la generación de energía, la inducción de estrés oxidativo o el endurecimiento del citoplasma al unirse al ADN y a los ribosomas— una vez que ha accedido al interior celular.
Qué significa esto para futuros antimicrobianos
En conjunto, el estudio muestra que el remodelado de la membrana —incluso cambios drásticos alejándose de los lípidos aniónicos habituales hacia el ácido fosfatídico— no libra a las bacterias de la melitina ni de la LL-37. Ambos péptidos se adaptan al nuevo paisaje lipídico, siguen uniéndose, insertándose y, en última instancia, matando. Los perfiles detallados de los ensayos revelan que la muerte bacteriana no es un interruptor simple que se activa en el momento en que se perfora la membrana, sino una red de eventos superpuestos que puede dejar a las células dañadas e incapaces de crecer mucho antes de que todas las señales metabólicas desaparezcan. Al vincular marcadores específicos de membrana y viabilidad con la muerte real, este trabajo proporciona un plano sobre cómo evaluar y comparar nuevos péptidos antimicrobianos, y sugiere que cambiar simplemente la composición lipídica de la membrana probablemente no sea una vía de escape fácil para las bacterias frente a estas moléculas potentes y multifacéticas.
Cita: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Palabras clave: péptidos antimicrobianos, membranas bacterianas, remodelado de lípidos, resistencia a antibióticos, LL-37 y melitina