Clear Sky Science · it
Destino delle cellule batteriche sotto stress: rimodellamento dei lipidi e attacco di peptidi antimicrobici
Perché questo è importante per combattere le infezioni
Man mano che sempre più batteri diventano resistenti ai nostri migliori antibiotici, gli scienziati si rivolgono a molecole difensive naturali chiamate peptidi antimicrobici, presenti in organismi che vanno dalle api all’uomo. Ma i batteri non sono bersagli passivi: possono rimodellare la membrana lipidica che avvolge le loro cellule, eludendo potenzialmente questi nuovi farmaci. Questo studio pone una domanda pratica dalle grandi implicazioni: quando i batteri modificano i lipidi di membrana sotto stress, due noti peptidi antimicrobici — la melittina del veleno delle api e l’LL-37 umano — riescono ancora a ucciderli, e in che modo lo fanno esattamente?
Batteri sotto pressione
I batteri affrontano costantemente condizioni avverse: variazioni di temperatura o salinità, attacchi del sistema immunitario ed esposizione ad antibiotici. Per far fronte a questi stress, riconfigurano le molecole grasse, o lipidi, che costituiscono il loro confine esterno, regolando proprietà come spessore, fluidità e carica superficiale. Un componente lipidico chiave, l’acido fosfatidico, normalmente presente solo in piccole quantità, può accumularsi quando altri lipidi anionici (negativamente carichi) si riducono. Questi lipidi carichi sono di solito i punti di ancoraggio preferenziali per i peptidi antimicrobici carichi positivamente. Gli autori hanno usato il batterio modello Escherichia coli e un ceppo mutante che è in gran parte privo di due principali lipidi anionici, sostituendoli con più acido fosfatidico, per imitare il tipo di rimodellamento di membrana che potrebbe verificarsi sotto pressione farmacologica.
Due peptidi, due stili di attacco
Il gruppo si è concentrato su melittina e LL-37, peptidi classici attivi sulle membrane che condividono una forma elicoidale ma differiscono nell’organizzazione delle regioni idrofile e idrofobiche. Usando strumenti di predizione strutturale e membrane modello, hanno mostrato che entrambi i peptidi possono legarsi non solo ai consueti lipidi anionici ma anche all’acido fosfatidico, inserendosi in queste membrane alterate e perturbandone l’organizzazione. La melittina si è rivelata particolarmente efficace nel rendere le membrane modello di E. coli permeabili, mentre LL-37 ha mostrato una perdita diretta più debole nelle stesse condizioni, suggerendo che potrebbe fare affidamento su un insieme più ampio di azioni oltre al semplice “foro” nella membrana.
Osservare le cellule morire in tempo reale
Per collegare il danno alla membrana con la morte batterica reale, i ricercatori hanno eseguito sei saggi complementari in parallelo. Questi tracciavano quanto bene i peptidi si legavano alla superficie cellulare, se la membrana esterna e interna diventavano permeabili, se il potenziale elettrico attraverso la membrana interna collassava e come cambiavano l’energia (ATP) e l’attività degli enzimi metabolici delle cellule. Fondamentale è che hanno misurato questi effetti sia in E. coli normale sia nel mutante con lipidi rimodellati, contando anche quante cellule potevano ancora formare colonie. Il risultato sono stati profili dettagliati che mostrano quali eventi aumentano e si saturano a quali concentrazioni e tempi di peptide, mappando in pratica la strada dal primo contatto alla morte cellulare.
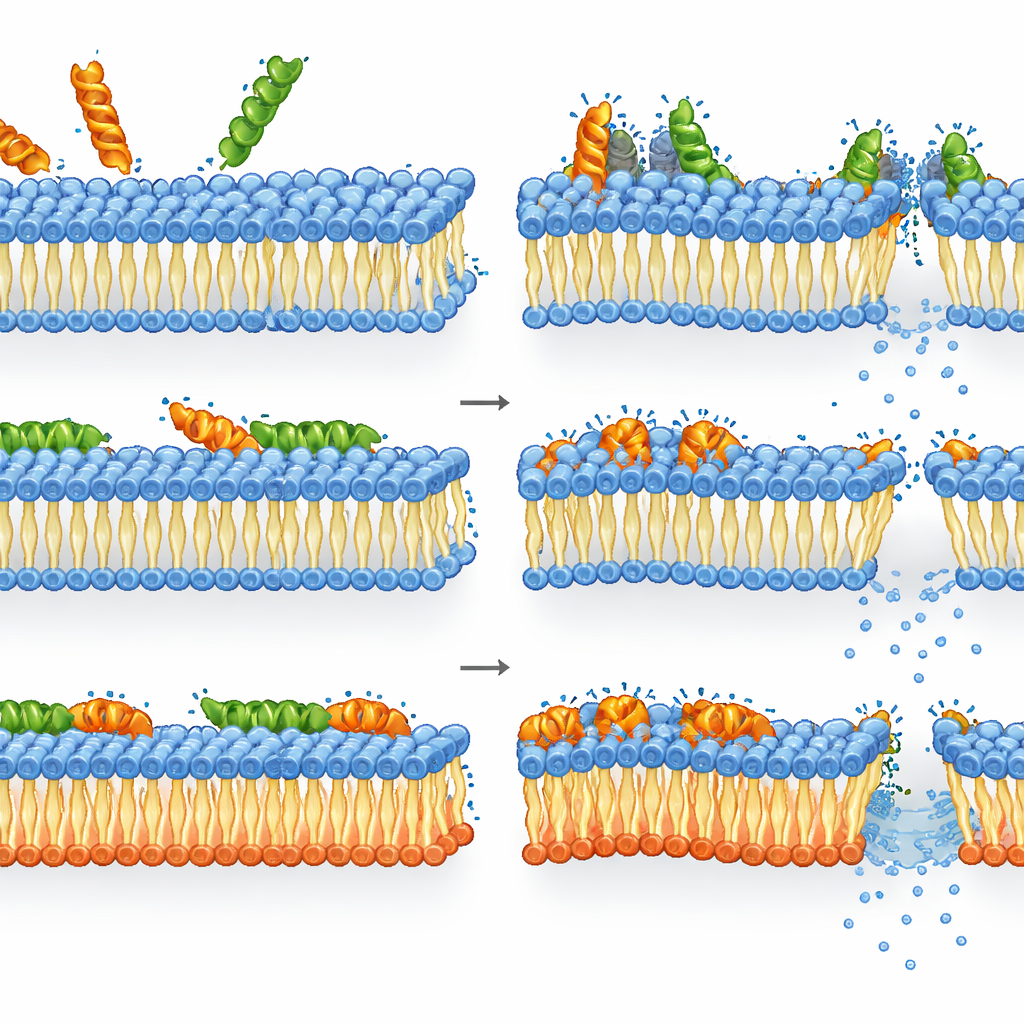
Come melittina e LL-37 affrontano le membrane rimodellate
La melittina si è dimostrata ancora più letale contro i batteri privi dei consueti lipidi anionici rispetto al tipo selvatico. Nel mutante, perdita dell’integrità della membrana, calo dell’energia e perdita di vitalità erano strettamente collegati: una volta che la melittina comprometteva la membrana rimodellata, le cellule morivano rapidamente. Nel ceppo selvatico, invece, il quadro era più sfumato. La permeabilizzazione e la depolarizzazione della membrana erano già sature a concentrazioni alle quali ATP e attività enzimatica rimanevano relativamente elevate. In altre parole, molte cellule avevano membrane gravemente danneggiate ma erano ancora metabolicamente attive pur non riuscendo a formare colonie — il che suggerisce che il potere uccidente della melittina deriva da danni alla membrana gravi, possibilmente transitori, dai quali le cellule non riescono a riprendersi completamente, anche se la loro macchina interna continua a funzionare brevemente.
Un peptide umano più robusto e versatile
LL-37 si è comportato diversamente. Ha neutralizzato la carica superficiale e danneggiato entrambe le membrane in cellule di tipo selvatico e mutante in misura quasi uguale, indicando che la sua azione era in larga parte indipendente dalla precisa composizione di lipidi anionici. A concentrazioni in cui membrana interna ed esterna erano già fortemente compromesse, molte cellule mostravano ancora attività metabolica misurabile e i livelli di ATP non scendevano sempre a zero. Questa discrepanza temporale suggerisce che il colpo mortale finale di LL-37 coinvolge probabilmente bersagli oltre la membrana stessa — come la compromissione della generazione di energia, l’innesco di stress ossidativo o l’irrigidimento del citoplasma legandosi a DNA e ribosomi — una volta che ha guadagnato accesso all’interno della cellula.
Cosa significa per i futuri antimicrobici
Complessivamente, lo studio dimostra che il rimodellamento della membrana — anche cambiamenti drastici che spostano la composizione dagli abituali lipidi anionici verso l’acido fosfatidico — non salva i batteri dalla melittina o da LL-37. Entrambi i peptidi si adattano al nuovo paesaggio lipidico, continuando a legarsi, inserirsi e infine uccidere. I profili dettagliati dei saggi rivelano che la morte batterica non è un semplice interruttore on–off nel momento in cui la membrana viene perforata, ma una rete di eventi sovrapposti che può lasciare le cellule danneggiate e incapaci di crescere molto prima che tutti i segnali metabolici svaniscano. Collegando marcatori specifici di membrana e di vitalità alla morte effettiva, questo lavoro fornisce una guida su come valutare e confrontare nuovi peptidi antimicrobici, e suggerisce che cambiare semplicemente la composizione lipidica della membrana è probabilmente una via di fuga difficile per i batteri di fronte a queste molecole potenti e multi‑pronged.
Citazione: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Parole chiave: peptidi antimicrobici, membrane batteriche, rimodellamento dei lipidi, resistenza agli antibiotici, LL-37 e melittina