Clear Sky Science · de
Bakterienzellschicksal unter Stress: Lipidumbau und Angriff durch antimikrobielle Peptide
Warum das für die Bekämpfung von Infektionen wichtig ist
Da immer mehr Bakterien gegen unsere wichtigsten Antibiotika resistent werden, richten Forscher ihr Augenmerk auf natürliche Abwehrmoleküle, sogenannte antimikrobielle Peptide, die in Organismen von Bienen bis zum Menschen vorkommen. Bakterien sind jedoch keine passiven Ziele: Sie können die ölige Membran, die ihre Zellen umgibt, umbauen und sich so möglicherweise gegen diese neuen Wirkstoffe schützen. Diese Studie stellt eine praktische Frage mit weitreichenden Folgen: Wenn Bakterien unter Stress ihre Membranlipide verändern, können zwei bekannte antimikrobielle Peptide — Melittin aus Bienengift und das humane LL-37 — sie dann noch abtöten, und wenn ja, wie genau geschieht das?
Bakterien unter Druck
Bakterien sind ständig rauen Bedingungen ausgesetzt: Temperaturschwankungen oder Salzveränderungen, Angriffen des Immunsystems und der Einwirkung von Antibiotika. Um damit fertigzuwerden, rekonfigurieren sie die Fettsäuremoleküle, also die Lipide, die ihre äußere Grenze bilden, und passen Eigenschaften wie Dicke, Fluidität und Oberflächenladung an. Ein wichtiger Lipidbaustein, Phosphatidinsäure, der normalerweise nur in geringen Mengen vorkommt, kann sich ansammeln, wenn andere negativ geladene Lipide reduziert werden. Diese geladenen Lipide sind normalerweise bevorzugte Anlagerungsstellen für positiv geladene antimikrobielle Peptide. Die Autoren nutzten das Modellbakterium Escherichia coli und einen Mutantenstamm, dem weitgehend zwei wichtige anionische (negativ geladene) Lipide fehlen und der stattdessen mehr Phosphatidinsäure aufweist, um den Membranumbau zu simulieren, der unter Arzneidruck auftreten könnte.
Zwei Peptide, zwei Angriffsarten
Das Team konzentrierte sich auf Melittin und LL-37, klassische membranaktive Peptide, die zwar beide eine helikale Form haben, sich aber in der Anordnung ihrer wasserliebenden und fettliebenden Bereiche unterscheiden. Mittels Strukturvorhersage-Tools und Modellmembranen zeigten sie, dass beide Peptide nicht nur an die üblichen anionischen Lipide binden, sondern auch an Phosphatidinsäure, in diese veränderten Membranen eindringen und deren Organisation stören können. Melittin erwies sich als besonders wirkungsvoll darin, Modellmembranen von E. coli durchlässig zu machen, während LL-37 unter denselben Bedingungen weniger direkte Leckage verursachte, was darauf hindeutet, dass es auf ein breiteres Wirkungsspektrum als reines „Lochstoßen" in der Membran ankommen könnte.
Zellen beim Sterben in Echtzeit beobachten
Um Membranschäden mit dem tatsächlichen Absterben der Bakterien zu verknüpfen, führten die Forscher sechs komplementäre Tests nebeneinander durch. Diese verfolgten, wie gut Peptide an die Zelloberfläche binden, ob die äußere und innere Membran durchlässig werden, ob das elektrische Potenzial über der inneren Membran zusammenbricht und wie sich die Energie der Zellen (ATP) und die Aktivität metabolischer Enzyme verändern. Entscheidend war, dass sie diese Effekte sowohl in normalen E. coli als auch im lipid-umgebauten Mutanten maßen und gleichzeitig die noch koloniebildungsfähigen Zellen zählten. So entstanden detaillierte „Profile“, die zeigen, welche Ereignisse bei welchen Peptidkonzentrationen und zu welchen Zeiten ansteigen und saturieren — eine Karte vom Erstkontakt bis zum Zelltod.
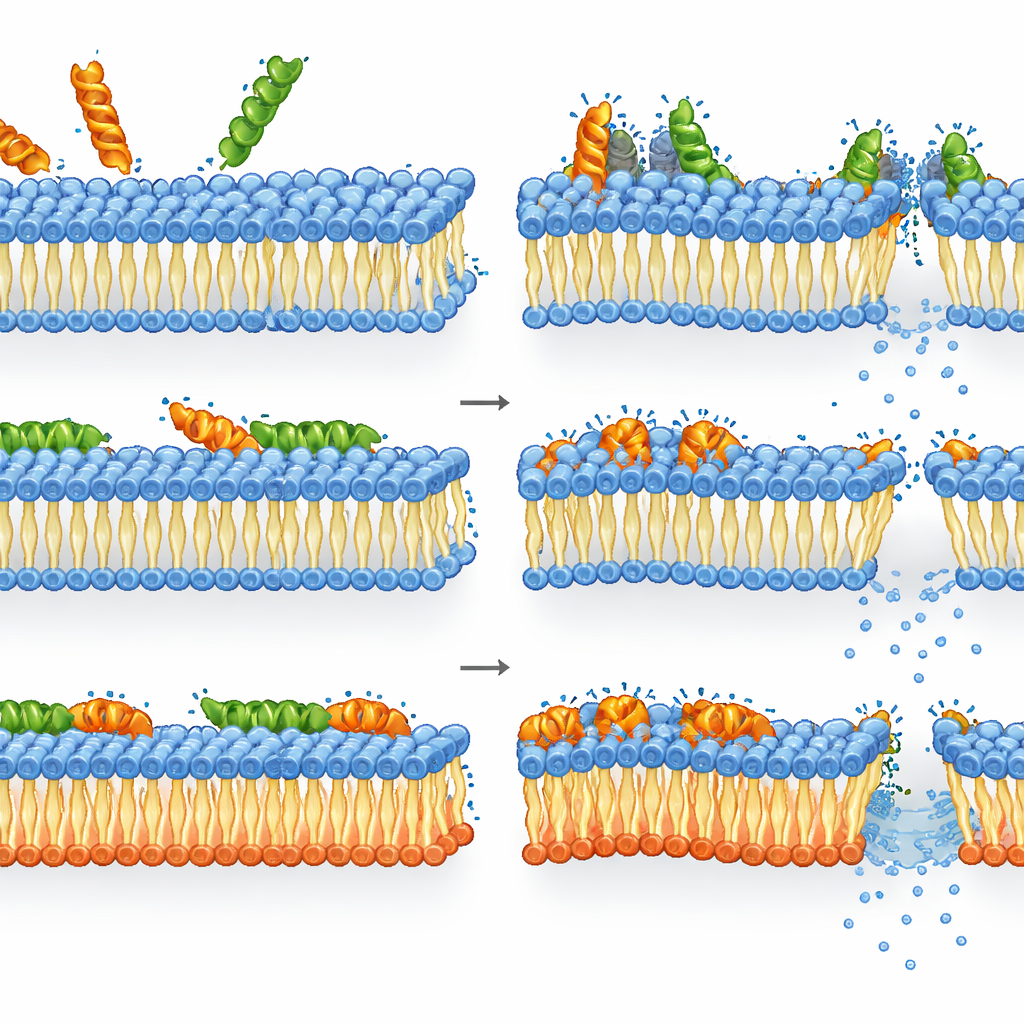
Wie Melittin und LL-37 mit umgebauten Membranen umgehen
Melittin erwies sich als sogar noch tödlicher gegen Bakterien, denen die üblichen anionischen Lipide fehlten, als gegen den Wildtyp. Im Mutanten waren Membranintegrität, abnehmende Energielevel und Verlust der Lebensfähigkeit eng miteinander verknüpft: Sobald Melittin die umgebaute Membran störte, starben die Zellen rapide. Beim Wildtyp war das Bild dagegen nuancierter. Membranpermeabilisierung und Depolarisation waren bereits bei Konzentrationen gesättigt, bei denen ATP und Enzymaktivität noch relativ hoch blieben. Mit anderen Worten: Viele Zellen hatten stark beschädigte Membranen, waren jedoch noch metabolisch aktiv, konnten aber keine Kolonien mehr bilden — was darauf hindeutet, dass Melittins Tötungskraft von schweren, möglicherweise vorübergehenden Membranschäden herrührt, von denen sich die Zellen nicht vollständig erholen können, selbst wenn ihre innere Maschinerie kurzzeitig weiterläuft.
Ein härteres, vielseitigeres humanes Peptid
LL-37 verhielt sich anders. Es neutralisierte die Oberflächenladung und schädigte beide Membranen in Wildtyp- und Mutantenzellen in nahezu gleichem Ausmaß, was darauf hinweist, dass seine Wirkung weitgehend unabhängig von der genauen Zusammensetzung anionischer Lipide ist. Bei Konzentrationen, bei denen innere und äußere Membran bereits stark beeinträchtigt waren, zeigten viele Zellen noch messbare Stoffwechselaktivität und die ATP-Spiegel fielen nicht immer auf null. Diese zeitliche Lücke deutet darauf hin, dass der finale Todesstoß von LL-37 wahrscheinlich Ziele jenseits der Membran umfasst — etwa die Störung der Energieerzeugung, Auslösung oxidativen Stresses oder das Versteifen des Zytoplasmas durch Bindung an DNA und Ribosomen — sobald es Zugang zum Zellinneren erlangt hat.
Was das für zukünftige antimikrobielle Mittel bedeutet
Insgesamt zeigt die Studie, dass Membranumbau — selbst drastische Verschiebungen weg von den üblichen anionischen Lipiden hin zu Phosphatidinsäure — die Bakterien weder vor Melittin noch vor LL-37 rettet. Beide Peptide passen sich der neuen Lipidlandschaft an, binden weiterhin, dringen ein und töten letztlich. Die detaillierten Testprofile machen deutlich, dass bakterieller Tod kein einfacher Ein-/Ausschalter im Moment des Membrandurchbruchs ist, sondern ein Geflecht überlappender Ereignisse, das Zellen schon lange vor dem Verschwinden aller metabolischen Signale beschädigt und das Wachstum verhindert. Indem bestimmte Membran- und Lebensfähigkeitsmarker mit tatsächlichem Absterben verknüpft werden, liefert diese Arbeit eine Vorlage dafür, wie neue antimikrobielle Peptide bewertet und verglichen werden können, und legt nahe, dass die bloße Änderung der Membranlipidzusammensetzung kaum ein leichter Fluchtweg für Bakterien gegen diese potenten, vielschichtigen Moleküle sein wird.
Zitation: Vejzovic, D., Schwaiger, T., Topciu, A. et al. Bacterial cell fate under stress: lipid remodeling and antimicrobial peptide attack. npj Antimicrob Resist 4, 22 (2026). https://doi.org/10.1038/s44259-026-00195-7
Schlüsselwörter: antimikrobielle Peptide, bakterielle Membranen, Lipidumbau, Antibiotikaresistenz, LL-37 und Melittin