Clear Sky Science · zh
PCBP1 调控先天性心肌病中 AARS2 的可变剪接
为什么有些婴儿天生心脏衰竭
一些婴儿在出生后不久就出现严重的心力衰竭,这并非由血管堵塞引起,而是源于心肌细胞在产生能量时的微小缺陷。临床上已将这种情况与名为 AARS2 的基因突变联系起来,但从 DNA 变化到心脏发育不良、功能减弱的分子中间步骤一直不明晰。这项研究揭示了一个关键的缺失环节:一种分子“编辑者”,在心肌细胞正确拼接 AARS2 信息上发挥作用,从而使线粒体——细胞的能量工厂——维持心脏跳动。
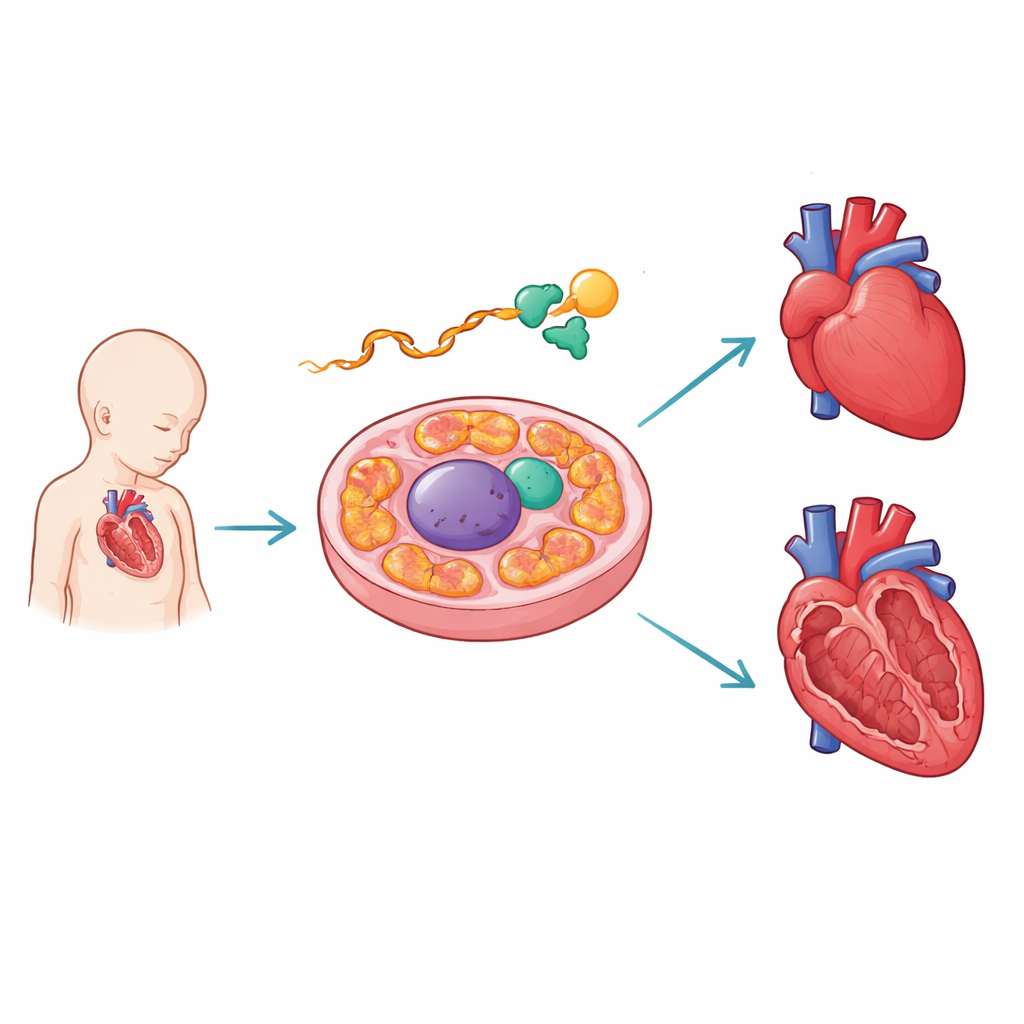
保护发育中心脏的分子编辑者
作者将注意力集中在 PCBP1 上,这是一种结合 RNA 的蛋白。在发育中的小鼠心脏中,他们发现 PCBP1 附着在 AARS2 的 RNA 上,位于一个关键的连接位点附近。AARS2 在将氨基酸丙氨酸加载到线粒体内的转运 RNA 上起重要作用,这是合成负责能量产生蛋白质的关键步骤。通过高通量结合位点图谱和工程化报告构建体,团队表明 PCBP1 的结合位点与人类致病突变重叠,这些突变会破坏 AARS2 信息中第 16 外显子的拼接。当 PCBP1 缺失或其结合位点受损时,该外显子会被跳过,导致无法生成全长的 AARS2 酶的指令被破坏。
当编辑失败,心脏结构紊乱
为了解这一变化对整个器官的影响,研究人员选择性地从小鼠心肌细胞中去除了 PCBP1。这些心脏发育异常:心壁变薄且呈海绵状而非致密,心尖常出现分裂,类似人类称为左室非致密化的畸形。许多小鼠在出生后不久死亡。在 RNA 水平上,数百个基因呈现出向早期胚胎不成熟模式的转变,表明心室腔室成熟延迟。值得注意的是,Aars2 的转录本几乎总是跳过第 16 外显子,导致转录本缩短且 AARS2 蛋白显著下降,证实该单一基因的错误剪接是丧失 PCBP1 的重要后果。
直接损伤 AARS2 可再现疾病表型
接着,团队构建了仅在心肌细胞中可删除 Aars2 第 16 外显子的工程小鼠。这些动物与 PCBP1 缺失模型高度相似:表现出室壁畸形、围生期死亡,并显示相同的不成熟基因表达特征。当研究者在出生后利用第二个遗传开关在生命后期触发 Aars2 丧失时,动物起初看似健康,但很快出现心脏扩大、功能衰弱并伴有广泛瘢痕。电子显微镜显示它们的线粒体内膜折叠减少,详细的生化检测表明呼吸链中负责能量生成的关键复合体,尤其是复合体 I 和 IV,在明显心力衰竭出现之前就已不稳定并丧失活性。
受损线粒体如何向细胞核发出信号
AARS2 的功能丧失使心肌细胞线粒体无法维持正常的氧化磷酸化,这是它们生成 ATP 的主要方式。在 PCBP1 缺失和 Aars2 缺失的心脏中,许多编码能量装置组分的核基因表达被下调,相应的线粒体蛋白也被耗竭。与此同时,细胞启动了一套协调的应激计划,即未折叠蛋白反应和整合性应激反应。该通路的关键因子,包括转录因子 ATF4 及其上游触发子磷酸化的 eIF2α,明显上升,线粒体蛋白酶 LONP1(负责清除受损蛋白)也升高。在年长的 Aars2 突变体中,研究者还观察到生长调节子 MYC 的激活和核仁(核糖体制造工厂)的肿大,以及核编码的线粒体翻译因子激增,提示细胞核正试图补偿线粒体蛋白质合成的衰退。
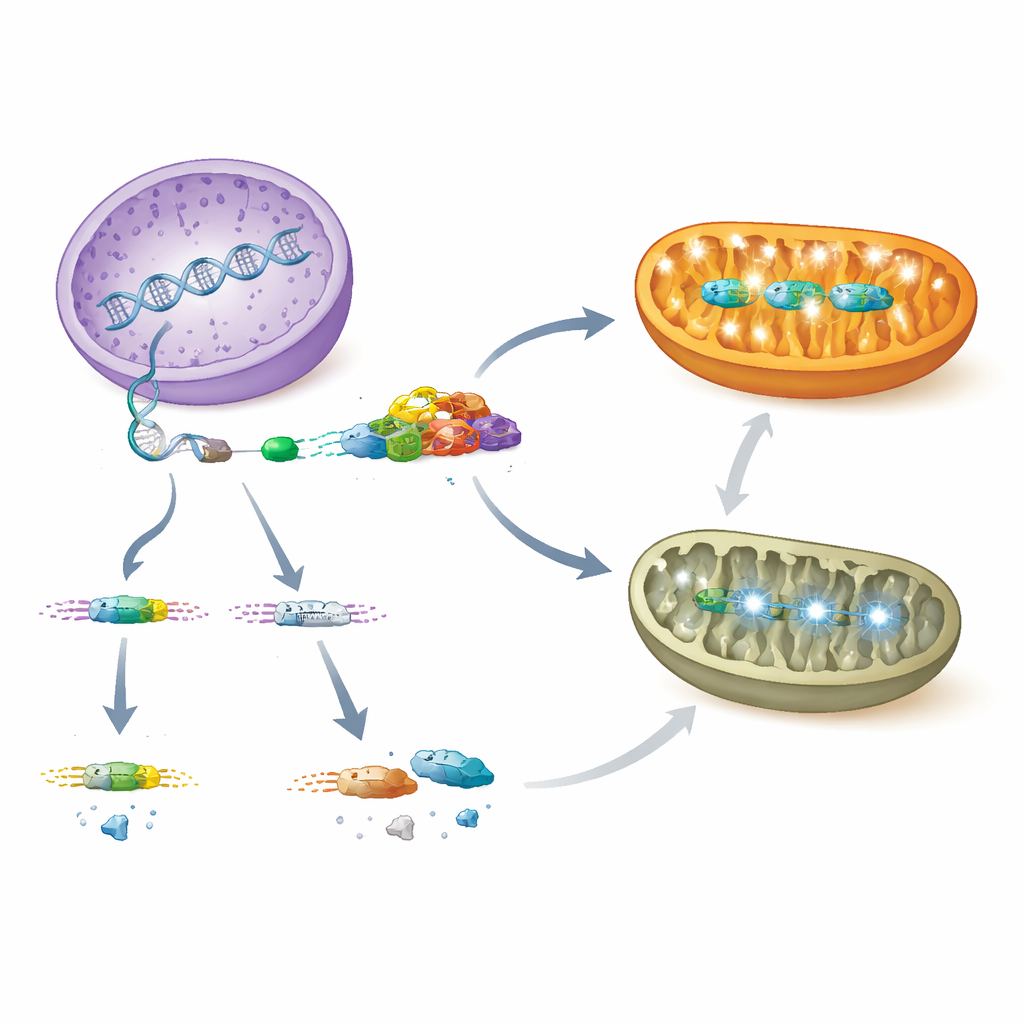
对罕见儿童心衰的意义
总体来看,这些发现描绘了一条从基因调控到器官疾病的清晰路径。PCBP1 在心肌细胞中结合 AARS2 的 RNA,确保第 16 外显子的包含,从而生成稳定的酶以支持线粒体蛋白合成和充足的能量输出。当 PCBP1 丢失或突变破坏这一剪接步骤时,第 16 外显子被跳过,AARS2 水平崩溃,线粒体能量复合体瓦解,心脏发育期的壁层无法正常致密化,导致致命性心肌病。受压的线粒体随后将信号传回细胞核以激活保护性程序,但这些反应不足以阻止心衰。通过阐明 PCBP1–AARS2 轴,这项研究提示了新的诊断标志物和潜在的治疗靶点,可用于诊断和干预那些病因不明的婴幼儿线粒体性心脏病。
引用: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
关键词: 线粒体性心肌病, RNA 剪接, 先天性心脏病, AARS2 基因, 线粒体应激反应