Clear Sky Science · sv
PCBP1 reglerar alternativ splitsning av AARS2 vid medfödd kardiomyopati
Varför vissa spädbarn föds med ett sviktande hjärta
Vissa nyfödda utvecklar kort efter födseln en svår form av hjärtsvikt som inte beror på tilltäppta blodkärl utan på små fel i hur deras hjärtceller framställer energi. Läkare har kopplat detta till mutationer i en gen som heter AARS2, men stegen som förbinder en DNA-förändring med ett svagt, illa format hjärta har förblivit oklara. Denna studie avslöjar en avgörande saknad länk: en molekylär ”redaktör” som hjälper hjärtceller att korrekt sammanfoga AARS2-meddelandet så att deras mitokondrier — cellens kraftverk — kan hålla hjärtat igång.
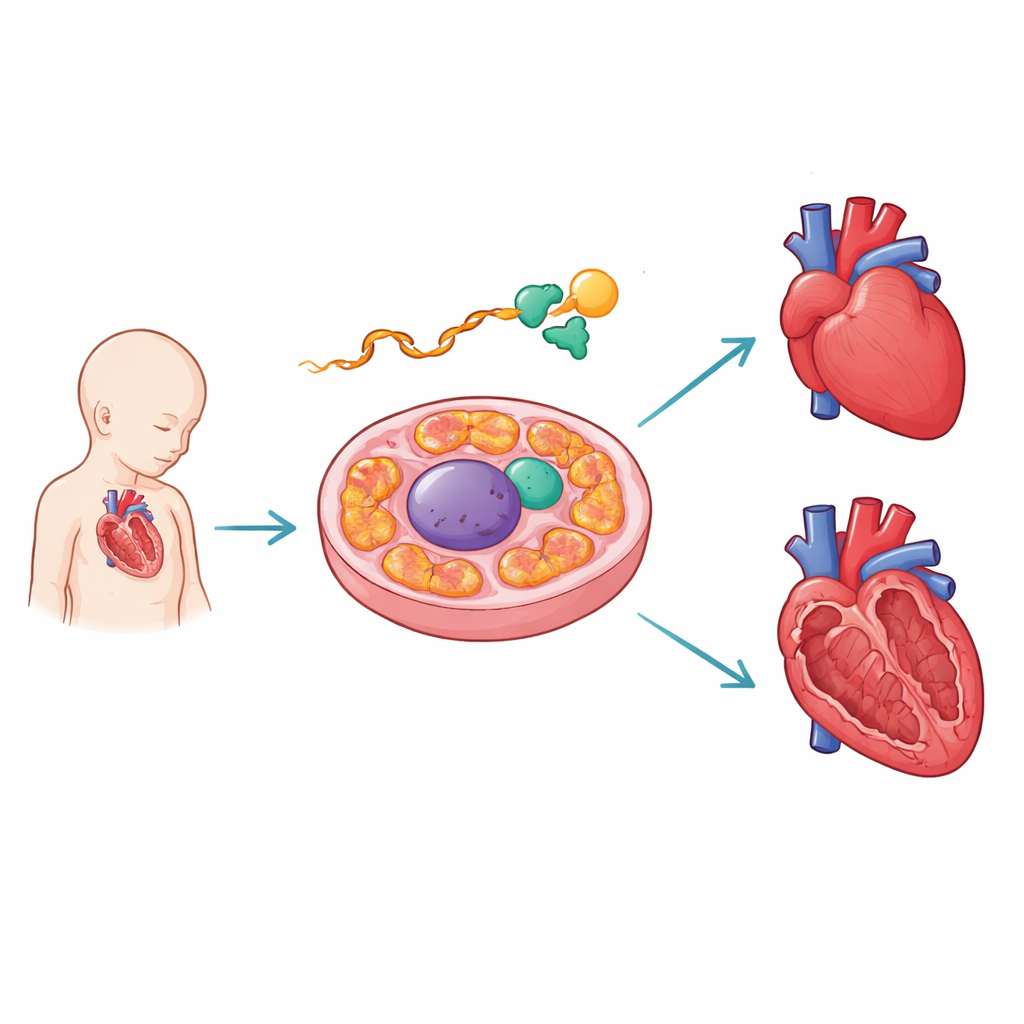
En molekylär redaktör som skyddar det växande hjärtat
Författarna koncentrerade sig på PCBP1, ett protein som binder RNA, de mellanliggande buden kopierade från DNA. I utvecklande musehjärtan fann de att PCBP1 fångar upp RNA för AARS2 nära en kritisk föreningspunkt. AARS2 hjälper till att fästa aminosyran alanin på transfer-RNA i mitokondrierna, ett viktigt steg i att bygga de proteiner som driver energiproduktionen. Med hjälp av höggenomströmmande kartläggning av bindningsställen och konstruerade rapporter visade teamet att PCBPs kontaktpunkter sammanfaller med humana sjukdomsmutationer som stör hopsättningen av en särskild del — exon 16 — av AARS2-meddelandet. När PCBP1 saknas eller dess bindningsställen är skadade hoppas detta exon över, vilket störtar instruktionerna för att göra ett fullängds AARS2-enzym.
När redigeringen misslyckas blir hjärtstrukturen felaktig
För att förstå vad detta innebär för ett helt organ borttog forskarna selektivt PCBP1 från musens hjärtmuskelceller. Dessa hjärtan utvecklades onormalt: deras väggar var tunna och svampiga istället för tätt kompakta, och hjärtspetsen delade sig ofta i två, en missbildning som liknar ett mänskligt tillstånd kallat left ventricular non-compaction. Många möss dog strax efter födseln. På RNA-nivå skiftade hundratals gener mot ett omoget, tidigt embryonalt mönster, vilket indikerar försenad mognad av hjärtkammare. Särskilt hoppade Aars2-meddelandet nästan alltid över exon 16, vilket ledde till ett förkortat transkript och en dramatisk minskning av AARS2-protein, vilket bekräftar att felaktig splitsning av denna enda gen är en huvudkonsekvens av att förlora PCBP1.
Direkt skada på AARS2 återskapar sjukdomen
Nästa steg var att konstruera möss där exon 16 i Aars2 endast kunde tas bort i hjärtmuskelceller. Dessa djur efterliknade PCBP1-utslagen: de visade missformade kammarväggar, dog kring födseln och deras hjärtan uppvisade samma omogna genuttryckssignatur. När forskarna utlöste förlust av Aars2 senare i livet med en andra, postnatal genetisk switch verkade djuren initialt friska men utvecklade snart förstorade, försvagade hjärtan med omfattande ärrbildning. Elektronmikroskopi visade att deras mitokondrier hade färre inre veck, och detaljerade biokemiska analyser visade att centrala energiproducerande komplex i andningskedjan, särskilt komplex I och IV, destabiliserades och förlorade aktivitet långt innan tydliga tecken på hjärtsvikt uppträdde.
Hur kämpande mitokondrier signalerar tillbaka till kärnan
Förlusten av AARS2 gjorde att hjärtcellernas mitokondrier inte kunde upprätthålla normal oxidativ fosforylering, det huvudsakliga sättet att producera ATP. I både PCBP1-defekta och Aars2-defekta hjärtan dämpades många nukleära gener som kodar för komponenter i energimaskineriet, och de faktiska mitokondriella proteinerna de producerade gick förlorade. Samtidigt aktiverade cellerna ett koordinerat stressprogram känt som den unfolded protein response och den integrerade stressresponser. Centrala aktörer i denna kaskad, inklusive proteinet ATF4 och dess upstream-trigger, fosforylerat eIF2α, ökade kraftigt, liksom LONP1, en mitokondriell proteas som rensar skadade proteiner. Hos äldre Aars2-mutanter såg forskarna också aktivering av tillväxtregulatorn MYC och förstorad nukleol — fabriken för ribosomtillverkning — tillsammans med en uppgång av nukleärt kodade faktorer för mitokondriell translation, vilket antyder att kärnan försökte kompensera för den bristande mitokondriella proteinproduktionen.
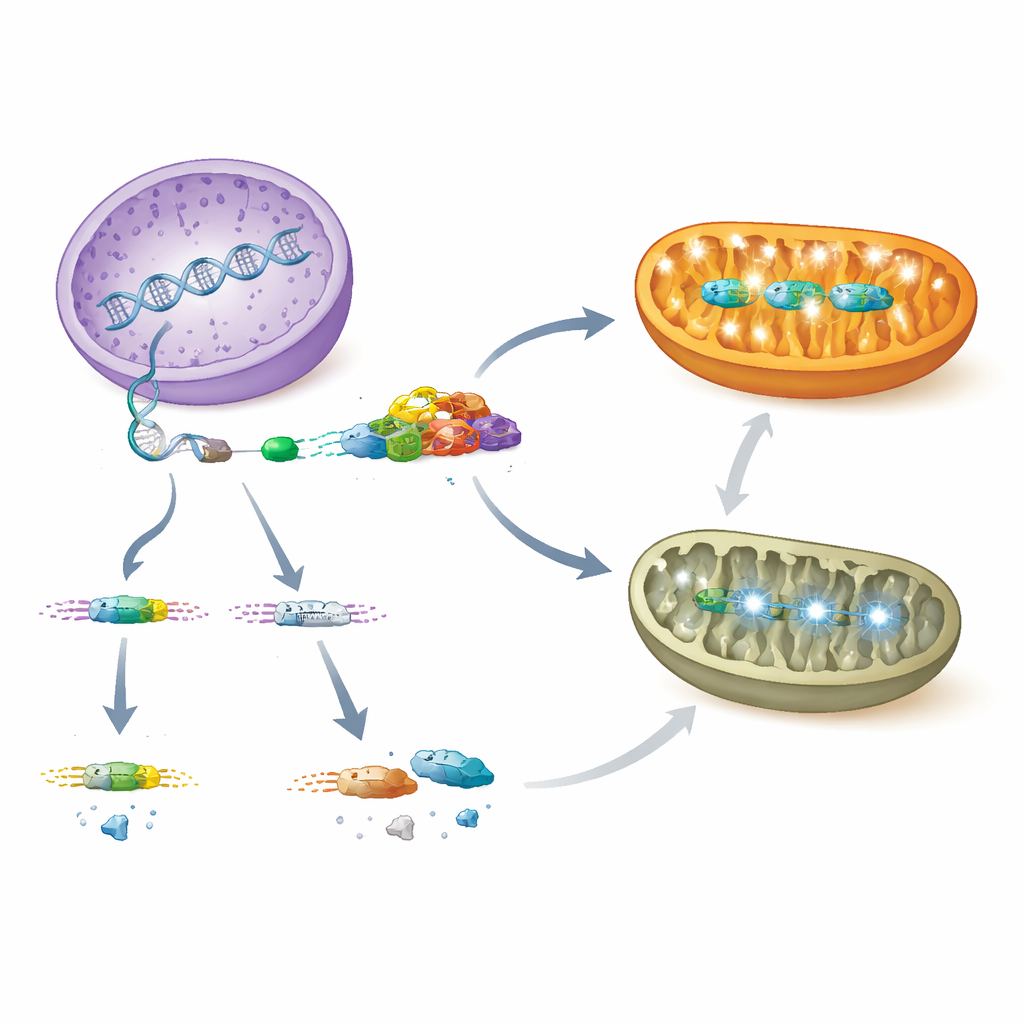
Vad detta innebär för barn med sällsynt hjärtsvikt
Tillsammans skisserar dessa fynd en tydlig väg från genreglering till organskada. PCBP1 binder normalt AARS2-RNA i hjärtceller och säkerställer att exon 16 inkluderas, vilket ger ett stabilt enzym som stödjer mitokondriell proteinsyntes och robust energiproduktion. När PCBP1 går förlorad eller när mutationer stör detta splitsningssteg hoppas exon 16 över, AARS2-nivåerna kollapsar, mitokondriella energikomplex faller isär och hjärtats väggar under utveckling kompakteras inte korrekt, vilket leder till dödlig kardiomyopati. De stressade mitokondrierna signalerar sedan tillbaka till kärnan för att aktivera skyddsprogram, men dessa svar räcker inte för att förhindra hjärtsvikt. Genom att belysa denna PCBP1–AARS2-axel föreslår studien nya diagnostiska markörer och potentiella terapeutiska mål för spädbarn och barn med annars oförklarlig mitokondriell hjärtsjukdom.
Citering: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Nyckelord: mitokondriell kardiomyopati, RNA-splitsning, medfödd hjärtsjukdom, AARS2-genen, mitokondriell stressrespons