Clear Sky Science · nl
PCBP1 reguleert alternatieve splicing van AARS2 bij congenitale cardiomyopathie
Waarom sommige baby’s met een falend hart worden geboren
Sommige zuigelingen ontwikkelen kort na de geboorte een ernstige vorm van hartfalen, niet door verstopte bloedvaten maar door kleine fouten in hoe hun hartcellen energie produceren. Artsen hebben deze aandoening in verband gebracht met mutaties in een gen dat AARS2 heet, maar de stappen die een verandering in het DNA verbinden met een zwak, slecht gevormd hart waren onduidelijk. Deze studie onthult een cruciale ontbrekende schakel: een moleculaire "redacteur" die helpt dat hartcellen het AARS2-bericht correct samenstellen, zodat hun mitochondriën — de energiecentrales van de cel — het kloppende hart kunnen blijven ondersteunen.
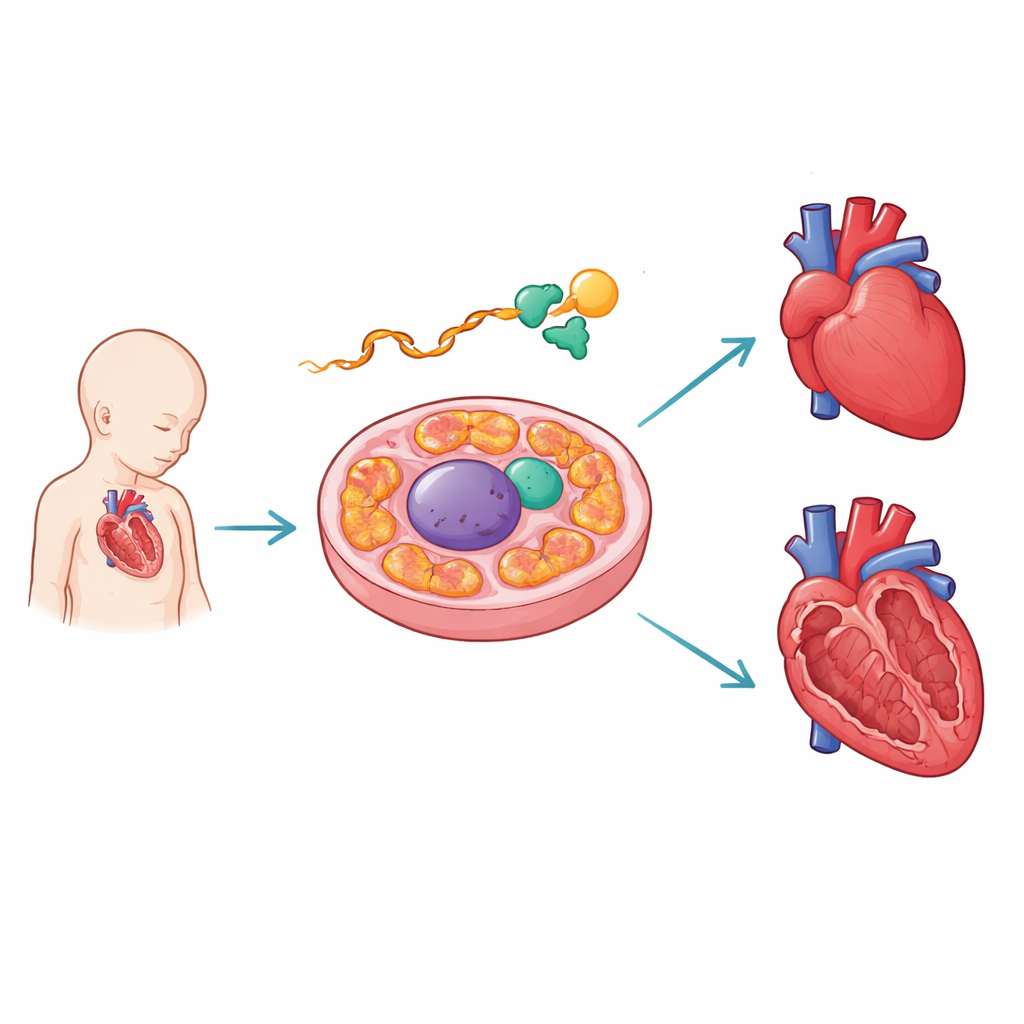
Een moleculaire redacteur die het ontwikkelende hart beschermt
De auteurs richtten zich op PCBP1, een eiwit dat aan RNA bindt, de tussenliggende boodschappen die van DNA worden gekopieerd. In zich ontwikkelende muizenharten vonden ze PCBP1 gebonden aan het RNA van Aars2 nabij een kritisch knooppunt. AARS2 helpt het aminozuur alanine op transport-RNA’s in mitochondriën te laden, een sleutelstap bij het opbouwen van de eiwitten die energieproductie aandrijven. Met behulp van grootschalige bindingskaarten en geconstrueerde rapporteurs toonden ze aan dat PCB P1’s contactpunten samenvallen met menselijke ziekte‑mutaties die het samenvoegen van één specifiek stukje — exon 16 — van het AARS2‑bericht verstoren. Wanneer PCBP1 ontbreekt of zijn bindingsplaatsen beschadigd zijn, wordt dit exon overgeslagen, waardoor de instructies voor het maken van een volledig AARS2‑enzym ontsporen.
Als het redigeren faalt, raakt de hartstructuur ontregeld
Om te zien wat dit voor een heel orgaan betekent, verwijderden de onderzoekers PCBP1 selectief uit muizenhartspiercellen. Deze harten ontwikkelden zich abnormaal: de wanden waren dun en sponsachtig in plaats van dicht en compact, en de top van het hart splitste vaak in twee, een misvorming die lijkt op de menselijke aandoening linksventrikel non‑compaction. Veel muizen overleden kort na de geboorte. Op RNA‑niveau schakelden honderden genen over naar een onrijper, vroeg‑embryonaal patroon, wat wijst op vertraagde rijping van de hartkamers. Opmerkelijk was dat het Aars2‑bericht vrijwel altijd exon 16 oversloeg, wat leidde tot een verkort transcript en een dramatische daling van het AARS2‑eiwit, waarmee wordt bevestigd dat foutieve splicing van dit enkele gen een belangrijk gevolg is van het verlies van PCBP1.
Direct schade toebrengen aan AARS2 bootst de ziekte na
Vervolgens maakten de onderzoekers muizen waarbij exon 16 van Aars2 alleen in hartspiercellen verwijderd kon worden. Deze dieren bootsten de PCBP1‑knockouts nauwkeurig na: ze vertoonden misvormde ventrikelwanden, overleden rond de geboorte en hun harten lieten hetzelfde onrijpe genexpressie‑kenmerk zien. Wanneer de onderzoekers het verlies van Aars2 later in het leven induceerden met een tweede, postnatale genetische schakelaar, leken de dieren aanvankelijk gezond maar ontwikkelden al snel vergrote, verzwakte harten met uitgebreide littekenvorming. Elektronenmicroscopie toonde dat hun mitochondriën minder interne plooien hadden, en gedetailleerde biochemische testen lieten zien dat sleutels voor energieproductie in de ademhalingsketen, vooral complexen I en IV, gedestabiliseerd waren en hun activiteit verloren ver vóórdat zichtbaar hartfalen optrad.
Hoe worstelende mitochondriën terugpraten met de kern
Het uitvallen van AARS2 maakte het voor mitochondriën in hartcellen onmogelijk om normale oxidatieve fosforylering te handhaven, de belangrijkste manier waarop ze ATP produceren. In zowel PCBP1‑deficiënte als Aars2‑deficiënte harten werden veel nucleaire genen die componenten van de energiemachines coderen omlaaggeschakeld, en de mitochondriale eiwitten die zij produceren raakten uitgeput. Tegelijkertijd zetten de cellen een gecoördineerd stressprogramma aan, bekend als de unfolded protein response en de geïntegreerde stressrespons. Centrale spelers in dit pad, waaronder het eiwit ATF4 en zijn upstream trigger, gefosforyleerd eIF2α, stegen sterk, evenals LONP1, een mitochondriale protease die beschadigde eiwitten opruimt. In oudere Aars2‑mutanten zagen de onderzoekers ook activatie van de groeiregulator MYC en vergroting van het nucleolus — de fabriek voor ribosoomproductie — samen met een sterke toename van nucleair gecodeerde factoren voor mitochondriale translatie, wat suggereert dat de kern probeerde te compenseren voor falende mitochondriale eiwitproductie.
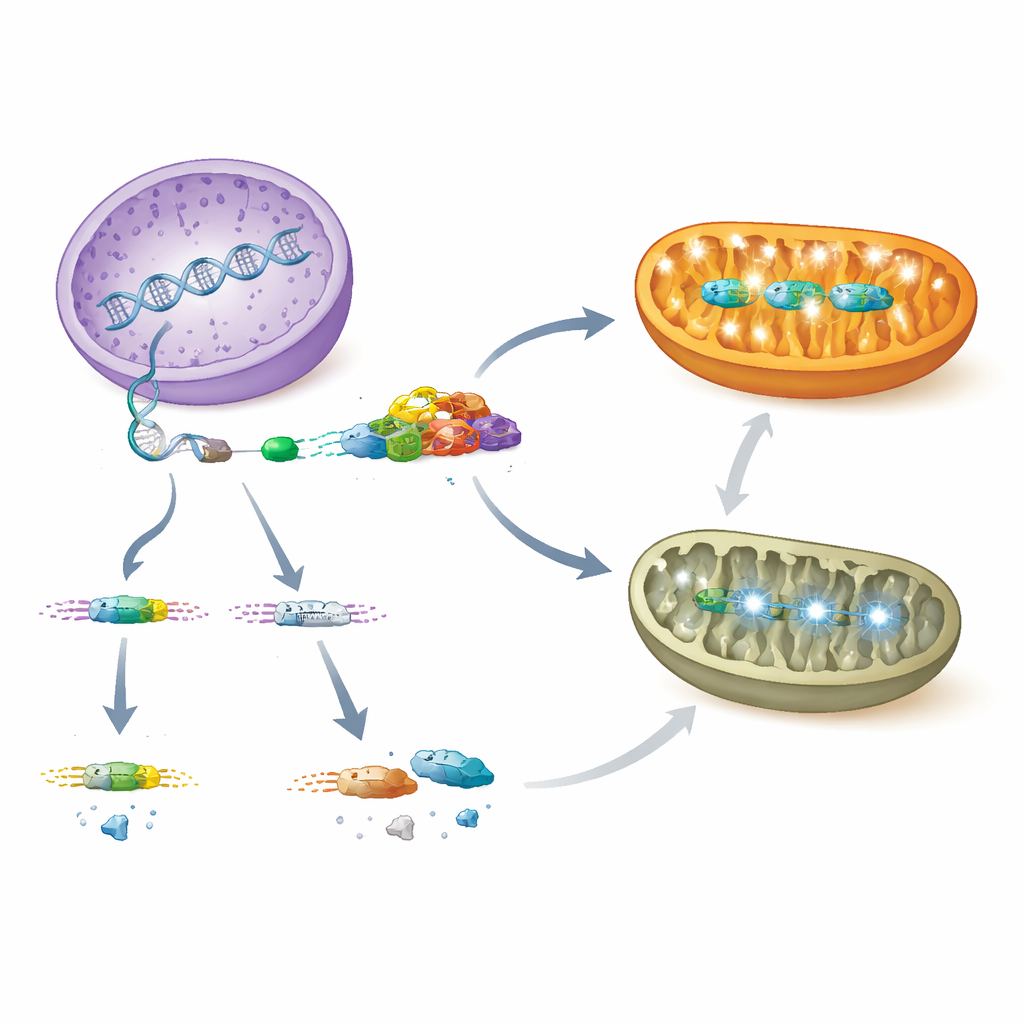
Wat dit betekent voor kinderen met zeldzaam hartfalen
Samen schetsen deze bevindingen een duidelijk pad van genregulatie naar orgaanaandoening. PCBP1 bindt normaal het AARS2‑RNA in hartcellen en zorgt dat exon 16 wordt opgenomen, wat een stabiel enzym produceert dat mitochondriale eiwitsynthese en robuuste energieproductie ondersteunt. Wanneer PCBP1 verloren gaat of wanneer mutaties deze splicingstap verstoren, wordt exon 16 overgeslagen, vallen AARS2‑niveaus in elkaar, vallen mitochondriale energiecomplexen uit elkaar en slagen de zich ontwikkelende hartwanden er niet in goed te compacten, wat leidt tot dodelijke cardiomyopathie. De gestreste mitochondriën geven vervolgens signalen terug aan de kern om beschermende programma’s te activeren, maar deze reacties zijn niet voldoende om hartfalen te voorkomen. Door deze PCBP1–AARS2‑as te belichten, suggereert de studie nieuwe diagnostische markers en potentiële therapeutische doelwitten voor zuigelingen en kinderen met anders onverklaarde mitochondriale hartaandoeningen.
Bronvermelding: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Trefwoorden: mitochondriale cardiomyopathie, RNA-splicing, aangeboren hartafwijking, AARS2-gen, mitochondriale stressrespons