Clear Sky Science · pt
PCBP1 regula o splicing alternativo de AARS2 na cardiomiopatia congênita
Por que alguns bebês nascem com corações que falham
Alguns lactentes desenvolvem uma forma grave de insuficiência cardíaca logo após o nascimento, causada não por artérias obstruídas, mas por pequenas falhas em como as células cardíacas produzem energia. Os médicos associaram essa condição a mutações em um gene chamado AARS2, porém os passos que ligam uma alteração no DNA a um coração fraco e mal formado permaneceram obscuros. Este estudo revela um elo crucial que faltava: um "editor" molecular que ajuda as células cardíacas a montar corretamente a mensagem de AARS2 para que suas mitocôndrias — as usinas de energia da célula — possam manter os corações batendo.
Um editor molecular que protege o coração em crescimento
Os autores se concentraram em PCBP1, uma proteína que se liga ao RNA, as mensagens intermediárias copiadas do DNA. Em corações de camundongos em desenvolvimento, eles encontraram o PCBP1 prendendo-se ao RNA de AARS2 próximo a uma junção crítica. AARS2 ajuda a carregar o aminoácido alanina em RNAs de transferência dentro das mitocôndrias, um passo-chave na construção das proteínas que impulsionam a produção de energia. Usando mapas de ligação de alto rendimento e construtos repórteres projetados, a equipe mostrou que os pontos de contato do PCBP1 coincidem com mutações humanas que perturbam a união de uma peça específica — o éxon 16 — da mensagem de AARS2. Quando o PCBP1 está ausente ou seus sítios de ligação são danificados, esse éxon é omitido, comprometendo as instruções para produzir uma enzima AARS2 de comprimento completo.
Quando a edição falha, a estrutura do coração se desorganiza
Para entender o impacto em um órgão inteiro, os pesquisadores removeram seletivamente o PCBP1 das células do músculo cardíaco de camundongos. Esses corações se desenvolveram de forma anormal: suas paredes ficaram finas e esponjosas em vez de densamente compactas, e a ponta do coração frequentemente se dividia em duas, uma malformação que lembra uma condição humana chamada não compactação ventricular esquerda. Muitos camundongos morreram pouco depois do nascimento. No nível do RNA, centenas de genes migraram para um padrão imaturo, típico de embriões iniciais, indicando atraso na maturação das câmaras cardíacas. Notavelmente, a mensagem de Aars2 quase sempre omitia o éxon 16, levando a um transcrito encurtado e a uma queda dramática da proteína AARS2, confirmando que o splicing defeituoso desse único gene é uma consequência importante da perda de PCBP1.
Danificar diretamente AARS2 recria a doença
Em seguida, a equipe engenheirou camundongos nos quais o éxon 16 de Aars2 poderia ser deletado apenas nas células do músculo cardíaco. Esses animais imitaram de perto os nocaute de PCBP1: apresentaram paredes ventriculares malformadas, morreram ao redor do nascimento e seus corações exibiram a mesma assinatura de expressão gênica imatura. Quando os pesquisadores provocaram a perda de Aars2 mais tarde na vida usando um segundo interruptor genético pós-natal, os animais inicialmente pareceram saudáveis, mas logo desenvolveram corações aumentados e enfraquecidos com extensa cicatrização. Microscopia eletrônica revelou que suas mitocôndrias tinham menos dobras internas, e ensaios bioquímicos detalhados mostraram que complexos chave da cadeia respiratória produtores de energia, especialmente os complexos I e IV, foram desestabilizados e perderam atividade muito antes do surgimento claro da insuficiência cardíaca.
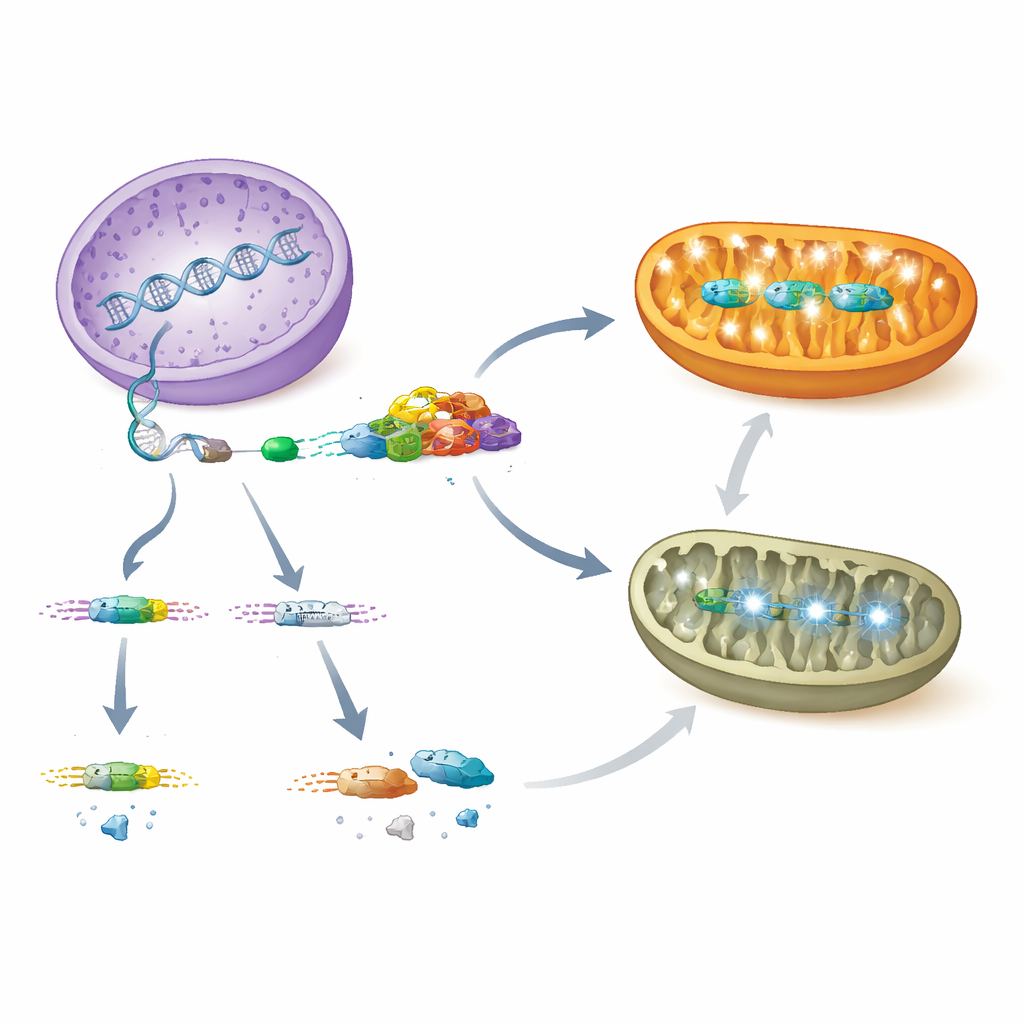
Como mitocôndrias em dificuldades se comunicam com o núcleo
A falha de AARS2 deixou as mitocôndrias das células cardíacas incapazes de manter a fosforilação oxidativa normal, a principal forma de gerar ATP. Tanto em corações deficientes em PCBP1 quanto em Aars2, muitos genes nucleares que codificam componentes da maquinaria energética foram reprimidos, e as proteínas mitocondriais correspondentes foram reduzidas. Ao mesmo tempo, as células ativaram um programa coordenado de estresse conhecido como resposta à proteína desnaturada e a resposta integrada ao estresse. Jogadores centrais dessa via, incluindo a proteína ATF4 e seu gatilho a montante, eIF2α fosforilado, aumentaram fortemente, assim como LONP1, uma protease mitocondrial que elimina proteínas danificadas. Em mutantes Aars2 mais velhos, os pesquisadores também observaram ativação do regulador de crescimento MYC e aumento do nucléolo — a fábrica de ribossomos — juntamente com um pico em fatores de tradução mitocondrial codificados pelo núcleo, sugerindo que o núcleo tentava compensar a falência da produção de proteínas mitocondriais.
O que isso significa para crianças com insuficiência cardíaca rara
Em conjunto, essas descobertas delineiam um caminho claro da regulação gênica à doença do órgão. O PCBP1 normalmente se liga ao RNA de AARS2 nas células cardíacas e assegura que o éxon 16 seja incluído, produzindo uma enzima estável que sustenta a síntese de proteínas mitocondriais e uma produção robusta de energia. Quando o PCBP1 é perdido ou quando mutações perturbam essa etapa de splicing, o éxon 16 é omitido, os níveis de AARS2 desabam, os complexos energéticos mitocondriais se desfazem e as paredes em desenvolvimento do coração deixam de compactar adequadamente, levando a uma cardiomiopatia letal. As mitocôndrias estressadas então sinalizam de volta ao núcleo para ativar programas de proteção, mas essas respostas não são suficientes para impedir a insuficiência cardíaca. Ao iluminar o eixo PCBP1–AARS2, o estudo sugere novos marcadores diagnósticos e potenciais alvos terapêuticos para lactentes e crianças com doença cardíaca mitocondrial de causa até então misteriosa.
Citação: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Palavras-chave: cardiomiopatia mitocondrial, splicing de RNA, doença cardíaca congênita, gene AARS2, resposta ao estresse mitocondrial