Clear Sky Science · he
PCBP1 מווסת את החלפת החיתוך של AARS2 בקרדיומיופתיה מולדת
מדוע תינוקות מסוימים נולדים עם לבים כושלים
בחלק מהתינוקות מתפתחת צורה קשה של אי־ספיקת לב זמן קצר לאחר הלידה, לא בגלל חסימות בעורקים אלא בגלל ליקויים זעירים באופן שבו תאי הלב שלהם מייצרים אנרגיה. רופאים קישורו מצב זה למוטציות בגן בשם AARS2, אך השלבים המקשרים בין שינוי ב‑DNA ללב חלש ומעוות נותרו מעורפלים. המחקר הזה חושף קישור חסר קריטי: "עורך" מולקולרי שעוזר לתאי הלב להרכיב נכון את המסר של AARS2 כדי שהמיטוכונדריות — תחנות הכוח של התא — יוכלו לשמור על פעילות הלב.
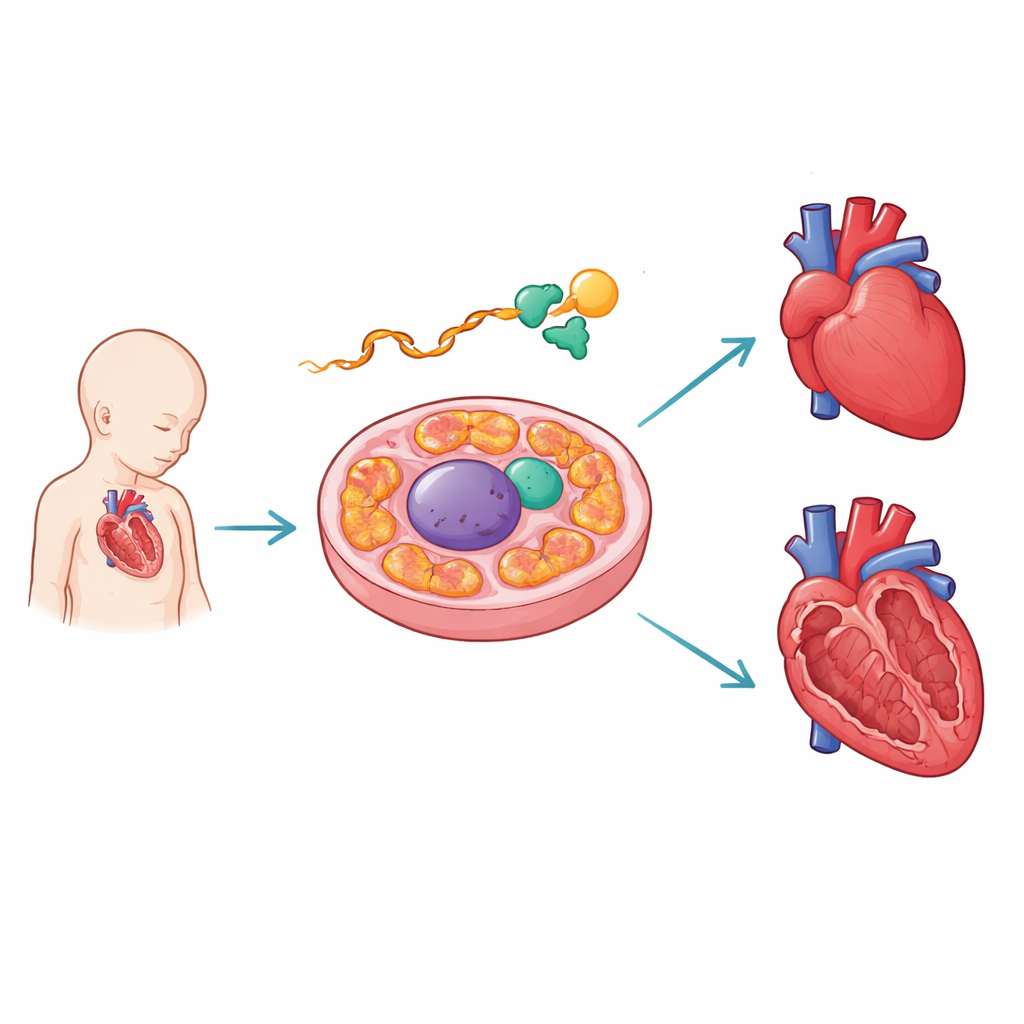
עורך מולקולרי שמגן על הלב המתפתח
המחברים התרכזו ב‑PCBP1, חלבון הקושר RNA — ההודעות הביניים המועתקות מה‑DNA. בלבבות עכברים בפיתוח הם מצאו את PCBP1 נקשר ל‑RNA של AARS2 בסמוך לצומת קריטי. AARS2 מסייע בעיגון חומצת האמינו אלנין ל‑tRNA בתוך המיטוכונדריה, שלב מרכזי בבניית החלבונים שמניעים את ייצור האנרגיה. באמצעות מיפויי קשירה ברזולוציה גבוהה ובניית דוחות ניסיוניים מהונדסים, הצוות הראה שנקודות המגע של PCBP1 מתיישבות עם מוטציות אנושיות שמפריעות לצירוף של מקטע מסוים — אקסון 16 — בהודעת AARS2. כאשר PCBP1 חסר או שאתרי הקשירה שלו פגועים, האקסון הזה מדולג, מה שמסיט את ההוראות ליצירת אנזים AARS2 באורך מלא.
כשעריכה נכשלה, מבנה הלב מתעוות
כדי להבין מה זה עושה לאיבר השלם, החוקרים הסירו באופן סלקטיבי את PCBP1 מתאי שריר הלב של עכברים. לבבות אלה התפתחו באופן לא תקין: דפנותיהם היו דקות וספוגיות במקום קומפקטיות בצפיפות, וקצות הלב לעתים קרובות נוצרו בשני חלקים — עיוות המזכיר מצב אנושי שנקרא אי‑קומפקטציה של החדר השמאלי. רבים מהעכברים מתו זמן קצר אחרי הלידה. ברמה של RNA, מאות גנים הראו דפוס צעיר יותר, שלבי התפתחות מוקדמים, שמעיד על עיכוב בבשלת חללי הלב. באופן בולט, ההודעה של Aars2 כמעט תמיד דילגה על אקסון 16, מה שהוביל לטרנסקריפט מקוצר ולירידה דרמטית בחלבון AARS2, ואישר שחיתוך לקוי של אותו גן יחיד הוא תוצאת לוואי מרכזית של אובדן PCBP1.
פגיעה ישירה ב‑AARS2 משחזרת את המחלה
בהמשך, הצוות הנדס עכברים שבהם ניתן היה למחוק את אקסון 16 של Aars2 רק בתאי שריר הלב. בעלי החיים הללו חיקו במדויק את הפגמים של חוסרי ה‑PCBP1: הם הראו דפנות חדריות מעוותות, מתו סביב זמן הלידה, ולבבותיהם הציגו את אותות הביטוי הגנטי הבלתי‑בשלים. כאשר החוקרים הופעלו מחיקה של Aars2 בשלב מאוחר יותר לאחר הלידה באמצעות מפסק גנטי משני, בעלי החיים הופיעו בתחילה בריאים אך במהרה פיתחו לבים מוגדלים וחלשים עם צלקת נרחבת. במיקרוסקופ אלקטרוני נראו מיטוכונדריות עם פחות קפלים פנימיים, ובבדיקות ביוכימיות מפורטות נראתה חוסר יציבות ואובדן פעילות במורכבים מרכזיים של שרשרת הנשימה, במיוחד במורכבים I ו‑IV, הרבה לפני הופעת אי‑ספיקת לב גלויה.
כיצד מיטוכונדריות במצוקה מתקשרות חזרה לגרעין
פירוק AARS2 השאיר את מיטוכונדריות תאי הלב שאינן מסוגלות לשמור על זרחון חמצוני תקין — הדרך העיקרית לייצור ATP. גם בלבבות חסרי PCBP1 וגם בלבבות חסרי Aars2, מספר גדול של גנים נומכרים בגרעין שמקודדים לרכיבי מכונת האנרגיה הופעלו פחות, והחלבונים המיטוכונדריאליים האמיתיים שהם מייצרים נדלדלו. במקביל, התאים הפעילו תוכנית מצוקה מתואמת הידועה כתגובה לפרוטאינים מקופלים לא נכונה וכתגובה משולבת ללחץ. שחקנים מרכזיים בדרך זו, כולל החלבון ATF4 וגורם ההדק שלו מעלה, eIF2α מזורחן, עלו בחדות, כמו גם LONP1, פרוטאז מיטוכונדריאלי שמנקה חלבונים פגומים. בעכברי Aars2 מבוגרים יותר ראו החוקרים גם הפעלת רגולטור הגדילה MYC והגדלה של הגרעינון — מפעל לייצור ריבוזומים — יחד עם גל של גורמי תרגום מיטוכונדריאליים המקודדים בגרעין, מה שנראה כהתאמצות הגרעין לפצות על כישלון ייצור החלבונים במיטוכונדריה.
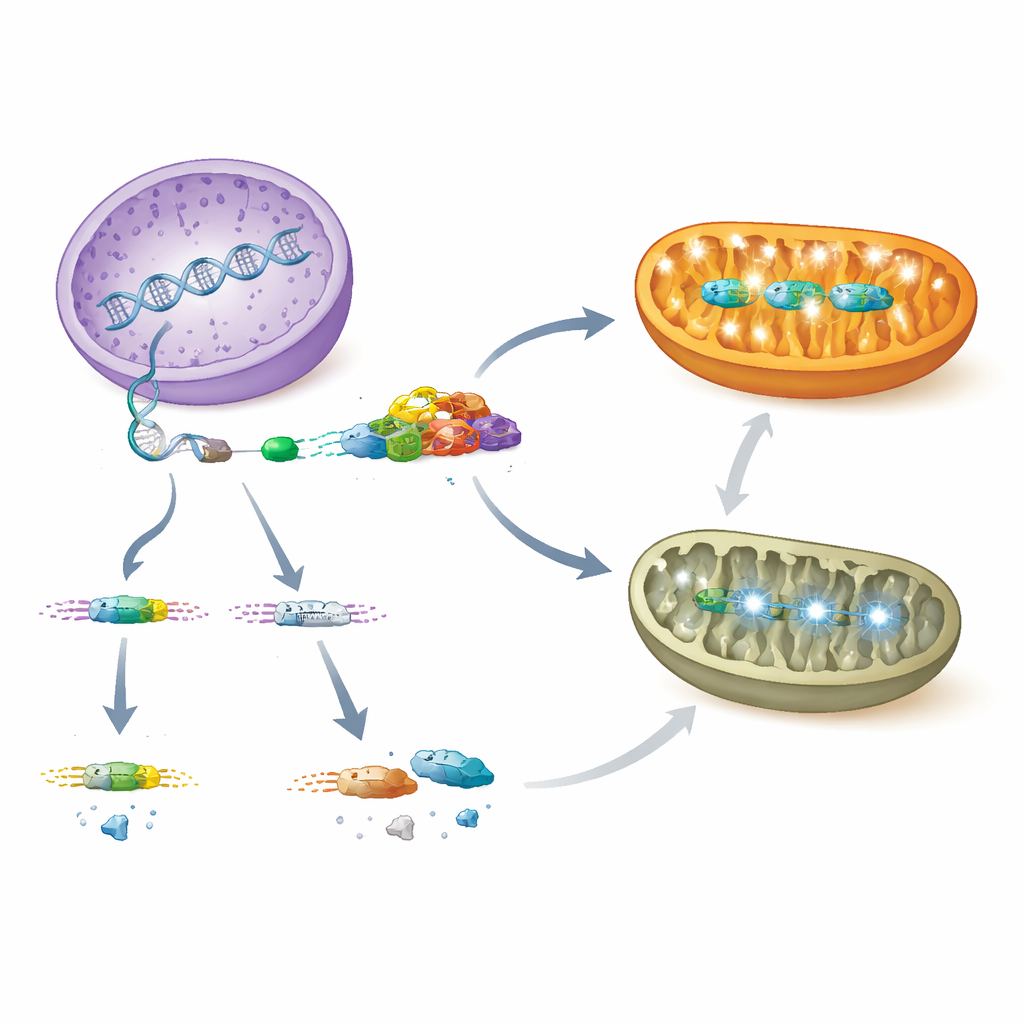
מה משמעות זה עבור ילדים עם אי‑ספיקת לב נדירה
ביחד, ממצאים אלה מסמנים מסלול ברור מהרגולציה הגנטית עד למחלת האיבר. PCBP1 כרגיל נקשר ל‑RNA של AARS2 בתאי הלב ומוודא שאקסון 16 ייכלל, מה שמייצר אנזים יציב התומך בתרגום חלבונים מיטוכונדריאליים ובפלט אנרגיה חזק. כאשר PCBP1 אובד או שמוטציות משבשות את שלב החיתוך הזה, אקסון 16 נדחה, רמות AARS2 קרסות, קומפלקסי האנרגיה במיטוכונדריה מתפרקים ודפנות הלב המתפתח נכשלות להיות קומפקטיות כראוי, מה שמוביל לקרדיומיופתיה קטלנית. המיטוכונדריות הנמצאות במתח משדרות אחר־כך חזרה לגרעין להפעיל תוכניות הגנה, אך תגובות אלה אינן מספיקות למנוע אי‑ספיקת לב. בהדגשת ציר PCBP1–AARS2, המחקר מציע סמנים אבחוניים חדשים ומטרות טיפול אפשריות לתינוקות וילדים עם מחלת לב מיטוכונדריאלית מסתורית אחרת.
ציטוט: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
מילות מפתח: קרדיומיופתיה מיטוכונדריאלית, חיתוך RNA, מחלות לב מולדות, גן AARS2, תגובה ללחץ מיטוכונדריאלי