Clear Sky Science · ar
PCBP1 ينظم اللُّصق البديل لجين AARS2 في اعتلال القلب الخلقي
لماذا يولد بعض الأطفال بقلوبٍ مُقصِرة
يصاب بعض الرضّع بصورة شديدة من فشل القلب بعد الولادة مباشرة، ناجمة ليس عن انسداد الشرايين بل عن عيوب دقيقة في طريقة إنتاج خلايا القلب للطاقة. ربط الأطباء هذه الحالة بطفَرات في جين يُدعى AARS2، ومع ذلك بقيت الخطوات التي تصل بين تغيير الحمض النووي وقلب ضعيف ضعيف التكوّن غامضة. تكشف هذه الدراسة حلقة مفقودة حاسمة: «مُحرِّر» جزيئي يساعد خلايا القلب على تجميع رسالة AARS2 بشكل صحيح لكي تستمر الميتوكوندريا — محطات طاقة الخلية — في إبقاء القلب نابضاً.
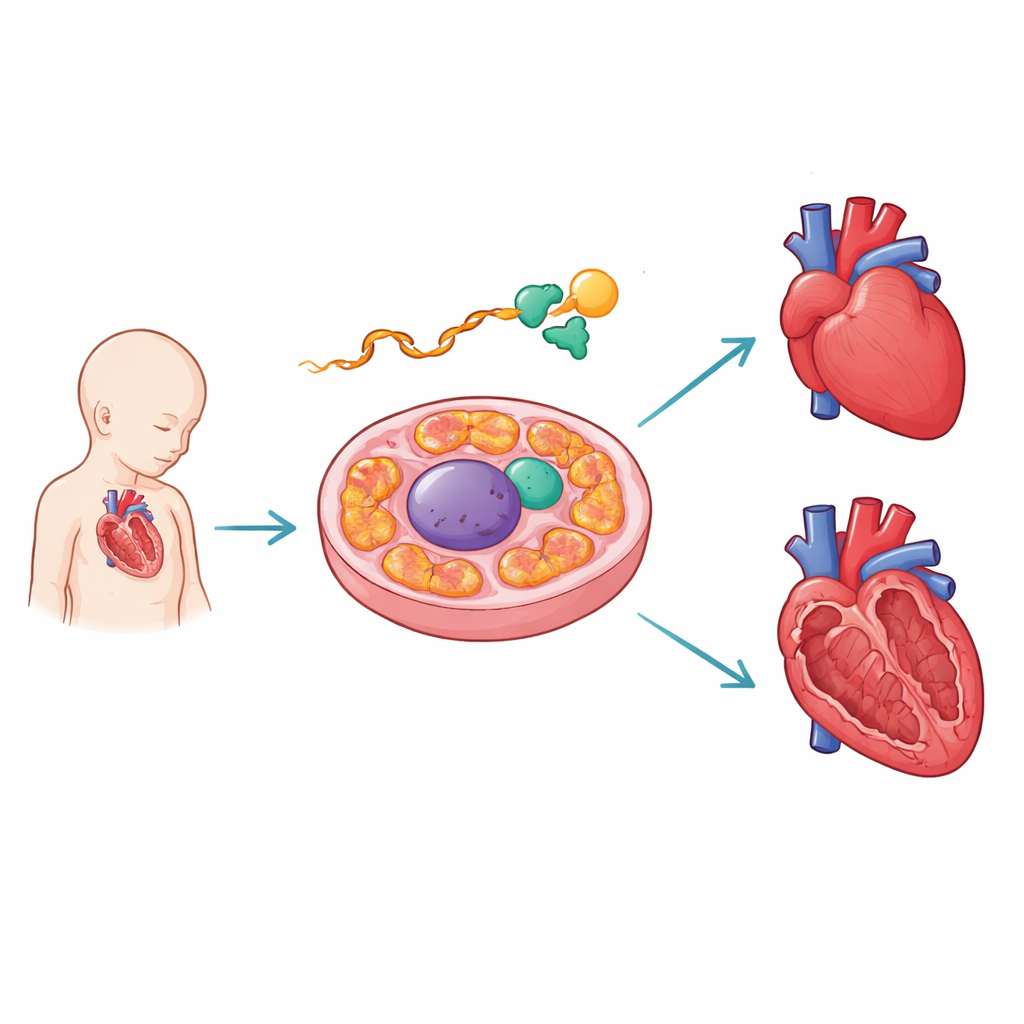
محرِّر جزيئي يحمي القلب النامي
ركّز الباحثون على PCBP1، بروتين يربط الحمض النووي الريبي، الرسائل الوسيطة المنسوخة من الحمض النووي. في قلوب الفئران النامية، وجدوا PCBP1 يلتصق برنا AARS2 بالقرب من مفصل حاسم. يساعد AARS2 على تحميل الحمض الأميني ألانين على الرنا الناقل داخل الميتوكوندريا، وهي خطوة رئيسية في تركيب البروتينات المسؤولة عن إنتاج الطاقة. باستخدام خرائط ارتباط عالية الإنتاجية ومرَكبات مراسلة مصممة، أظهر الفريق أن نقاط اتصال PCBP1 تتزامن مع طفرات بشرية تُعطِّل ضم قطعة واحدة محددة — المقطع 16 (الإكسون 16) — من رسالة AARS2. عند غياب PCBP1 أو تلف مواقع ارتباطه، يتم تجاوز هذا الإكسون، مما يعطل التعليمات لصنع إنزيم AARS2 بكامل طوله.
عندما يفشل التحرير، يتشوّه بنية القلب
لمعرفة تأثير ذلك على عضوٍ كامل، أزال الباحثون PCBP1 انتقائياً من خلايا عضلة قلب الفأر. تطورت هذه القلوب بشكل غير طبيعي: جدرانها كانت رقيقة ومخاطية بدلاً من مدمجة بكثافة، وغالباً ما انقسم طرف القلب إلى جزأين، تشوه يشبه حالة بشرية تُسمى ضعف تكون البطين الأيسر غير المضغوط. مات العديد من الفئران في وقتٍ قريب بعد الولادة. على مستوى الرنا، انحرفت مئات الجينات إلى نمط جنيني مبكّر وغير ناضج، ما يدل على تأخر نضج حجرات القلب. ولاحظ الباحثون أن رسالة Aars2 كانت تتجاوز الإكسون 16 في الغالب، مما يؤدي إلى نسخة مختصرة من المراسلة وانخفاض دراماتيكي في بروتين AARS2، مما يؤكد أن لُصق هذا الجين المفرد بشكل خاطئ هو نتيجة رئيسية لفقدان PCBP1.
إصابة AARS2 مباشرة تعيد إنتاج المرض
بعد ذلك، صمّم الفريق فئراناً يمكن فيها حذف الإكسون 16 من Aars2 فقط في خلايا عضلة القلب. حاكت هذه الحيوانات نموذج إزالة PCBP1 عن كثب: أظهرت جدران بطينية مشوهة، وماتت حول وقت الولادة، وبرزت في قلوبها نفس بصمة التعبير الجيني غير الناضج. عندما حفّز الباحثون فقدان Aars2 لاحقاً في الحياة باستخدام مفتاح جيني ما بعد الولادة، بدا الحيوان سليماً في البداية لكنه سرعان ما طور قلوباً متضخمة ومضعفة مع تندب واسع. كشفت المجهرية الإلكترونية أن ميتوكوندرياته كان بها طيات داخلية أقل، وأظهرت التحليلات الكيميائية الحيوية أن مجمعات توليد الطاقة في سلسلة التنفّس، وخصوصاً المجمعان I وIV، أصبحت غير مستقرة وفقدت نشاطها قبل ظهور فشل القلب الصريح بفترة.
كيف تُرسل الميتوكوندريا المتعثرة إشارات إلى النواة
أدى انهيار AARS2 إلى عجز ميتوكوندريا خلايا القلب عن المحافظة على الفسفرة التأكسدية الطبيعية، الوسيلة الرئيسية لتوليد الأدينوسين ثلاثي الفوسفات (ATP). في القلوب التي تفتقر إلى PCBP1 أو Aars2، انخفض تعبير العديد من الجينات النووية المشفرة لمكوّنات آليات الطاقة، ونفدت البروتينات الميتوكوندرية الفعلية التي تُنتج. في الوقت نفسه، نشّطت الخلايا برنامج إجهاد منسق يعرف باستجابة البروتين غير المطوي والاستجابة المتكاملة للإجهاد. ارتفعت عوامل محورية في هذا المسار، بما في ذلك البروتين ATF4 ومحفزه الأعلى فسفرة eIF2α، وكذلك LONP1، وهو بروتياز ميتوكوندري يزيل البروتينات المتضررة. في طفرات Aars2 الأكبر سناً، لاحظ الباحثون أيضاً تنشيط منظم النمو MYC وتكبّر النوية — مصنع تركيب الريبوسومات — مع زيادة في عوامل الترجمة الميتوكوندرية المشفرة نووياً، ما يشير إلى أن النواة كانت تحاول التعويض عن فشل إنتاج البروتين في الميتوكوندريا.
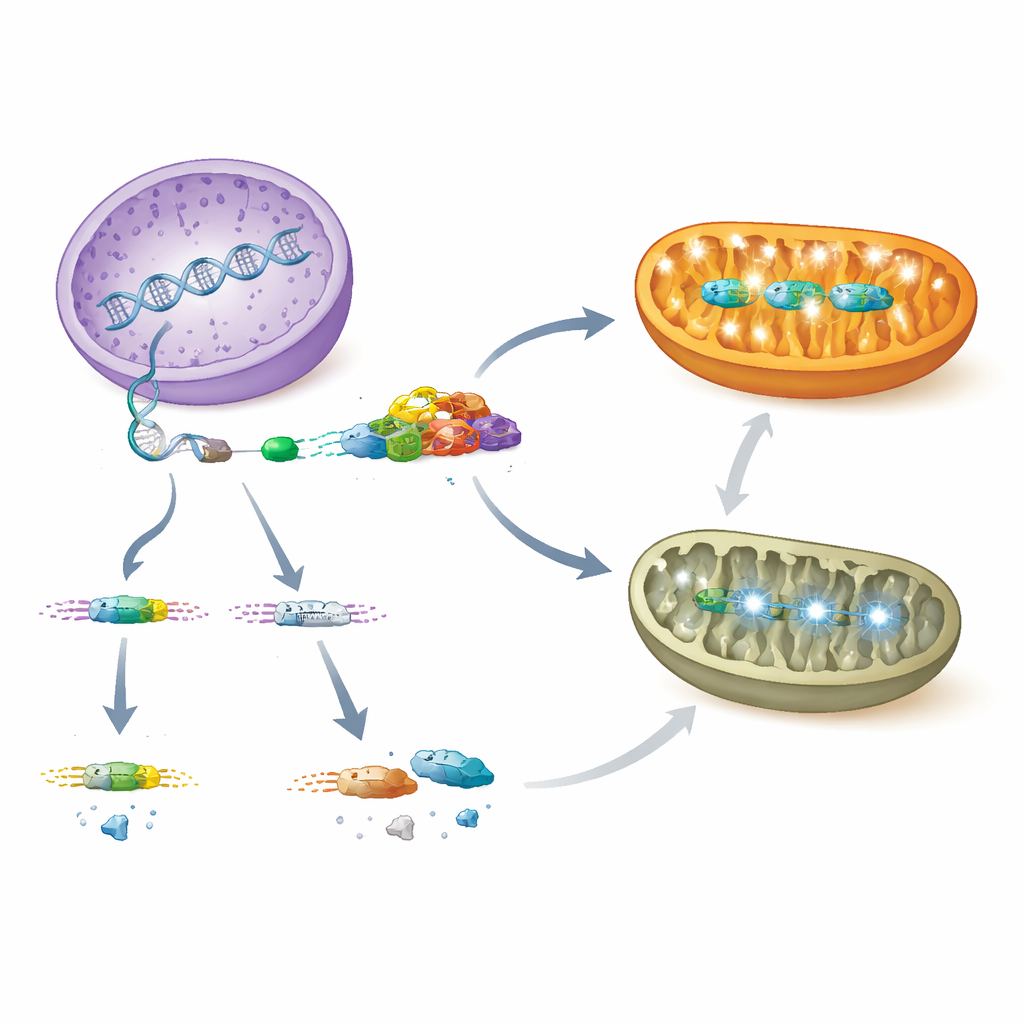
ما يعنيه هذا للأطفال المصابين بفشل قلبي نادر
تحدد هذه النتائج مساراً واضحاً من تنظيم الجينات إلى مرض العضو. يربط PCBP1 عادة رنا AARS2 في خلايا القلب ويضمن إدماج الإكسون 16، مما ينتج إنزيماً مستقراً يدعم تخليق البروتينات الميتوكوندرية وإنتاج الطاقة القوي. عندما يُفقد PCBP1 أو تُعيق الطفرات هذه الخطوة اللُصقية، يُتجاوز الإكسون 16، تنهار مستويات AARS2، تفكك مجمعات الطاقة الميتوكوندرية وتفشل جدران القلب النامية في التكاثف بشكلٍ صحيح، مما يؤدي إلى اعتلال قلبي مميت. تُرسل الميتوكوندريا المتوترة بعد ذلك إشارات إلى النواة لتنشيط برامج وقائية، لكن هذه الاستجابات لا تكفي لمنع فشل القلب. من خلال إظهار محور PCBP1–AARS2 هذا، تقترح الدراسة مؤشرات تشخيصية جديدة وأهداف علاجية محتملة للرضع والأطفال المصابين باعتلال قلبي ميتوكوندري غامض في أصله.
الاستشهاد: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
الكلمات المفتاحية: اعتلال القلب الميتوكوندري, لُصق الحمض النووي الريبي, أمراض القلب الخلقية, جين AARS2, استجابة الإجهاد الميتوكوندرية