Clear Sky Science · ja
PCBP1は先天性心筋症におけるAARS2の選択的スプライシングを制御する
なぜ一部の乳児は心不全を抱えて生まれるのか
一部の新生児は、生後まもなく深刻な心不全を発症しますが、その原因は動脈の閉塞ではなく、心筋細胞がエネルギーを作る過程に生じた微細な異常にあります。医師たちはこの状態をAARS2と呼ばれる遺伝子の変異と関連づけてきましたが、DNAの変化が虚弱でうまく形成されない心臓へと至る過程は不明瞭なままでした。本研究は重要な欠落していた一連のつながりを明らかにします:心筋細胞がミトコンドリア(細胞の発電所)を維持して拍動を保つために、AARS2メッセージを正しく組み立てることを助ける分子上の“編集者”です。
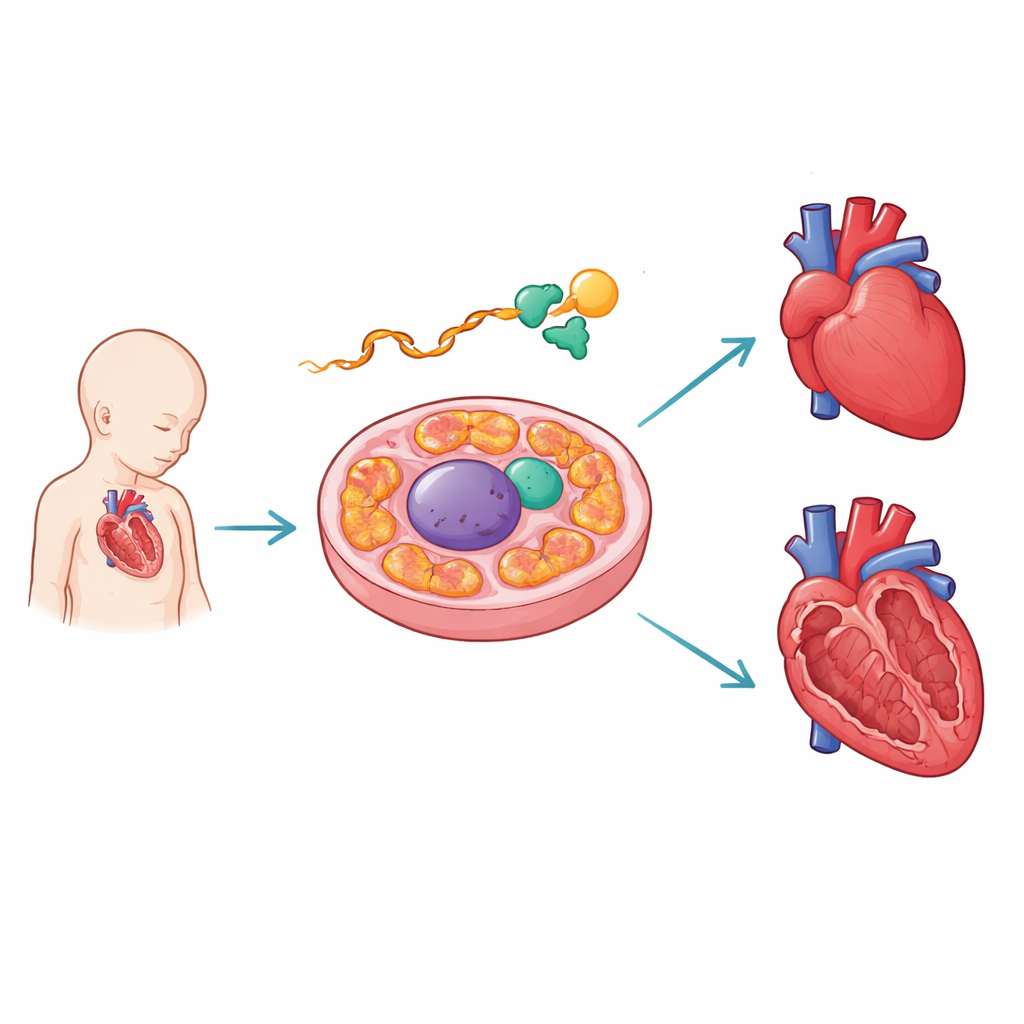
成長する心臓を守る分子編集者
著者らはRNAに結合するタンパク質PCBP1に着目しました。発生中のマウス心臓では、PCBP1がAARS2のRNAの重要な接合部付近に結合していることが見つかりました。AARS2はミトコンドリア内でアミノ酸アラニンをトランスファーRNAに結び付ける役割を担い、エネルギー産生に必要なタンパク質を作る上で重要なステップです。ハイスループットの結合マップや設計したリポーター構築体を用いて、チームはPCBP1の結合点がヒトの病的変異と一致し、それがAARS2メッセージの特定の断片—エクソン16—の接合を乱すことを示しました。PCBP1が欠損するかその結合部位が損なわれると、このエクソンはスキップされ、全長のAARS2酵素を作る指示が脱線します。
編集が失敗すると心臓の構造が乱れる
臓器全体にとってこれが何を意味するかを調べるために、研究者らはマウスの心筋細胞から選択的にPCBP1を除去しました。これらの心臓は異常に発達しました:心壁は密にコンパクトする代わりに薄くスポンジ状で、心尖部が二つに裂けることが多く、人間の左室非コンパクションに類似した奇形を示しました。多くのマウスは生後まもなく死亡しました。RNAレベルでは数百の遺伝子が未熟で初期胚様の発現パターンへとシフトし、心室の成熟が遅れていることを示しました。特にAars2のメッセージはほとんど常にエクソン16をスキップし、短縮された転写産物とAARS2タンパク質の劇的な減少を招き、単一遺伝子のスプライシング不良がPCBP1喪失の主要な結果であることを確証しました。
AARS2を直接損なうと病態が再現される
次にチームは、Aars2のエクソン16を心筋細胞限定で削除できるように遺伝子改変マウスを作製しました。これらの動物はPCBP1ノックアウトとよく似た症状を示しました:心室壁の奇形、出生前後の致死、そして同じような未熟な遺伝子発現シグネチャーが観察されました。研究者らが出生後の第二の遺伝学的スイッチでAars2欠失を後期に誘導した場合、初めは健康に見えたものの、やがて拡大し弱った心臓と広範な瘢痕化を発症しました。電子顕微鏡ではミトコンドリア内部のひだが減少しており、詳細な生化学的解析は呼吸鎖の主要なエネルギー産生複合体、特に複合体IおよびIVが不安定化して活性を失い、明確な心不全が現れるずっと前から機能低下が起きていることを示しました。
機能不全のミトコンドリアは核へどう信号を送るか
AARS2の破綻により、心筋細胞のミトコンドリアは通常の酸化的リン酸化を維持できなくなり、ATP生成が障害されました。PCBP1欠損心とAars2欠損心の両方で、エネルギー機構を構成する多くの核遺伝子の発現が抑えられ、それに対応するミトコンドリアタンパク質も枯渇していました。同時に、細胞は折り畳み不良タンパク質応答(UPR)や統合ストレス応答(ISR)として知られる協調的なストレスプログラムを起動しました。この経路の中心選手である転写因子ATF4やその上流のトリガーであるリン酸化されたeIF2αが急増し、損傷タンパク質を除去するミトコンドリアプロテアーゼLONP1も上昇しました。年長のAars2変異体では成長調節因子MYCの活性化やリボソームを作る工場である核小体の肥大、さらに核コードのミトコンドリア翻訳因子の急増も観察され、核が失敗したミトコンドリアのタンパク質合成を補おうとしていることが示唆されました。
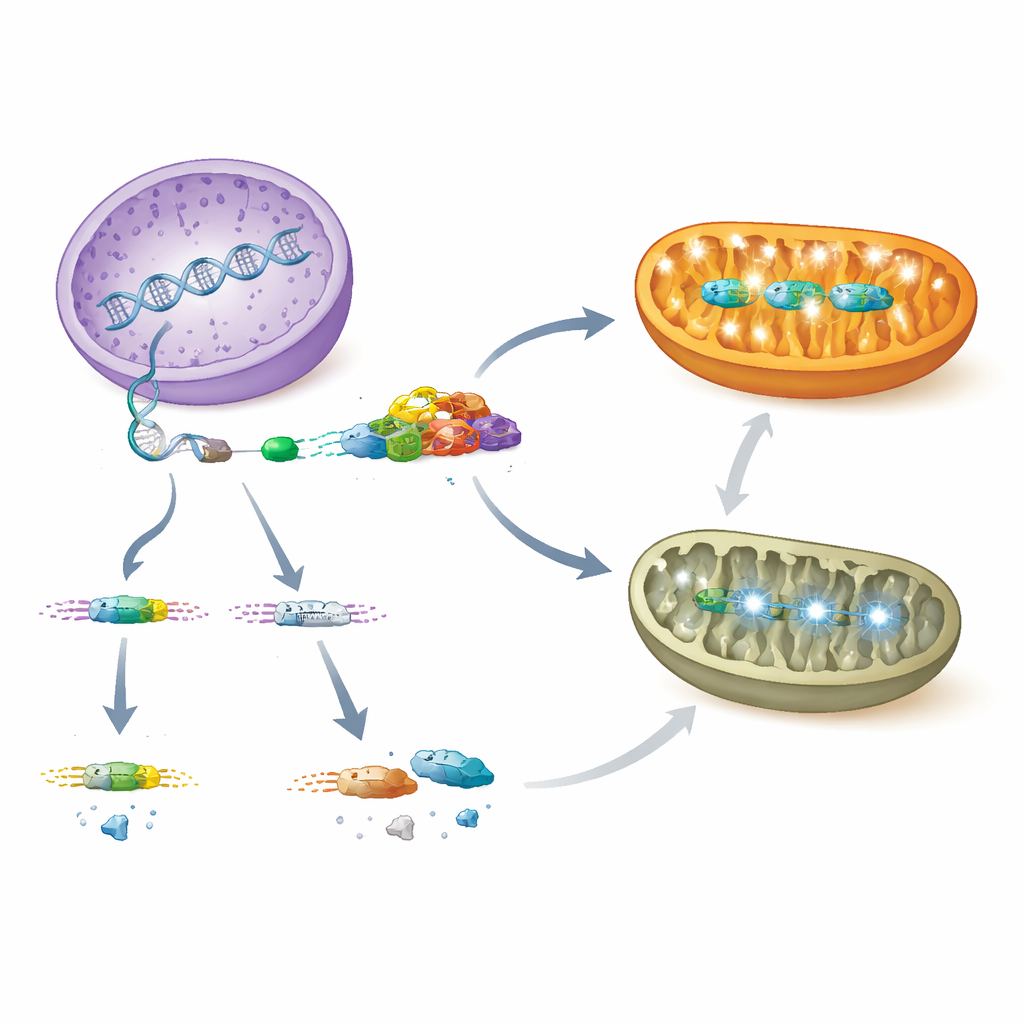
希少な小児心不全への意味
総じて、これらの知見は遺伝子制御から臓器疾患へ至る明瞭な経路を描きます。PCBP1は通常、心筋細胞においてAARS2のRNAに結合し、エクソン16の包含を確保して安定な酵素を産生し、ミトコンドリアのタンパク質合成と十分なエネルギー産生を支えます。PCBP1が失われるか、このスプライシング段階を乱す変異が起きると、エクソン16はスキップされ、AARS2レベルが崩壊し、ミトコンドリアのエネルギー複合体が崩れ、発生中の心壁が正常にコンパクト化できず致死的な心筋症を引き起こします。ストレスを受けたミトコンドリアは核へ逆に信号を送り保護プログラムを活性化しますが、これらの応答だけでは心不全を防ぐには不十分です。PCBP1–AARS2軸を明らかにしたことで、これまで謎であった乳児・小児のミトコンドリア性心疾患に対する新たな診断マーカーや治療標的の可能性が示唆されます。
引用: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
キーワード: ミトコンドリア性心筋症, RNAスプライシング, 先天性心疾患, AARS2遺伝子, ミトコンドリアストレス応答