Clear Sky Science · tr
PCBP1, doğuştan gelen kardiyomiyopatide AARS2'nin alternatif ekson bağlanmasını düzenliyor
Neden bazı bebekler kalp yetmezliğiyle doğar
Bazı bebekler doğumdan kısa süre sonra şiddetli kalp yetmezliği geliştirir; bunun nedeni damar tıkanıklığı değil, kalp hücrelerinin enerji üretiminde küçük hatalardır. Doktorlar bu durumu AARS2 adlı gendeki mutasyonlarla ilişkilendirmişti, ancak bir DNA değişikliğinin zayıf, düzgün gelişmemiş bir kalbe nasıl yol açtığı belirsiz kalmıştı. Bu çalışma kritik bir bağlantıyı ortaya koyuyor: kalp hücrelerinin AARS2 mesajını doğru şekilde bir araya getirmesine yardımcı olan moleküler bir “düzenleyici”, böylece mitokondriler—hücrenin enerji santralleri—çarpan kalpleri canlı tutabiliyor.
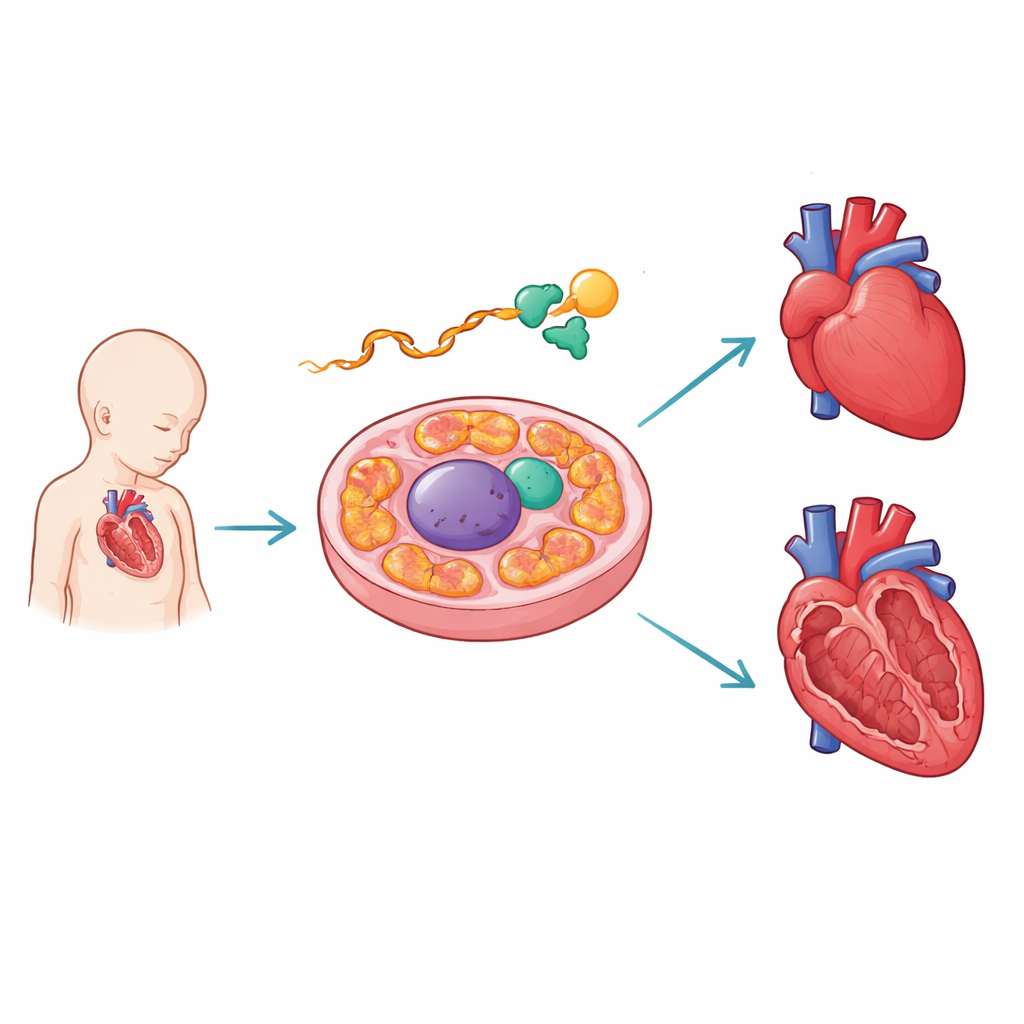
Büyüyen kalbi koruyan moleküler bir editör
Yazarlar, DNA'dan kopyalanan ara mesaj olan RNA'ya bağlanan bir protein olan PCBP1'e odaklandı. Gelişen fare kalplerinde PCBP1'in kritik bir kavşağın yakınında AARS2 RNA'sına tutunduğunu buldular. AARS2, mitokondriler içinde alanin amino asidini taşıyıcı RNA'lara yüklemeye yardımcı olur; bu, enerji üreten proteinlerin sentezinde kilit bir adımdır. Yüksek verimli bağlanma haritaları ve tasarlanmış raporlayıcı yapılar kullanarak ekip, PCBP1'in temas noktalarının insan hastalığı mutasyonlarıyla çakıştığını ve bunların AARS2 mesajının belirli bir parçası—ekzon 16—birleşimini bozduğunu gösterdi. PCBP1 eksik olduğunda veya bağlanma bölgeleri zarar gördüğünde bu ekzon atlanıyor ve tam uzunlukta AARS2 enzimi üretimi için talimatlar aksıyor.
Düzenleme başarısız olunca kalp yapısı bozuluyor
Bunun bütün bir organa ne anlama geldiğini görmek için araştırmacılar PCBP1'i seçici olarak fare kalp kası hücrelerinden çıkardı. Bu kalpler anormal gelişti: duvarları yoğun kompakt yerine ince ve süngerimsiydi ve kalbin ucu sıklıkla ikiye ayrılarak insanlardaki sol ventriküler non-kompaktasyon adı verilen duruma benzer bir malformasyona yol açtı. Birçok fare doğumdan kısa süre sonra öldü. RNA düzeyinde yüzlerce gen olgunlaşmamış, erken embriyo desenine kaydı; bu da kalp odacıklarının olgunlaşmasının geciktiğini gösteriyordu. Özellikle Aars2 mesajı neredeyse her zaman ekzon 16'yı atlıyordu; bunun sonucunda kısalmış bir transkript ve AARS2 proteininde dramatik bir düşüş gözlendi; bu da tek bir genin hatalı bağlanmasının PCBP1 kaybının önemli bir sonucu olduğunu doğruladı.
AARS2'yi doğrudan hasarlamak hastalığı yeniden yaratıyor
Sırada, araştırmacılar Aars2'nin ekzon 16'sının yalnızca kalp kası hücrelerinde silinebildiği fareler üretti. Bu hayvanlar PCBP1 yokluklarını yakından taklit etti: ventriküler duvarlarda malformasyon, doğum civarında ölüm ve aynı olgunlaşmamış gen ifadesi imzası görüldü. Araştırmacılar Aars2 kaybını yaşamın daha ileri döneminde, doğum sonrası bir genetik anahtar kullanarak tetiklediklerinde hayvanlar başlangıçta sağlıklı görünse de kısa süre içinde genişlemiş, zayıflamış ve yaygın skar dokusu içeren kalpler geliştirdiler. Elektron mikroskobu mitokondrilerinin iç kıvrımlarının azaldığını gösterdi ve ayrıntılı biyokimyasal testler solunum zincirindeki özellikle I ve IV kompleksleri olmak üzere ana enerji üreten komplekslerin kararsızlaştığını ve belirgin kalp yetmezliği ortaya çıkmadan çok önce aktivite kaybettiklerini ortaya koydu.
Mücadele eden mitokondriler çekirdeğe nasıl sinyal gönderir
AARS2'nin bozulması, kalp hücresi mitokondrilerinin normal oksidatif fosforilasyonu sürdürmesini engelledi; bu, ATP üretiminin ana yoludur. Hem PCBP1 eksik hem de Aars2 eksik kalplerde, enerji makinası bileşenlerini kodlayan birçok nükleer gen aşağı doğru düzenlendi ve bu genlerin ürettiği gerçek mitokondriyal proteinler tükenmişti. Aynı zamanda hücreler, katlanmamış protein yanıtı ve entegre stres yanıtı olarak bilinen koordine bir stres programını açtı. Bu yolun merkezi oyuncuları olan ATF4 protein ve upstream tetikleyicisi fosforile eIF2α keskin şekilde arttı; hasarlı proteinleri temizleyen mitokondriyal proteaz LONP1 de yükseldi. Daha yaşlı Aars2 mutantlarında araştırmacılar ayrıca büyüme düzenleyicisi MYC'in aktivasyonunu ve ribozom fabrikası olan nükleolüsün büyümesini, ayrıca nükleer kaynaklı mitokondriyal transkripsiyon faktörlerinde bir artışı gördüler; bu da çekirdeğin başarısız mitokondriyal protein üretimini telafi etmeye çalıştığını düşündürüyor.
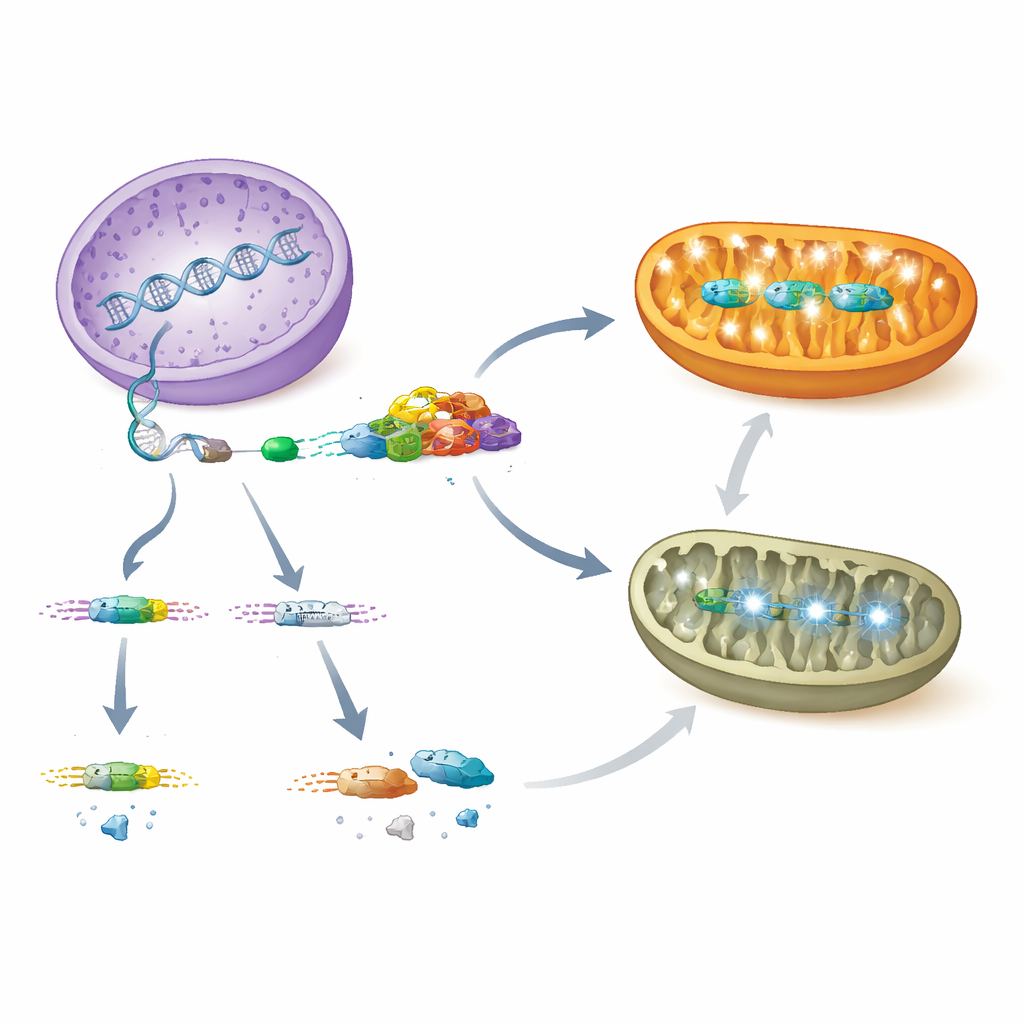
Nadir kalp yetmezliği olan çocuklar için bunun anlamı
Bu bulgular bir gen regülasyonundan organ hastalığına net bir yol haritası çiziyor. PCBP1 normalde kalp hücrelerinde AARS2 RNA'sına bağlanır ve ekzon 16'nın dahil edilmesini sağlar; böylece mitokondriyal protein sentezini ve güçlü enerji üretimini destekleyen stabil bir enzim üretilir. PCBP1 kaybolduğunda veya mutasyonlar bu ekson bağlanma adımını bozduğunda ekzon 16 atlanır, AARS2 seviyeleri çöker, mitokondriyal enerji kompleksleri parçalanır ve gelişen kalp duvarları uygun şekilde kompakte olamaz; bu da ölümcül kardiyomiyopatiye yol açar. Stres altındaki mitokondriler daha sonra koruyucu programları aktive etmek için çekirdeğe sinyal gönderir, ancak bu yanıtlar kalp yetmezliğini önlemeye yetmez. PCBP1–AARS2 eksenini aydınlatarak çalışma, gizemli mitokondriyal kalp hastalığı olan bebekler ve çocuklar için yeni tanısal belirteçler ve potansiyel tedavi hedefleri önermektedir.
Atıf: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Anahtar kelimeler: mitokondriyal kardiyomiyopati, RNA ekson bağlanması, doğuştan kalp hastalığı, AARS2 geni, mitokondriyal stres yanıtı