Clear Sky Science · fr
PCBP1 régule l'épissage alternatif de AARS2 dans la cardiomyopathie congénitale
Pourquoi certains bébés naissent avec un cœur défaillant
Certains nourrissons développent peu après la naissance une forme sévère d’insuffisance cardiaque due non pas à des artères bouchées mais à de petites défaillances dans la façon dont les cellules cardiaques produisent de l’énergie. Les cliniciens ont relié cette maladie à des mutations du gène AARS2, mais les étapes reliant une altération de l’ADN à un cœur faible et mal formé sont restées opaques. Cette étude met au jour un maillon essentiel manquant : un « éditeur » moléculaire qui aide les cellules cardiaques à assembler correctement le message d’AARS2 afin que leurs mitochondries — les centrales énergétiques de la cellule — puissent maintenir le muscle cardiaque en activité.
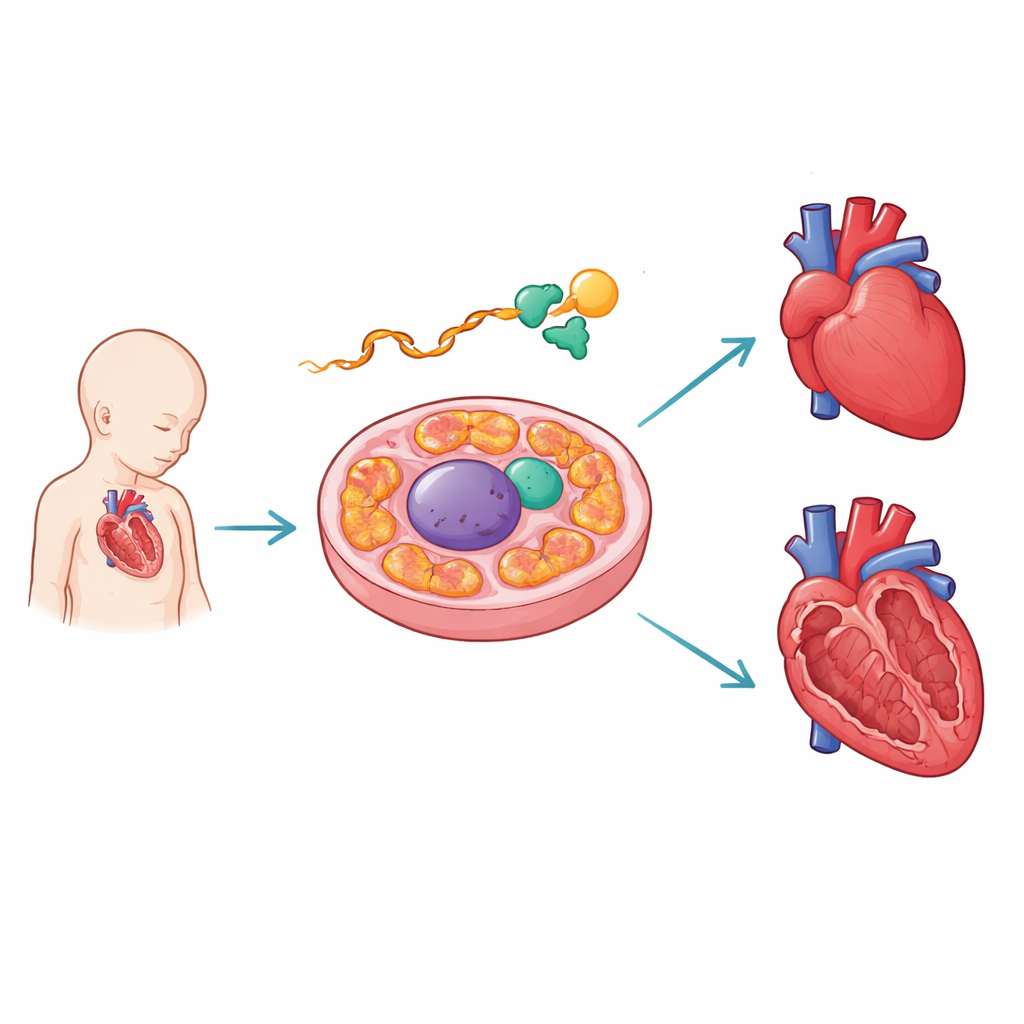
Un éditeur moléculaire qui protège le cœur en formation
Les auteurs se sont intéressés à PCBP1, une protéine qui se lie à l’ARN, ces messages intermédiaires copiés à partir de l’ADN. Dans des cœurs de souris en développement, ils ont observé PCBP1 se fixer sur l’ARN d’AARS2 à proximité d’une jonction critique. AARS2 aide à charger l’acide aminé alanine sur les ARN de transfert à l’intérieur des mitochondries, une étape clé pour fabriquer les protéines qui assurent la production d’énergie. À l’aide de cartographies de liaison à haut débit et de réporteurs conçus, l’équipe a montré que les points de contact de PCBP1 coïncident avec des mutations humaines responsables de la perturbation de l’assemblage d’un segment particulier — l’exon 16 — du message d’AARS2. Lorsque PCBP1 manque ou que ses sites de liaison sont endommagés, cet exon est omis, compromettant les instructions pour produire une enzyme AARS2 en longueur complète.
Quand l’édition échoue, la structure du cœur déraille
Pour évaluer l’impact au niveau de l’organe, les chercheurs ont supprimé sélectivement PCBP1 des cellules musculaires cardiaques de souris. Ces cœurs se sont développés de façon anormale : leurs parois étaient fines et spongieuses au lieu d’être compactes, et la pointe du cœur se scindait souvent en deux, une malformation rappelant la non-compaction ventriculaire gauche chez l’humain. De nombreux animaux sont morts peu après la naissance. Au niveau de l’ARN, des centaines de gènes ont basculé vers un profil immature, typique d’un stade embryonnaire précoce, indiquant un retard de maturation des cavités cardiaques. De manière notable, le message Aars2 omettait presque systématiquement l’exon 16, conduisant à un transcrit raccourci et à une chute dramatique de la protéine AARS2, confirmant que le mauvais épissage de ce seul gène est une conséquence majeure de la perte de PCBP1.
Endommager directement AARS2 recrée la maladie
Puis, l’équipe a génétiquement modifié des souris afin que l’exon 16 d’Aars2 puisse être supprimé uniquement dans les cellules musculaires cardiaques. Ces animaux ont fortement reproduit le phénotype des suppressions de PCBP1 : parois ventriculaires mal formées, mortalité périnatale et signature d’expression génique immature dans le cœur. Lorsque les chercheurs ont déclenché la perte d’Aars2 plus tard, après la naissance, les animaux semblaient d’abord en bonne santé mais ont rapidement développé des cœurs dilatés et affaiblis avec une importante fibrose. La microscopie électronique a révélé que leurs mitochondries présentaient moins de replis internes, et des tests biochimiques détaillés ont montré que des complexes clés de la chaîne respiratoire, en particulier les complexes I et IV, étaient déstabilisés et perdaient leur activité bien avant l’apparition d’une insuffisance cardiaque manifeste.
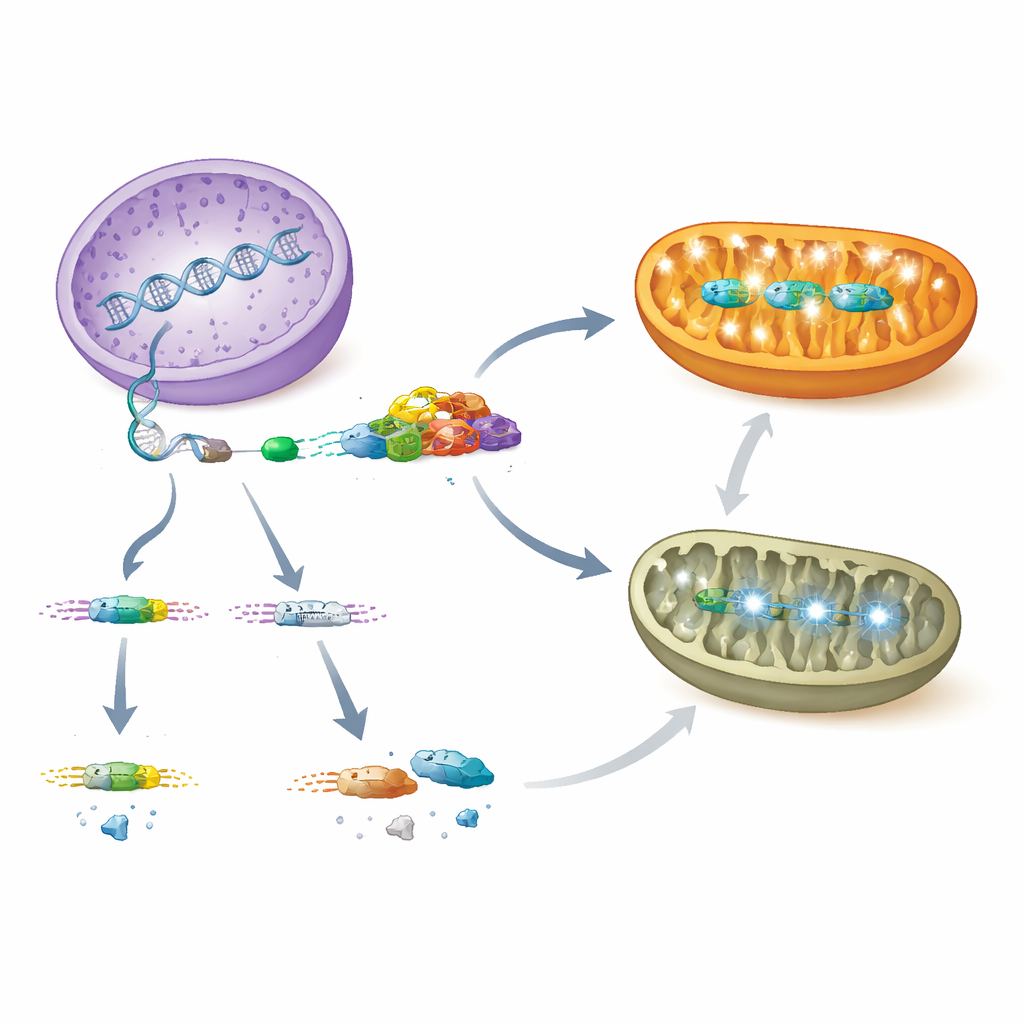
Comment les mitochondries en difficulté communiquent avec le noyau
La défaillance d’AARS2 empêchait les mitochondries des cellules cardiaques de maintenir une phosphorylation oxydative normale, la principale voie de production d’ATP. Dans les cœurs déficients en PCBP1 comme en Aars2, de nombreux gènes nucléaires codant pour des composants de la machinerie énergétique étaient réprimés, et les protéines mitochondriales correspondantes étaient appauvries. Parallèlement, les cellules ont activé un programme coordonné de stress connu sous le nom de réponse aux protéines mal repliées et la réponse intégrée au stress. Des acteurs centraux de cette voie, notamment la protéine ATF4 et son déclencheur en amont, l’eIF2α phosphorylé, ont augmenté fortement, tout comme LONP1, une protéase mitochondriale qui élimine les protéines endommagées. Chez les mutants Aars2 plus âgés, les chercheurs ont également observé l’activation du régulateur de croissance MYC et l’agrandissement du nucléole — l’usine de fabrication des ribosomes — ainsi qu’une hausse des facteurs de traduction mitochondriale codés par le noyau, suggérant que le noyau tentait de compenser la défaillance de la production protéique mitochondriale.
Ce que cela signifie pour les enfants atteints d’insuffisance cardiaque rare
Dans l’ensemble, ces résultats tracent une voie claire du contrôle génétique à la maladie d’organe. PCBP1 se lie normalement à l’ARN d’AARS2 dans les cellules cardiaques et garantit l’inclusion de l’exon 16, produisant une enzyme stable qui soutient la synthèse protéique mitochondriale et une production d’énergie robuste. Lorsque PCBP1 est perdu ou que des mutations perturbent cette étape d’épissage, l’exon 16 est omis, les niveaux d’AARS2 s’effondrent, les complexes énergétiques mitochondriaux se désagrègent et les parois cardiaques en développement n’arrivent pas à se compacter correctement, conduisant à une cardiomyopathie létale. Les mitochondries stressées envoient alors des signaux au noyau pour activer des programmes protecteurs, mais ces réponses ne suffisent pas à prévenir l’insuffisance cardiaque. En éclairant cet axe PCBP1–AARS2, l’étude suggère de nouveaux marqueurs diagnostiques et des cibles thérapeutiques potentielles pour les nourrissons et les enfants atteints de maladies cardiaques mitochondriales autrement inexpliquées.
Citation: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Mots-clés: cardiomyopathie mitochondriale, épissage de l'ARN, malformation cardiaque congénitale, gène AARS2, réponse au stress mitochondrial