Clear Sky Science · es
PCBP1 regula el splicing alternativo de AARS2 en la cardiomiopatía congénita
Por qué algunos bebés nacen con corazones que fallan
Algunos lactantes desarrollan una forma grave de insuficiencia cardíaca poco después del nacimiento, causada no por arterias obstruidas sino por pequeños fallos en cómo las células cardiacas generan energía. Los médicos han vinculado esta condición con mutaciones en un gen llamado AARS2, pero los pasos que conectan un cambio en el ADN con un corazón débil y mal formado han permanecido poco claros. Este estudio descubre un eslabón crucial: un "editor" molecular que ayuda a las células cardíacas a ensamblar correctamente el mensaje de AARS2 para que sus mitocondrias —las plantas de energía de la célula— puedan mantener vivos los corazones en latido.
Un editor molecular que protege el corazón en crecimiento
Los autores se centraron en PCBP1, una proteína que se une al ARN, el mensaje intermedio copiado del ADN. En corazones de ratón en desarrollo, encontraron a PCBP1 fijándose al ARN de AARS2 cerca de una unión crítica. AARS2 ayuda a cargar el aminoácido alanina en los ARN de transferencia dentro de las mitocondrias, un paso clave en la construcción de las proteínas que impulsan la producción de energía. Usando mapas de unión de alto rendimiento y constructos reporteros diseñados, el equipo mostró que los puntos de contacto de PCBP1 coinciden con mutaciones humanas que interrumpen el empalme de una pieza concreta —el exón 16— del mensaje de AARS2. Cuando falta PCBP1 o se dañan sus sitios de unión, este exón se omite, descarrilando las instrucciones para fabricar una enzima AARS2 de longitud completa.
Cuando falla la edición, la estructura del corazón se altera
Para ver qué significa esto a nivel de órgano, los investigadores eliminaron selectivamente PCBP1 de las células del músculo cardíaco de ratón. Estos corazones se desarrollaron de forma anómala: sus paredes eran finas y esponjosas en lugar de densamente compactas, y la punta del corazón con frecuencia se dividía en dos, una malformación que se asemeja a una condición humana llamada no compaction ventricular izquierda. Muchos ratones murieron poco después del nacimiento. A nivel de ARN, cientos de genes cambiaron hacia un patrón inmaduro, propio de embriones tempranos, lo que indica una maduración retardada de las cámaras cardíacas. De forma notable, el mensaje de Aars2 casi siempre omitía el exón 16, dando lugar a un transcript acortado y a una caída dramática de la proteína AARS2, confirmando que el empalme defectuoso de este único gen es una consecuencia principal de la pérdida de PCBP1.
Dañar directamente AARS2 recrea la enfermedad
A continuación, el equipo diseñó ratones en los que el exón 16 de Aars2 podía eliminarse solo en las células del músculo cardíaco. Estos animales imitaron de cerca a los nulos para PCBP1: mostraron paredes ventriculares malformadas, murieron alrededor del nacimiento y sus corazones exhibieron la misma firma de expresión génica inmadura. Cuando los investigadores provocaron la pérdida de Aars2 más tarde en la vida usando un segundo interruptor genético posnatal, los animales inicialmente parecían sanos pero pronto desarrollaron corazones agrandados y debilitados con cicatrización extensa. La microscopía electrónica reveló que sus mitocondrias tenían menos pliegues internos, y ensayos bioquímicos detallados mostraron que complejos clave productores de energía en la cadena respiratoria, especialmente los complejos I y IV, se desestabilizaron y perdieron actividad mucho antes de que apareciera la insuficiencia cardíaca evidente.
Cómo las mitocondrias en apuros retroalimentan al núcleo
La pérdida de AARS2 dejó a las mitocondrias de las células cardíacas incapaces de mantener la fosforilación oxidativa normal, la principal vía para generar ATP. En corazones deficientes en PCBP1 y en Aars2, muchos genes nucleares que codifican componentes de la maquinaria energética se expresaron menos, y las proteínas mitocondriales correspondientes quedaron agotadas. Al mismo tiempo, las células activaron un programa coordinado de estrés conocido como la respuesta ante proteínas desplegadas y la respuesta integrada de estrés. Participantes centrales en esta vía, incluida la proteína ATF4 y su activador aguas arriba, eIF2α fosforilada, aumentaron marcadamente, al igual que LONP1, una proteasa mitocondrial que elimina proteínas dañadas. En mutantes de Aars2 de mayor edad, los investigadores también observaron activación del regulador de crecimiento MYC y agrandamiento del nucléolo —la fábrica de ribosomas— junto con un auge de factores de traducción mitocondrial codificados por el núcleo, lo que sugiere que el núcleo intentaba compensar la caída en la producción de proteínas mitocondriales.
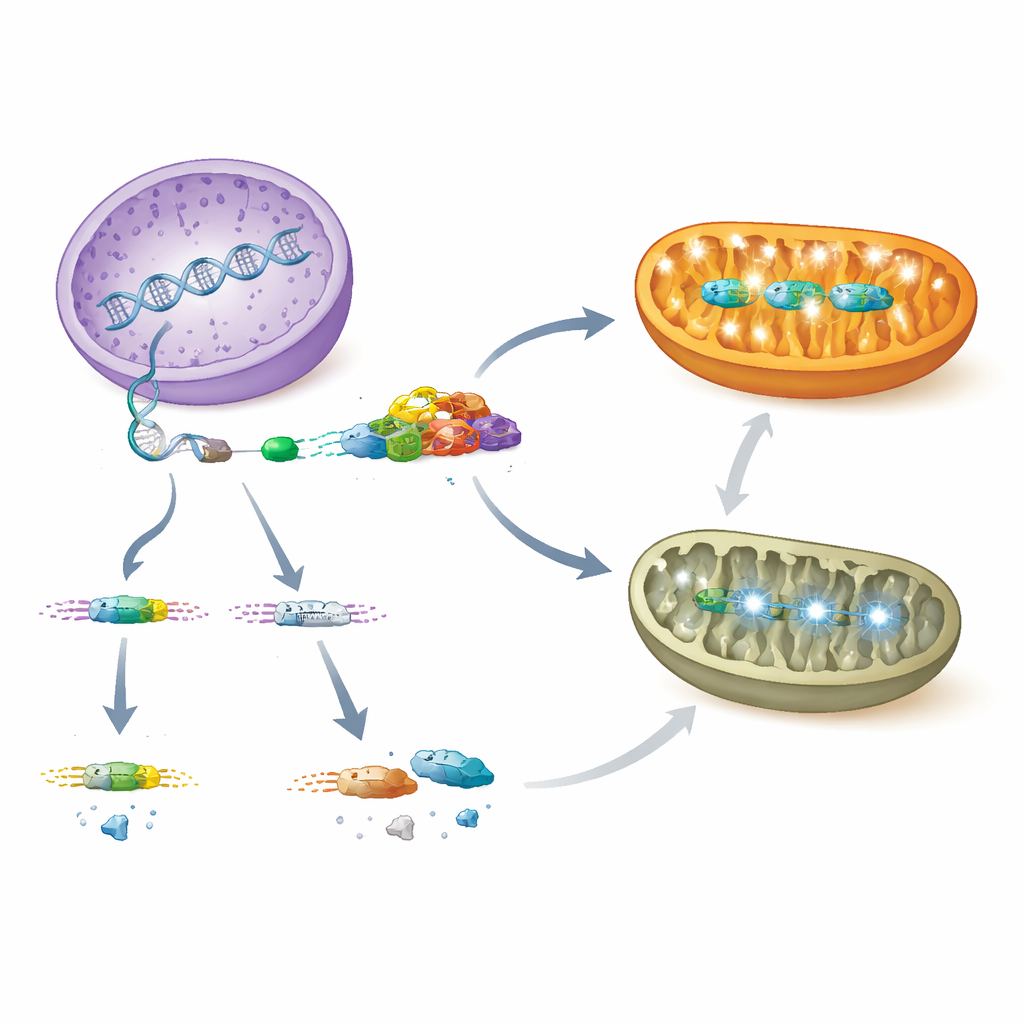
Qué significa esto para niños con insuficiencia cardíaca rara
En conjunto, estos hallazgos delinean una vía clara desde la regulación génica hasta la enfermedad del órgano. PCBP1 normalmente se une al ARN de AARS2 en las células cardíacas y asegura que se incluya el exón 16, produciendo una enzima estable que sostiene la síntesis de proteínas mitocondriales y un rendimiento energético robusto. Cuando se pierde PCBP1 o cuando las mutaciones interrumpen este paso de empalme, el exón 16 se omite, los niveles de AARS2 colapsan, los complejos energéticos mitocondriales se desarman y las paredes en desarrollo del corazón no se compactan correctamente, conduciendo a una cardiomiopatía letal. Las mitocondrias estresadas entonces señalan de vuelta al núcleo para activar programas protectores, pero estas respuestas no son suficientes para prevenir la insuficiencia cardíaca. Al iluminar este eje PCBP1–AARS2, el estudio sugiere nuevos marcadores diagnósticos y posibles dianas terapéuticas para lactantes y niños con una enfermedad cardíaca mitocondrial que de otro modo es misteriosa.
Cita: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Palabras clave: cardiomiopatía mitocondrial, splicing de ARN, enfermedad cardíaca congénita, gen AARS2, respuesta al estrés mitocondrial