Clear Sky Science · ru
PCBP1 регулирует альтернативный сплайсинг AARS2 при врожденной кардиомиопатии
Почему некоторые младенцы рождаются с недостаточностью сердца
У некоторых новорождённых вскоре после рождения развивается тяжёлая форма сердечной недостаточности, вызванная не закупоркой сосудов, а крошечными сбоями в том, как сердечные клетки вырабатывают энергию. Врачи связали это состояние с мутациями в гене AARS2, однако механизмы, приводящие от изменения в ДНК к слабому, плохо сформированному сердцу, оставались неясными. В этом исследовании обнаружена ключевая недостающая ссылка: молекулярный «редактор», который помогает сердечным клеткам правильно собирать матрицу AARS2, чтобы их митохондрии — электростанции клетки — могли поддерживать работу сердца.
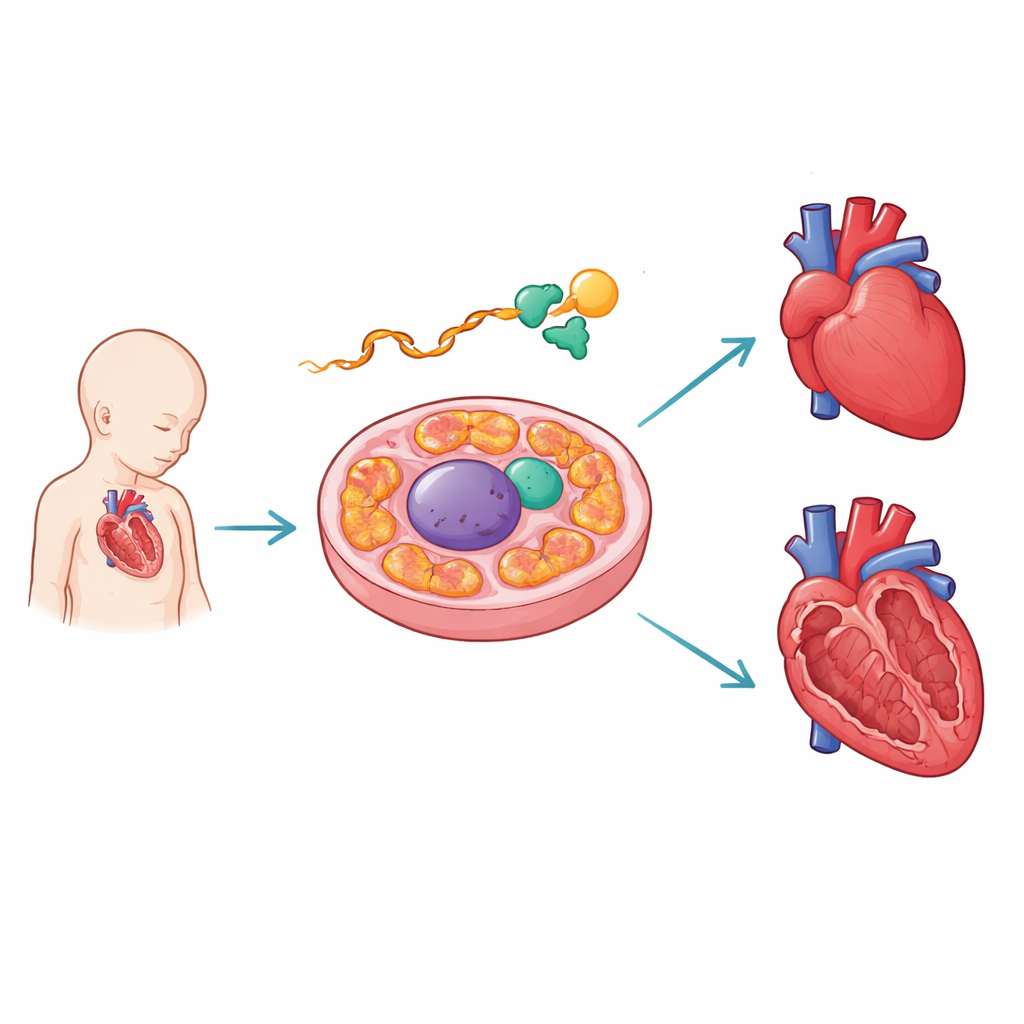
Молекулярный редактор, охраняющий развивающееся сердце
Авторы сосредоточились на белке PCBP1, который связывается с РНК — промежуточными сообщениями, переписываемыми с ДНК. В развивающихся сердцах мышей они обнаружили, что PCBP1 цепляется за РНК AARS2 рядом с критическим участком сплайсинга. AARS2 помогает присоединять аминокислоту аланин к транспортным РНК внутри митохондрий — ключевой шаг в построении белков, обеспечивающих выработку энергии. С помощью высокопроизводительного картирования сайтов связывания и инженерных репортерных конструкций команда показала, что точки контакта PCBP1 совпадают с человеческими болезнетворными мутациями, нарушающими включение одного конкретного фрагмента — экзона 16 — в транскрипт AARS2. Когда PCBP1 отсутствует или его сайты связывания повреждены, этот экзон вырезается, что сбивает инструкцию по синтезу полноразмерного фермента AARS2.
Когда «редактирование» даёт сбой, строение сердца искажается
Чтобы посмотреть, что это означает для целого органа, исследователи выборочно удалили PCBP1 из кардиомиоцитов мыши. Такие сердца развивались ненормально: их стенки были тонкими и губчатыми вместо плотной компактности, а кончик сердца часто распадался на две части — дефект, напоминающий у человека состояние, известное как ненапряжённая компактность левого желудочка. Многие мыши умирали вскоре после рождения. На уровне РНК сотни генов смещались к незрелому, эмбриональному паттерну, что указывает на задержку созревания камер сердца. Примечательно, что транскрипт Aars2 почти всегда исключал экзон 16, что приводило к укороченной матрице и драматическому падению уровня белка AARS2, подтвердив, что ошибочный сплайсинг этого единственного гена — важное следствие потери PCBP1.
Прямое повреждение AARS2 воспроизводит заболевание
Далее команда создала мышей, в которых экзон 16 Aars2 можно было удалить только в кардиомиоцитах. Эти животные сильно напоминали ПКВP1-«выключенные» модели: у них наблюдались уродства стенок желудочка, смерть около рождения и такой же незрелый профиль экспрессии генов в сердце. Когда исследователи вызвали потерю Aars2 позже, после рождения, используя второй генетический переключатель, животные сначала выглядели здоровыми, но вскоре развили увеличенные, ослабленные сердца с обширным рубцеванием. Электронная микроскопия показала, что у их митохондрий стало меньше внутренних складок, а биохимические анализы выявили дестабилизацию и потерю активности ключевых комплексов дыхательной цепи, особенно комплексов I и IV, задолго до явной сердечной недостаточности.
Как испытывающие трудности митохондрии «отвечают» ядру
Нарушение AARS2 лишило митохондрии кардиомиоцитов способности поддерживать нормальный окислительный фосфорилирование — основной путь генерирования АТФ. И в сердцах, дефицитных по PCBP1, и в Aars2-дефицитных сердцах многие ядерные гены, кодирующие компоненты энергетического аппарата, были подавлены, а соответствующие митохондриальные белки истощены. Одновременно клетки включили скоординированную программу стресса, известную как ответ на неправильную свёртку белков и интегрированный стрессовый ответ. Центральные участники этого пути, включая белок ATF4 и его верхний триггер фосфорилированный eIF2α, резко возросли, как и LONP1 — митохондриальная протеаза, удаляющая повреждённые белки. У старших Aars2-мутантов исследователи также наблюдали активацию регулятора роста MYC и увеличение ядрышка — фабрики по сборке рибосом — вместе с всплеском ядерно-кодируемых факторов митохондриального трансляции, что указывает на попытки ядра компенсировать падающее митохондриальное производство белка.
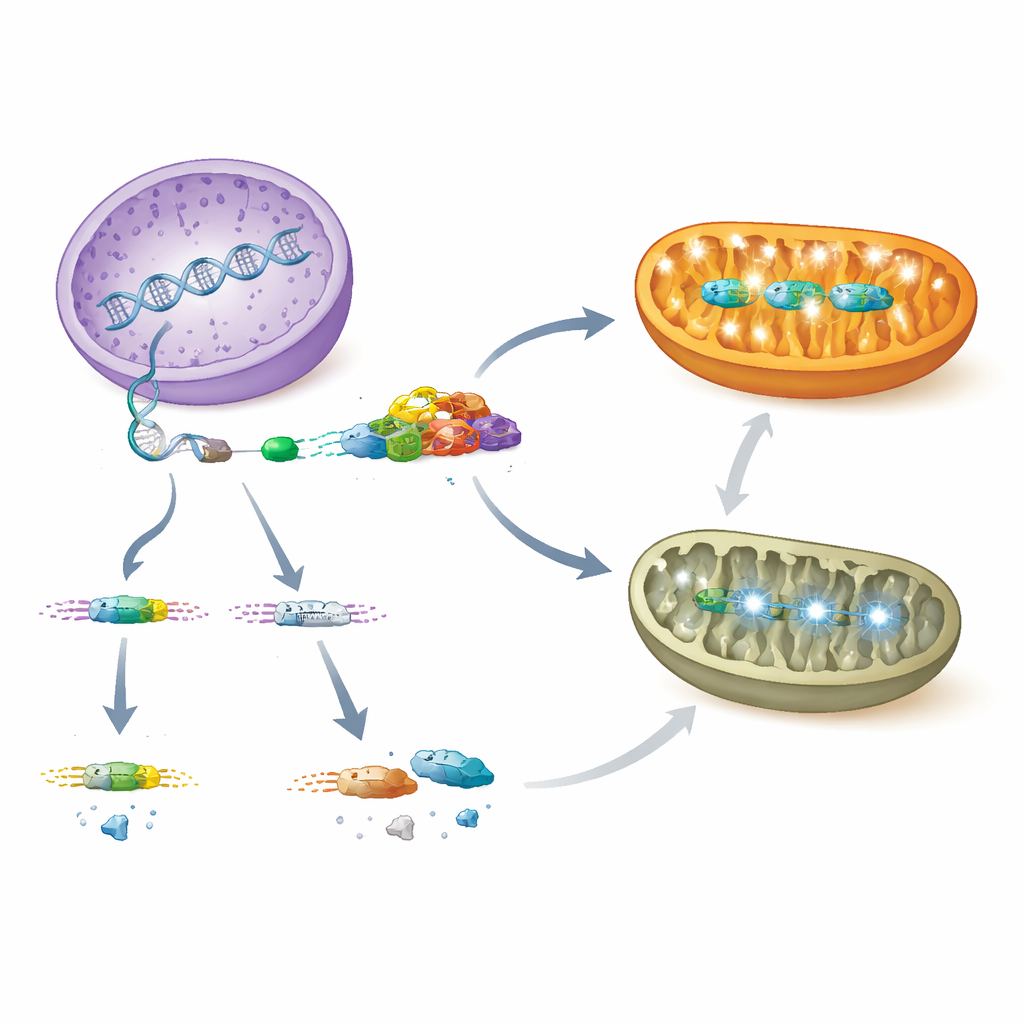
Что это значит для детей с редкой сердечной недостаточностью
Вместе эти результаты описывают ясный путь от регуляции гена до органного заболевания. В норме PCBP1 связывается с РНК AARS2 в кардиомиоцитах и обеспечивает включение экзона 16, что даёт стабильный фермент, поддерживающий митохондриальный синтез белка и надёжную выработку энергии. Когда PCBP1 теряется или мутации нарушают этот шаг сплайсинга, экзон 16 исключается, уровень AARS2 падает, митохондриальные энергетические комплексы распадаются, и стенки развивающегося сердца не компактизируются должным образом, что приводит к летальной кардиомиопатии. Испытывающие стресс митохондрии затем посылают сигналы обратно в ядро, активируя защитные программы, но эти ответы оказываются недостаточными, чтобы предотвратить сердечную недостаточность. Осветив ось PCBP1–AARS2, исследование предлагает новые диагностические маркеры и потенциальные терапевтические мишени для младенцев и детей с загадочными митохондриальными заболеваниями сердца.
Цитирование: Lu, Y.W., Liang, Z., Dorr, K. et al. PCBP1 regulates alternative splicing of AARS2 in congenital cardiomyopathy. Nat Cardiovasc Res 5, 328–350 (2026). https://doi.org/10.1038/s44161-026-00798-3
Ключевые слова: митохондриальная кардиомиопатия, сплайсинг РНК, врожденные пороки сердца, ген AARS2, ответ на митохондриальный стресс