Clear Sky Science · zh
衰老钟描绘对神经变性易感或具有抗性的新元胞类型并识别神经保护干预措施
为何某些脑细胞衰老更快
为何有些脑细胞在生命早期就衰退,而另一些则能保持数十年旺盛?这个问题是阿尔茨海默病、帕金森病等多种衰老相关疾病的核心。在这项研究中,研究者使用了一个微小的线虫秀丽隐杆线虫(Caenorhabditis elegans),其整个神经系统已逐细胞绘制出连结图,用以探究不同类型的神经元是否具有各自的“生物学年龄”,以及这些年龄是否能预测哪些细胞会变性。研究不仅锁定了易受损的神经元类型和加速其衰退的分子过程,还发现了可以减慢或加速神经元衰老的小分子——这些线索可能对人类大脑有所启发。
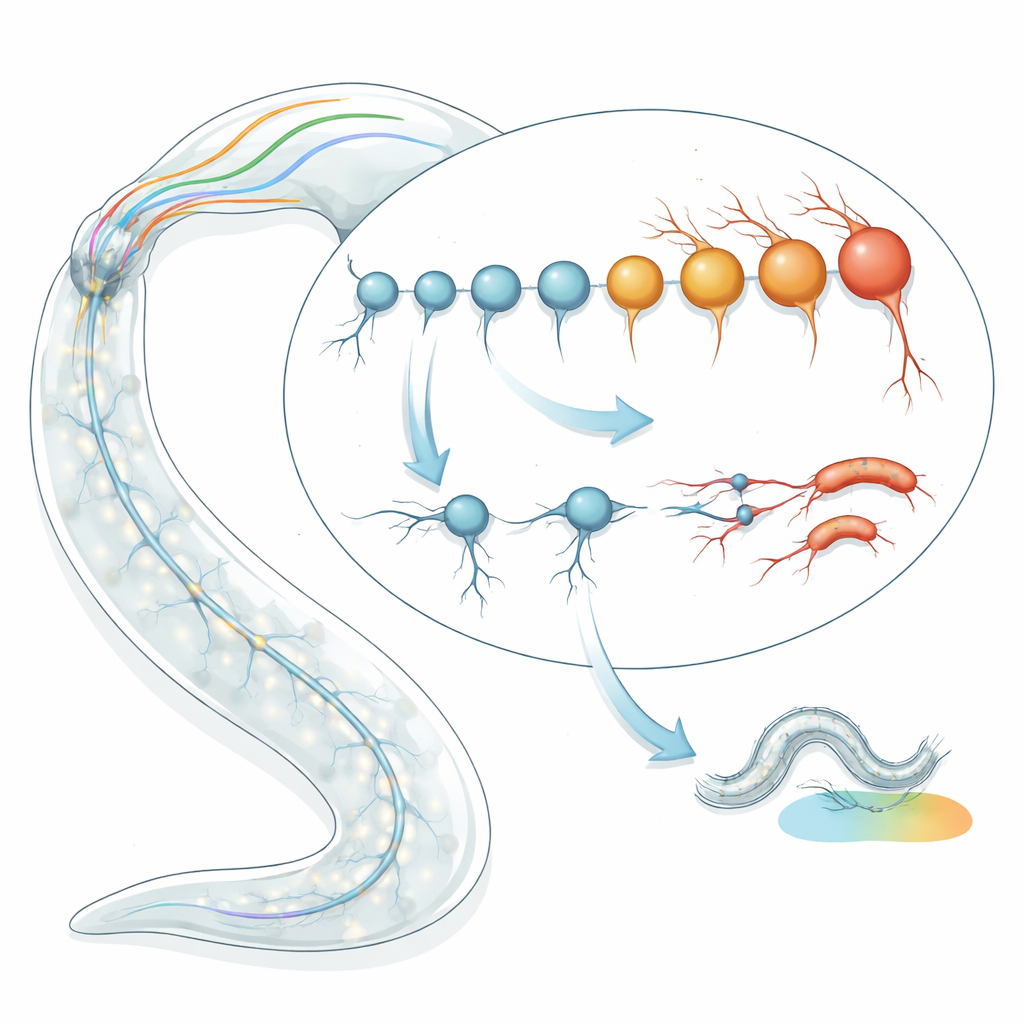
单个神经细胞的年龄计时
研究团队首先将转录组学“衰老钟”应用到C. elegans的单个神经元类型上。他们不以线虫的日历年龄为准,而是通过基因活动模式来估算每类细胞的生物学年龄。使用两种独立的钟模型——一种基于典型的衰老基因特征,另一种捕捉随机变化随时间累积的模式——他们分析了晚幼虫期和成年早期线虫中128种定义明确的神经元类型的RNA测序数据。令人惊讶的是,在这些时间上相同的神经元之间,预测的生物学年龄存在近两到四倍的差异。有些神经元看起来远比预期“年轻”,而另一些则显得过早“老化”,且这些估计在多个数据集和测序方法间一致。
从分子年龄到可见损伤与行为丧失
为了验证这些年龄预测在真实线虫中的意义,研究者使用荧光标记随时间追踪所选神经元的结构状况。被预测为生物学上年轻的神经元(如 I2、OLL 和 PHC)在老化过程中仅有少数动物出现轻微结构损伤。相反,被预测为“年老”的神经元(包括 ASI、ASJ 和 ASK)在晚幼虫期近一半就已显示退化迹象,到成虫一周时约达90%。损伤表现为沿神经纤维出现的微小肿胀和突起,并且沿每条神经突起的大致分布呈随机增加,符合一种随机性衰老过程而非固定的发育程序。早期结构衰退也转化为真实的行为缺陷:在某些由单一神经元类型控制特定任务的回路中,该神经元的退化与防御病原体或基于盐度的学习失败紧密对应。
为何暴露的感受性神经元风险更高
将生物学年龄估计映射到线虫的完整神经系统连结组上,呈现出引人注目的模式。最老的神经元聚集在头部的纤毛感受性细胞中,尤其是那些纤毛直接暴露于环境的嗅器(amphid)神经元。这些细胞负责感知化学物质、气味和其他信号,富含神经肽和受体。在神经元类型间,表达更多神经肽和受体的神经元与较高的生物学年龄相关,而突触数量本身并不相关。其纤毛感受末端伸出到外界的神经元最为老化,提示环境暴露与高强度信号处理负荷可能使其更容易早期衰退。这与人类神经学的观察相呼应:在人类阿尔茨海默病中,暴露于环境的嗅觉系统纤毛神经元往往首当其冲退化。
蛋白质生成:衰老的驱动因素与调控手柄
为揭示这些年龄差异背后的机制,团队按生物学年龄对神经元分组并检查基因表达趋势。他们发现与核糖体生物发生、蛋白质合成和核仁功能相关的过程在较老的神经元中富集,伴随突触和神经肽信号基因的变化。这提示高强度的蛋白质生成可能成为加速神经元磨损的负担。研究者随后用适量环己酰亚胺(cycloheximide)进行测试,这是一种可以部分减缓翻译的化合物。对快速衰老的神经元而言,这种温和抑制显著减少了结构损伤并在盐学习任务中保留了功能,且保护效果在停药后仍持续。相较之下,缓慢衰老的神经元基本不受影响。这些结果将高翻译负荷与神经元特异性易感性联系起来,并表明通过降低蛋白质合成可以恢复易损细胞的结构和功能完整性。
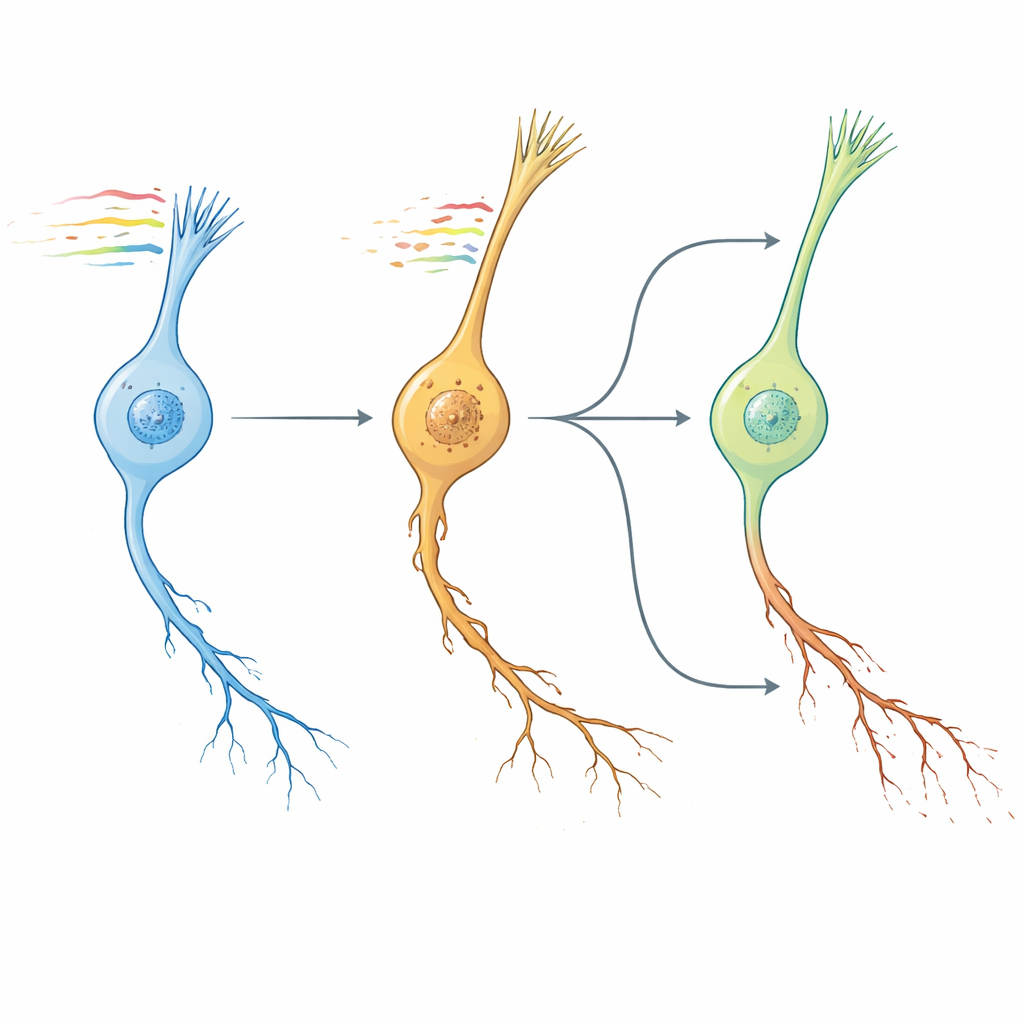
线虫衰老钟、人类大脑与药物线索
接下来,作者考察线虫神经元的衰老模式是否类似哺乳动物的大脑衰老。通过比较保守基因的通路层面变化,他们发现C. elegans的转录组“NeuronAge”特征与来自多个小鼠和人类脑区的衰老轨迹紧密聚类,而已知的延缓衰老干预——如年轻血液因子、运动和膳食化合物——则显示相反的模式。利用这种保守性,他们转向大型人类细胞系资源,进行体外计算搜索以找出能逆转或模拟 NeuronAge 的小分子。那些与 NeuronAge 表型相反的化合物被标记为潜在的神经保护剂;强化该表型的则被视为潜在神经毒素。在线虫中的实验验证了若干预测。植物来源代谢物丁香酸(syringic acid)和药物 vanoxerine 都减少了快速衰老神经元的退化而不损害年轻神经元;而 Bay K8644 和 WAY-100635 等试剂则加剧了神经突起损伤并损害行为。即便广为宣称具有保护作用的白藜芦醇(resveratrol),在该系统中也表现为促衰老并增加了神经病理。
对大脑健康的意义
归根结底,这项工作表明即便在单一神经系统内,不同类型的神经元也以不同速度经历衰老,而这些内部时钟可以预测哪些细胞会首先退化并丧失功能。面向外界且蛋白质合成水平高的感受性神经元尤其脆弱。通过将神经元特异性衰老与保守的基因表达通路联系起来,该研究提供了一种将简单线虫的发现转译到人类大脑的方法。同样重要的是,它证明了转录组衰老特征可以作为筛选工具,识别能减缓或加速神经变性的分子。尽管在将这些候选物用于人类治疗之前仍需大量工作,该方法指向了一个未来:我们不仅能测量各类神经元的生物学年龄,还能基于理性设计的干预使其保持更长时间的年轻状态。
引用: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
关键词: 神经元衰老, 神经变性, 蛋白质合成, 秀丽隐杆线虫, 神经保护