Clear Sky Science · tr
Yaşlanma saatleri, nörodejenerasyona karşı savunmasız veya dirençli olan nöron tiplerini ayırt ediyor ve nöroprotektif müdahaleleri tanımlıyor
Neden bazı beyin hücreleri diğerlerinden daha hızlı yaşlanır
Neden bazı beyin hücreleri yaşamın erken dönemlerinde solarken, diğerleri onlarca yıl boyunca dayanıklı kalır? Bu soru, Alzheimer’dan Parkinson hastalığına kadar birçok yaşa bağlı bozukluğun merkezinde yer alır. Bu çalışmada araştırmacılar, tüm sinir sistemi hücre hücreye haritalanmış küçük bir yuvarlak solucan olan Caenorhabditis elegans’i kullanarak farklı nöron tiplerinin kendi “biyolojik yaşları” olup olmadığını ve bu yaşların hangi hücrelerin dejenerasyona uğrayacağını öngörüp öngörmediğini incelediler. Çalışmaları yalnızca savunmasız nöron tiplerini ve bunların çöküşünü hızlandıran moleküler bir süreci belirlemekle kalmıyor, aynı zamanda nöronal yaşlanmayı yavaşlatabilen veya hızlandırabilen küçük molekülleri de açığa çıkararak insan beyni için çıkarımlar sunuyor.
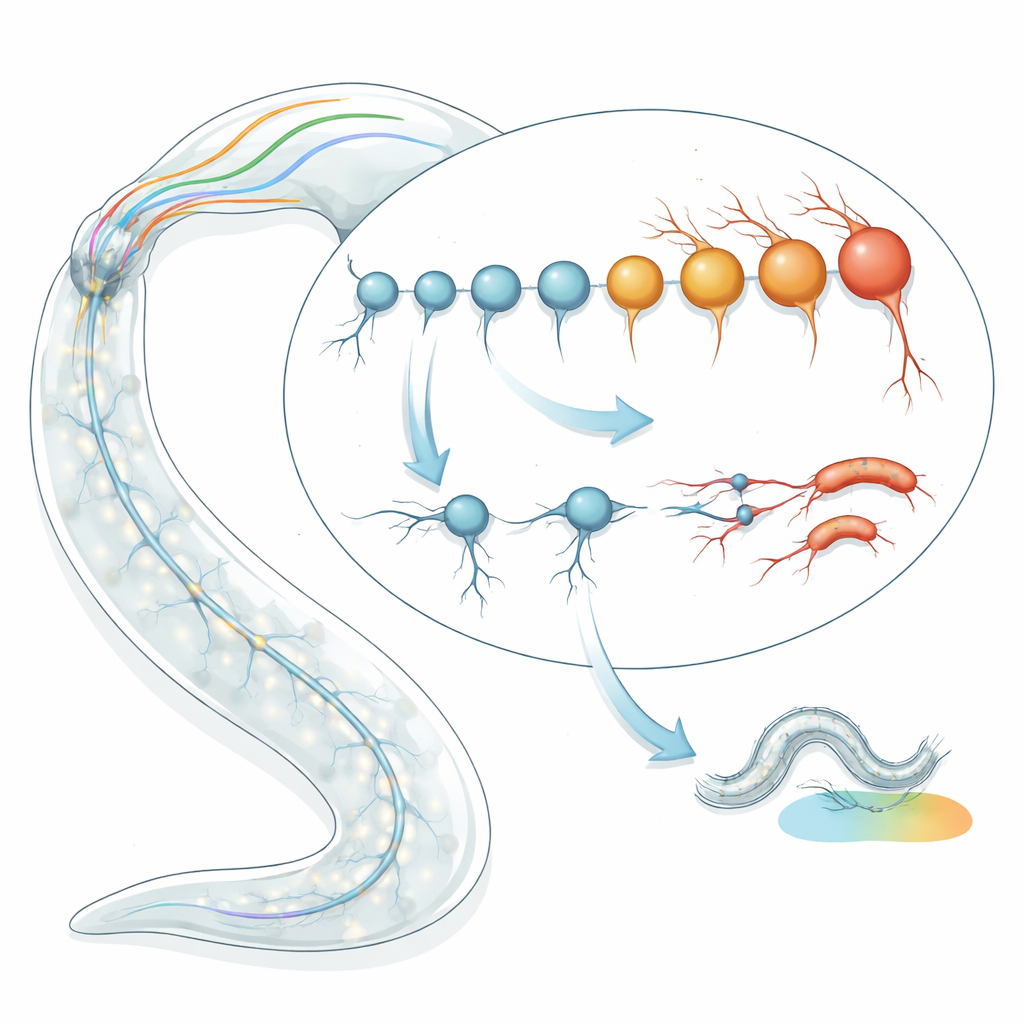
Tek tek sinir hücrelerinin yaşını zamanlamak
Takım, C. elegans’taki bireysel nöron tiplerine transkriptomik “yaşlanma saatleri” uygulayarak başladı. Solucanın yaşına günler olarak bakmak yerine, her hücre tipinin biyolojik yaşını tahmin etmek için gen etkinliği desenlerini incelediler. Birisi karakteristik yaşlanma gen imzalarına dayanan ve diğeri rastgele değişimlerin zamanla nasıl biriktiğini yakalayan iki bağımsız saat modelini kullanarak, geç larva ve genç yetişkin solucanlardan 128 iyi tanımlanmış nöron tipi için RNA dizileme verilerini analiz ettiler. Şaşırtıcı biçimde, aynı kronolojik yaşta olan nöronlar arasında tahmini biyolojik yaşta neredeyse iki ila dört katı bulan bir yayılma buldular. Bazı nöronlar beklenenden çok daha “genç” görünürken, diğerleri erken “yaşlı” görünüyordu ve bu tahminler birden çok veri seti ve dizileme yöntemi arasında tutarlıydı.
Moleküler yaştan görünür hasar ve davranış kaybına
Bu yaş tahminlerinin gerçek solucanlarda önemli olup olmadığını test etmek için araştırmacılar seçilen nöronların fiziksel durumunu zaman içinde floresan belirteçlerle izlediler. Biyolojik olarak genç olduğu tahmin edilen nöronlar (örneğin I2, OLL ve PHC), solucanlar yaşlandıkça sadece az sayıda hayvanda hafif yapısal hasar gösterdi. Buna karşılık, yaşlı olduğu tahmin edilen nöronlar (ASI, ASJ ve ASK dahil), geç larvaların neredeyse yarısında zaten bozulma belirtileri gösteriyor ve yetişkinliğin bir haftasında bu oran yaklaşık %90’a yükseliyordu. Hasar, sinir lifleri boyunca küçük şişkinlikler ve uzantılar olarak belirdi ve her bir nöritte yaklaşık olarak rastgele bir şekilde arttı; bu, sabit bir gelişim programından ziyade stokastik bir yaşlanma süreciyle tutarlıydı. Erken yapısal çöküş aynı zamanda gerçek davranışsal bozukluklara da yansıdı: tek bir nöron tipinin belirli bir görevi kontrol ettiği devrelerde, o nöronun dejenerasyonu patojen kaçınması veya tuz temelli öğrenmedeki başarısızlıklarla yakından eşleşti.
Neden açıkta olan duyu nöronları özel risk altında
Biyolojik yaş tahminlerini solucanın tam sinir sistemi konnektomuna haritalamak çarpıcı bir desen ortaya koydu. En yaşlı nöronlar, özellikle kılı tüylü (silialı) baştaki duyu hücreleri arasında kümelenmişti; özellikle cilia’ları doğrudan çevreye açık olan amfid nöronlar göze çarpıyordu. Bu hücreler kimyasalları, kokuları ve diğer ipuçlarını algılar ve çok sayıda nöropeptit ve reseptörle donatılmıştır. Nöron tipleri arasında daha yüksek sayıda ifade edilen nöropeptit ve reseptör, daha yaşlı biyolojik yaş ile koreleydi; oysa sinapsların toplam sayısı böyle bir ilişki göstermedi. Duyu uçları dış dünyaya doğru uzanan silialı nöronlar en yaşlı olanlardı; bu da çevresel maruziyetin ve yoğun sinyal yükünün bunları erken çöküşe yatkın kılabileceğini düşündürüyor. Bu durum, insan nörolojisindeki bir yankıyla örtüşüyor: Alzheimer hastalığında çevresel olarak maruz kalan, olfaktör sistemdeki silialı nöronlar ilk bozulanlar arasında yer alır.
Proteinin üretilmesi: yaşlanmanın itici gücü — ve müdahale noktası
Bu yaş farklarının arkasındaki mekanizmaları açığa çıkarmak için ekip, nöronları biyolojik yaşlarına göre gruplandırdı ve gen ifade eğilimlerini inceledi. Ribozom biyogenezi, protein sentezi ve nükleol fonksiyonuyla ilgili süreçlerin, sinaptik ve nöropeptid sinyalleşme genlerindeki değişikliklerle birlikte, daha yaşlı nöronlarda zenginleştiğini buldular. Bu, yoğun protein üretiminin nöronal aşınmayı hızlandıran olası bir yük olduğunu işaret ediyordu. Araştırmacılar daha sonra translasyonu kısmen yavaşlatan sikloheksimid adlı bileşiğin mütevazı bir dozunu test ettiler. Hızlı yaşlanan nöronlarda, bu hafif inhibisyon yapısal hasarı önemli ölçüde azalttı ve bir tuz öğrenme görevindeki performansı korudu; koruyucu etkiler tedavi durduktan sonra bile sürdü. Yavaş yaşlanan nöronlar ise büyük ölçüde etkilenmedi. Bu sonuçlar yüksek translasyon yükünü nöron-spesifik kırılganlıkla bağdaştırıyor ve protein sentezini kısmanın risk altındaki hücrelerde yapısal ve işlevsel bütünlüğü yeniden sağlayabileceğini gösteriyor.
Solucan saatleri, insan beyinleri ve ilaç adayları
Sırada yazarlar, solucan nöron yaşlanma örüntülerinin memelilerdeki beyin yaşlanmasına benzer olup olmadığını sordular. Korunmuş genler arasındaki yol düzeyindeki değişiklikleri karşılaştırarak, C. elegans’taki transkriptomik “NeuronAge” imzasının birden çok fare ve insan beyin bölgesinden gelen yaşlanma yörüngeleriyle sıkı bir şekilde kümelendiğini buldular; bilinen geroprotektif müdahaleler—genç kan faktörleri, egzersiz ve diyet bileşikleri gibi—karşıt desenler gösteriyordu. Bu korunumu kullanarak, in silico olarak NeuronAge’i tersine çeviren veya taklit eden küçük molekülleri aramak için büyük bir insan hücre hattı kaynağına yöneldiler. Profilleri NeuronAge’e karşıt olan bileşikler potansiyel nörokoruyucular; onu güçlendirenler ise potansiyel nörotoksinler olarak işaretlendi. Solucanlarda yapılan deneysel testler birkaç tahmini doğruladı. Bitkisel kaynaklı metabolit siringik asit ve ilaç vanoxerine, genç nöronlara zarar vermeden hızlı yaşlanan nöronlardaki dejenerasyonu azalttı; Bay K8644 ve WAY-100635 gibi ajanlar ise nörit hasarını kötüleştirdi ve davranışı bozdu. Sıklıkla koruyucu olarak öne sürülen resveratrol bile bu sistemde pro-yaşlanma olarak ortaya çıktı ve nöronal patolojiyi artırdı.
Bu, beyin sağlığı için ne anlama geliyor
Özetle, bu çalışma tek bir sinir sistemi içinde bile farklı nöron tiplerinin farklı hızlarda yaşlandığını ve bu iç saatlerin hangi hücrelerin önce dejenerasyona uğrayıp işlevini kaybedeceğini öngördüğünü gösteriyor. Dış dünyaya bakan ve yoğun protein üretimi yürüten duyu nöronları özellikle hassas görünüyor. Nöron-spesifik yaşlanmayı korunmuş gen ifade yollarına bağlayarak, çalışma basit bir solucandan insan beynine çıkarım yapmanın bir yolunu sunuyor. Aynı derecede önemli olarak, transkriptomik yaşlanma imzalarının nörodejenerasyonu yavaşlatan veya hızlandıran molekülleri tanımlamak için güçlü bir filtre olarak kullanılabileceğini gösteriyor. Bu adayların insan tedavisi için düşünülmeden önce yapılması gereken çok şey olsa da, yaklaşım bize bireysel nöron tiplerinin biyolojik yaşını ölçebileceğimiz ve bunları daha uzun süre genç tutmak için müdahaleleri akılcı şekilde tasarlayabileceğimiz bir geleceğe işaret ediyor.
Atıf: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Anahtar kelimeler: nöronal yaşlanma, nörodejenerasyon, protein sentezi, Caenorhabditis elegans, nörokoruma