Clear Sky Science · sv
Åldringsklockor skiljer ut neuron-typer sårbara eller motståndskraftiga mot neurodegeneration och identifierar neurobeskyddande interventioner
Varför vissa hjärnceller åldras snabbare än andra
Varför viss hjärnceller vissnar tidigt i livet medan andra förblir robusta i årtionden? Denna fråga ligger i kärnan för många åldersrelaterade sjukdomar, från Alzheimers till Parkinsons sjukdom. I denna studie använde forskarna en liten rundmask, Caenorhabditis elegans, vars hela nervsystem är kartlagt cell för cell, för att undersöka om olika neurontyper har sina egna ”biologiska åldrar” och om dessa åldrar förutsäger vilka celler som kommer att degenerera. Deras arbete pekar inte bara ut sårbara neurontyper och en molekylär process som snabbar på deras förfall, utan visar också små molekyler som kan bromsa eller påskynda neuronal åldrande — vilket ger ledtrådar som kan vara relevanta även för människans hjärna.
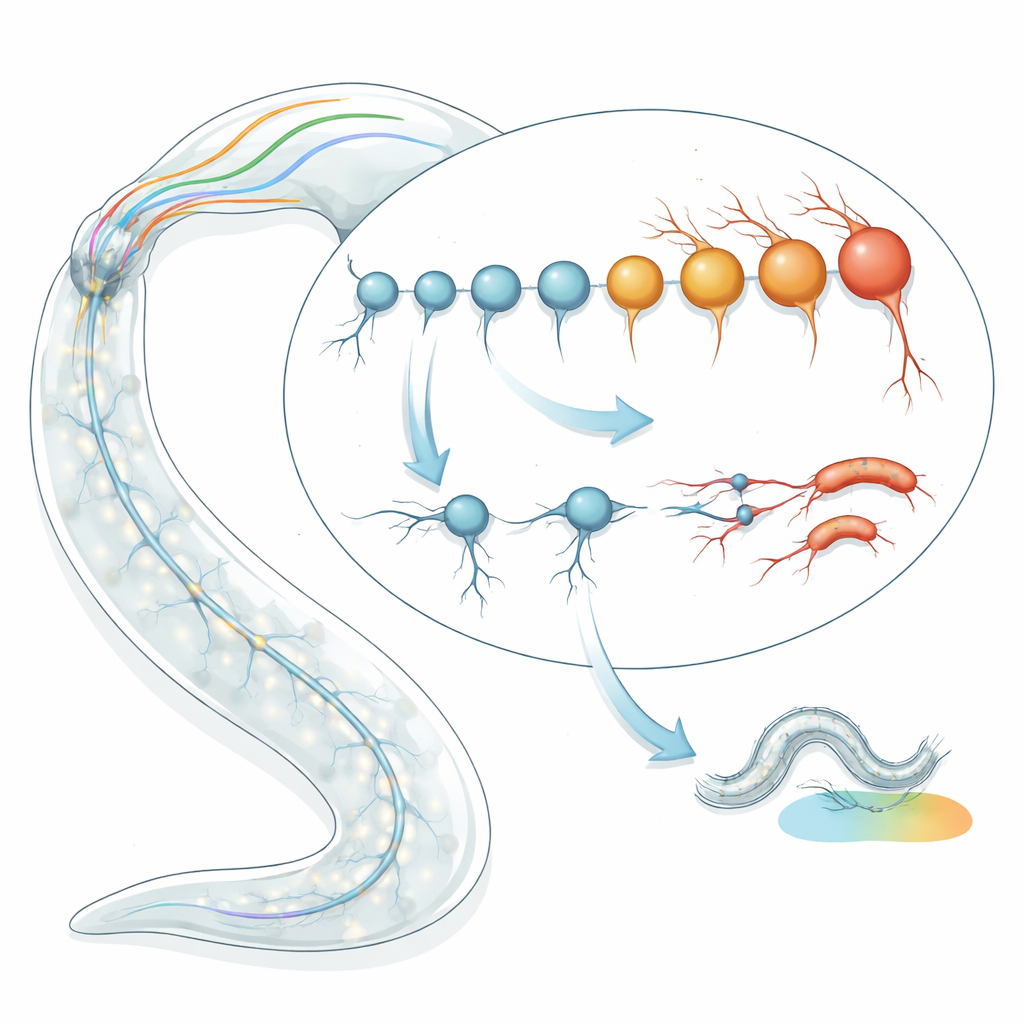
Tidsbestämning av enskilda nervcellers ålder
Teamet började med att tillämpa transcriptomiska ”åldringsklockor” på individuella neurontyper i C. elegans. Istället för att se på maskens ålder i dagar undersökte de mönster av genaktivitet för att uppskatta varje celltyps biologiska ålder. Med två oberoende klockmodeller — en baserad på karakteristiska åldringsgensignaturer och en annan som fångar hur stokastiska förändringar ackumuleras över tid — analyserade de RNA-sekvenseringsdata för 128 väl definierade neurontyper i sena larv- och unga vuxna maskar. Förvånansvärt nog fann de nästan två- till fyrfaldig spridning i förutsagd biologisk ålder bland neuroner som alla hade samma kronologiska ålder. Vissa neuroner framstod som mycket ”yngre” än väntat, medan andra verkade för tidigt ”gamla”, och dessa uppskattningar var konsekventa över flera dataset och sekvenseringsmetoder.
Från molekylär ålder till synlig skada och förlorat beteende
För att testa om dessa åldersprediktioner spelade roll i verkliga maskar följde forskarna fysisk kondition hos utvalda neuroner över tid med fluorescerande markörer. Neuroner som förutsagts vara biologiskt unga (såsom I2, OLL och PHC) visade bara lindrig strukturell skada hos en minoritet av djuren när maskarna åldrades. I stark kontrast visade neuroner som förutsagts vara gamla (inklusive ASI, ASJ och ASK) redan tecken på försämring hos nästan hälften av sena larver, vilket steg till omkring 90 % vid en veckas vuxen ålder. Skadorna visade sig som små svullnader och utväxter längs nervfibrerna och ökade ungefär slumpmässigt längs varje neurit, i överensstämmelse med en stokastisk åldringsprocess snarare än ett fast utvecklingsprogram. Tidig strukturell nedgång överförde sig också till verkliga beteendedeficiter: i kretsar där en enda neurontyp styr en specifik uppgift matchade degenerationen av just den neuronen nära misslyckanden i patogenundvikande beteende eller saltbaserat lärande.
Varför exponerade sensoriska neuroner är särskilt utsatta
Kartläggning av de biologiska åldersuppskattningarna på maskens fullständiga nervsystem-connectome avslöjade ett slående mönster. De äldsta neuronerna klustrade bland cilierade sensoriska celler i huvudet, särskilt amphid-neuroner vars cilier är direkt exponerade mot omgivningen. Dessa celler detekterar kemikalier, dofter och andra signaler och är rikligt utrustade med neuropeptider och receptorer. Över neurontyper korrelerade ett högre antal uttryckta neuropeptider och receptorer med äldre biologisk ålder, medan antalet synapser i sig inte gjorde det. Cilierade neuroner vars sensoriska ändar sticker ut mot omvärlden var de mest åldrade, vilket tyder på att både miljöexponering och tung signaleringsbelastning kan predisponera dem för tidigt förfall. Detta ekar mänsklig neurologi, där miljöexponerade, cilierade neuroner i luktssystemet är bland de första att degenerera i Alzheimers sjukdom.
Proteintillverkning som en drivkraft — och ett handtag — för åldrande
För att avslöja mekanismer bakom dessa åldersskillnader grupperade teamet neuroner efter biologisk ålder och undersökte genuttryckstrender. De fann att processer relaterade till ribosombildning, proteinsyntes och nukleolär funktion var förhöjda i äldre neuroner, tillsammans med förändringar i synaptisk och neuropeptid-signalering. Detta pekade mot hög proteintillverkning som en möjlig belastning som accelererar neuronal slitage. Forskarna prövade därefter en måttlig dos cykloheximid, en förening som delvis sänker translationen. I snabbåldrande neuroner minskade denna milda hämning signifikant strukturella skador och bevarade prestanda i en salt-lärande uppgift, med skyddseffekter som kvarstod även efter att behandlingen upphört. Långsammare åldrande neuroner påverkades däremot i stort sett inte. Dessa resultat kopplar hög translational belastning till neuronspecifik sårbarhet och visar att neddragning av proteinsyntes kan återställa strukturell och funktionell integritet hos utsatta celler.
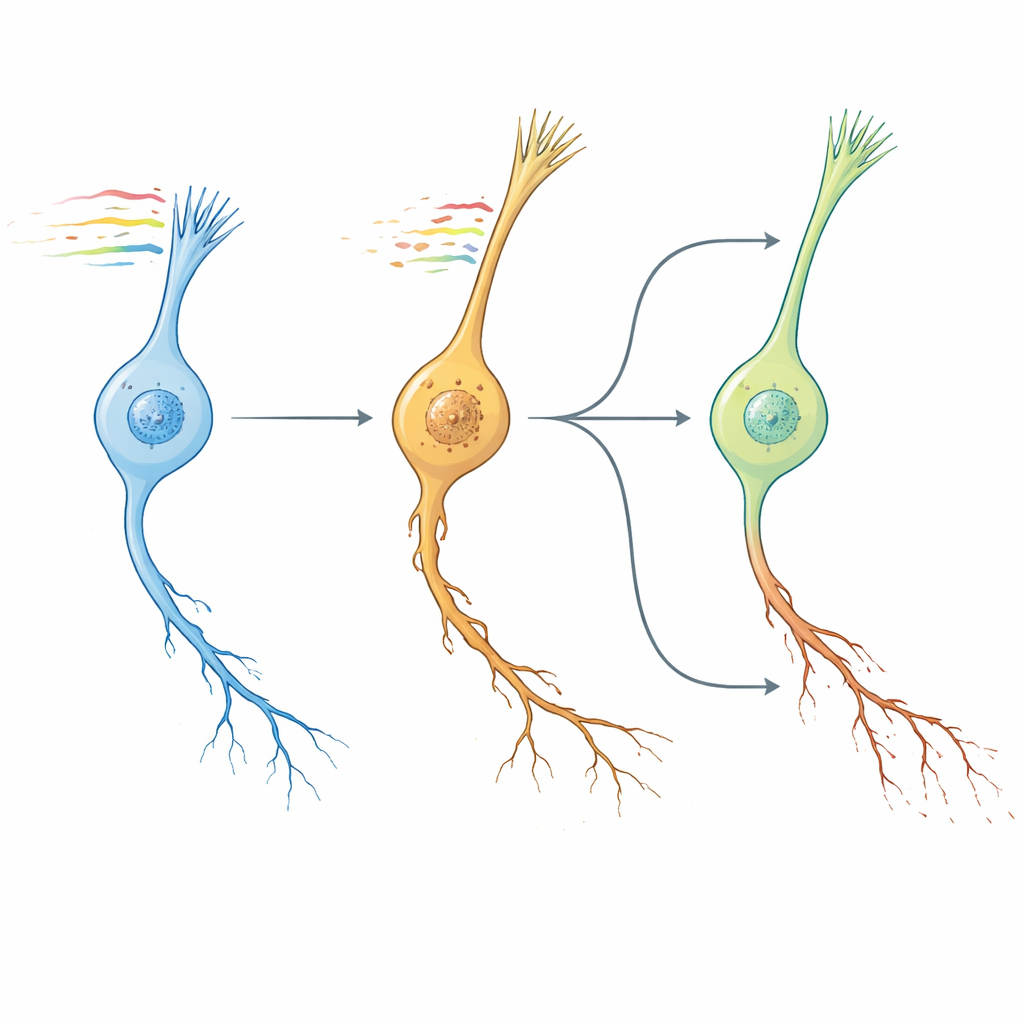
Maskklockor, mänskliga hjärnor och läkemedelsledtrådar
Nästa steg frågade författarna om deras mönster för neuronåldrande i masken liknade hjärnans åldrande hos däggdjur. Genom att jämföra väg-nivå förändringar över bevarade gener fann de att transcriptomiska ”NeuronAge”-signaturen i C. elegans klustrade tätt med åldringsbanor från flera mus- och mänskliga hjärnregioner, medan kända geroprotektiva interventioner — såsom unga blodfaktorer, motion och dietära föreningar — visade motsatta mönster. Med denna konservering i åtanke vände de sig till en stor human cellinje-resurs för att i silico söka efter små molekyler vars effekter motverkar eller efterliknar NeuronAge. Föreningar vars profiler motsatte sig NeuronAge flaggades som potentiella neurobeskyddare; de som förstärkte den som potentiella neurotoxiner. Experimentella tester i maskar validerade flera av förutsägelserna. Den växtbaserade metaboliten syringinsyra och läkemedlet vanoxerine minskade båda degeneration i snabbåldrande neuroner utan att skada unga, medan ämnen såsom Bay K8644 och WAY-100635 förvärrade neurit-skador och försämrade beteende. Till och med resveratrol, ofta framhållen som skyddande, framträdde som pro-åldrande i detta system och ökade neuronal patologi.
Vad detta betyder för hjärnhälsa
Sammanfattningsvis visar detta arbete att även inom ett enda nervsystem åldras olika neurontyper i olika takt, och att dessa interna klockor förutsäger vilka celler som först kommer att degenerera och förlora funktion. Sensoriska neuroner som är exponerade mot omvärlden och som har hög proteintillverkning framstår som särskilt sköra. Genom att koppla neuronspecifikt åldrande till bevarade genuttrycksvägar erbjuder studien ett sätt att översätta insikter från en enkel mask till människans hjärna. Lika viktigt visar den att transcriptomiska åldringssignaturer kan användas som ett kraftfullt filter för att identifiera molekyler som bromsar eller påskyndar neurodegeneration. Mycket återstår innan dessa kandidater kan övervägas för mänsklig terapi, men angreppssättet pekar mot en framtid där vi inte bara kan mäta den biologiska åldern hos individuella neurontyper, utan också rationellt utforma interventioner för att hålla dem yngre längre.
Citering: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Nyckelord: neuronal åldrande, neurodegeneration, proteinsyntes, Caenorhabditis elegans, neuroprotektion