Clear Sky Science · it
Gli orologi dell’invecchiamento delineano i tipi neuronali vulnerabili o resistenti alla neurodegenerazione e identificano interventi neuroprotettivi
Perché alcune cellule cerebrali invecchiano più in fretta di altre
Perché alcune cellule del cervello si deteriorano precocemente mentre altre restano robuste per decenni? Questa domanda è al centro di molti disturbi legati all’età, dall’Alzheimer al morbo di Parkinson. In questo studio, i ricercatori hanno utilizzato un piccolo verme tondo, Caenorhabditis elegans, il cui sistema nervoso è mappato cellula per cellula, per verificare se diversi tipi neuronali possiedono una propria “età biologica” e se tali età predicono quali cellule andranno incontro a degenerazione. Il loro lavoro non solo individua i tipi neuronali vulnerabili e un processo molecolare che accelera il loro declino, ma scopre anche piccole molecole che possono rallentare o accelerare l’invecchiamento neuronale — offrendo indizi che potrebbero estendersi al cervello umano.
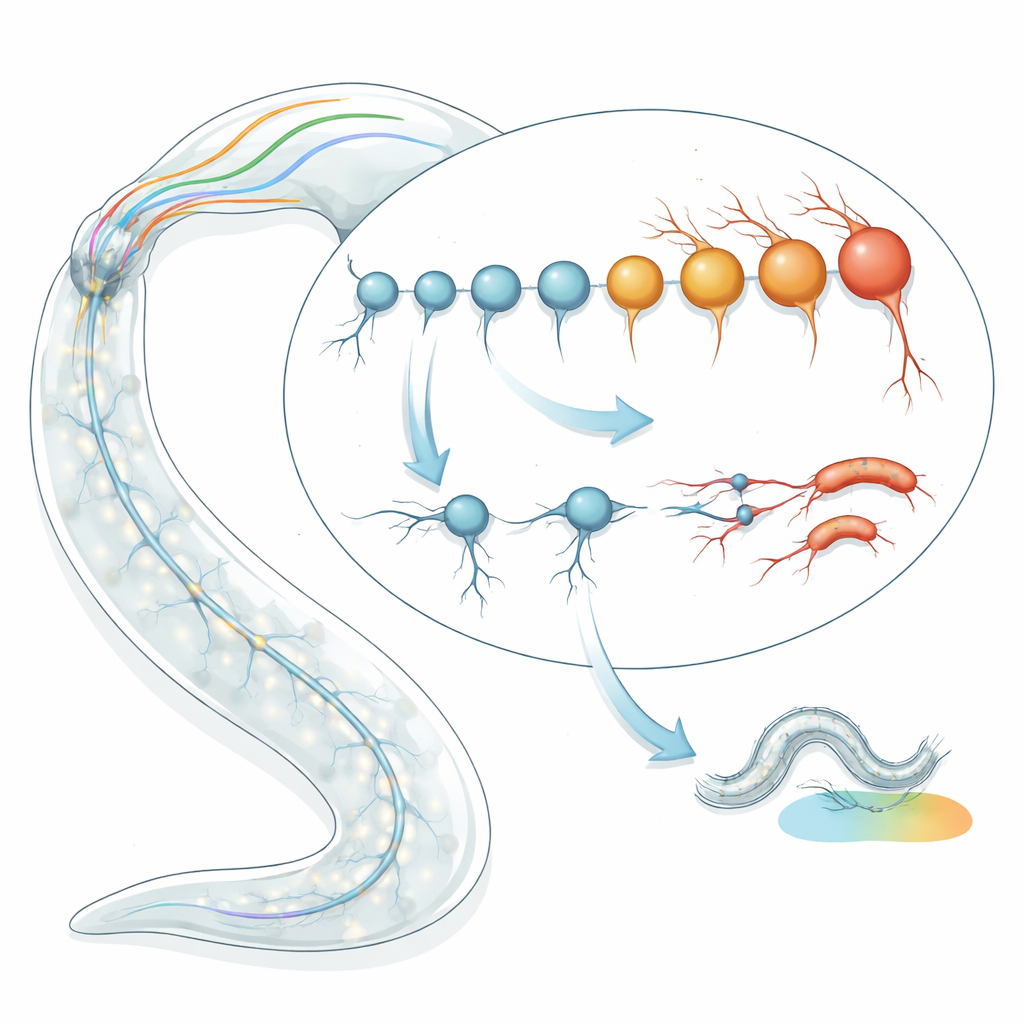
Misurare l’età delle singole cellule nervose
Il team ha iniziato applicando “orologi” trascrittomici dell’invecchiamento ai singoli tipi neuronali di C. elegans. Invece di guardare l’età del verme in giorni, hanno esaminato i modelli di attività genica per stimare l’età biologica di ciascun tipo cellulare. Utilizzando due modelli di orologio indipendenti — uno basato su firme geniche caratteristiche dell’invecchiamento e un altro che cattura come i cambiamenti casuali si accumulano nel tempo — hanno analizzato dati di RNA-seq per 128 tipi neuronali ben definiti in vermi allo stadio larvale tardivo e in giovani adulti. Con sorpresa, hanno trovato una dispersione di circa due- fino a quattro- volte nell’età biologica predetta tra neuroni tutti della stessa età cronologica. Alcuni neuroni apparivano molto più “giovani” del previsto, mentre altri sembravano prematuramente “vecchi”, e queste stime risultavano coerenti attraverso più set di dati e metodi di sequenziamento.
Dall’età molecolare a danni visibili e perdita di comportamento
Per verificare se queste previsioni di età avessero rilevanza nei vermi reali, i ricercatori hanno seguito nel tempo lo stato fisico di neuroni selezionati usando marcatori fluorescenti. I neuroni predetti giovani (come I2, OLL e PHC) mostravano solo lievi danni strutturali in una minoranza di animali con l’avanzare dell’età. In netto contrasto, neuroni predetti vecchi (inclusi ASI, ASJ e ASK) presentavano già segni di deterioramento in quasi metà dei larve tardivi, salendo a circa il 90% dopo una settimana di età adulta. Il danno si manifestava come piccole tumefazioni e escrescenze lungo le fibre nervose e aumentava in modo grossolanamente casuale lungo ogni neurite, coerente con un processo di invecchiamento stocastico piuttosto che con un programma di sviluppo fisso. Il declino strutturale precoce si traduceva anche in deficit comportamentali reali: in circuiti dove un singolo tipo neuronale controlla un compito specifico, la degenerazione di quel neurone corrispondeva strettamente a fallimenti nell’evitare patogeni o nell’apprendimento basato sul sale.
Perché i neuroni sensoriali esposti sono particolarmente a rischio
Mappare le stime di età biologica sull’intero connettoma nervoso del verme ha rivelato un pattern evidente. I neuroni più anziani si raggruppavano tra le cellule sensoriali ciliati nella testa, in particolare nelle cellule anfidiali i cui cigli sono direttamente esposti all’ambiente. Queste cellule rilevano sostanze chimiche, odori e altri segnali e sono ricche di neuropeptidi e recettori. Tra i diversi tipi neuronali, un numero maggiore di neuropeptidi e recettori espressi correla con un’età biologica più elevata, mentre il numero assoluto di sinapsi non lo fa. I neuroni ciliati i cui terminali sensoriali si protendono verso l’esterno erano i più invecchiati, suggerendo che sia l’esposizione ambientale sia un intenso carico di segnalazione possano predisporli a un declino precoce. Questo risuona con la neurologia umana, dove neuroni ciliati esposti, nel sistema olfattivo, sono tra i primi a degenerare nella malattia di Alzheimer.
La produzione proteica come motore — e leva — dell’invecchiamento
Per individuare i meccanismi alla base di queste differenze di età, il team ha raggruppato i neuroni per età biologica e ha esaminato i trend di espressione genica. Hanno trovato che processi legati alla biogenesi dei ribosomi, alla sintesi proteica e alla funzione nucleolare erano arricchiti nei neuroni più vecchi, insieme a cambiamenti nei geni di segnalazione sinaptica e dei neuropeptidi. Questo ha indicato un’elevata produzione proteica come possibile onere che accelera l’usura neuronale. I ricercatori hanno quindi testato una dose modestà di cicloeossipamide, un composto che rallenta parzialmente la traduzione. Nei neuroni a invecchiamento rapido, questa lieve inibizione ha ridotto significativamente i danni strutturali e preservato le prestazioni in un compito di apprendimento sul sale, con effetti protettivi che persistevano anche dopo la fine del trattamento. I neuroni a invecchiamento più lento, al contrario, sono rimasti per lo più invariati. Questi risultati collegano un alto carico traslazionale alla vulnerabilità specifica dei neuroni e mostrano che ridurre la sintesi proteica può ripristinare l’integrità strutturale e funzionale delle cellule a rischio.
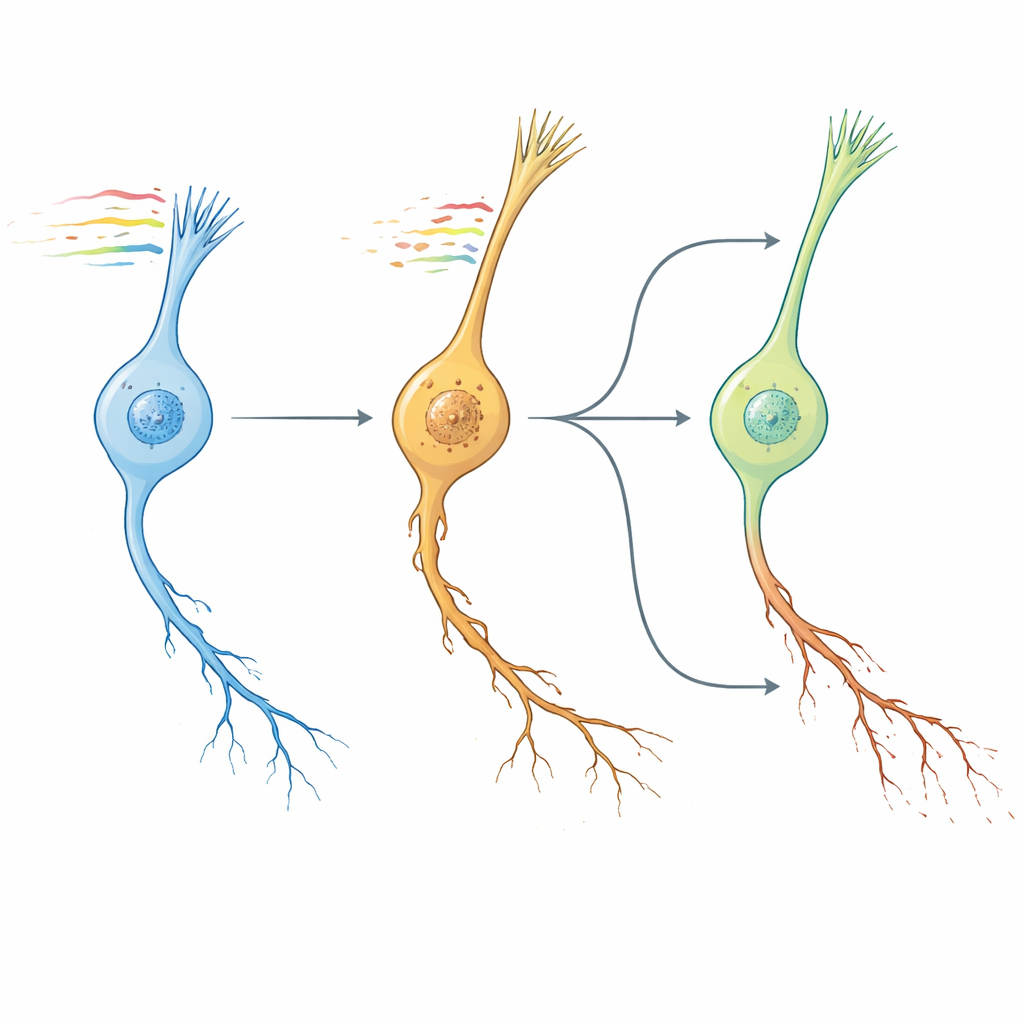
Orologi dei vermi, cervelli umani e piste per farmaci
Successivamente, gli autori si sono chiesti se il pattern di invecchiamento neuronale nel verme somigliasse all’invecchiamento cerebrale nei mammiferi. Confrontando i cambiamenti a livello di vie metaboliche tra geni conservati, hanno scoperto che la firma trascrittomica “NeuronAge” in C. elegans si raggruppava strettamente con le traiettorie di invecchiamento provenienti da più regioni del cervello di topo e umano, mentre interventi geroprotettivi noti — come fattori presenti nel sangue giovane, esercizio fisico e composti dietetici — mostravano pattern opposti. Sfruttando questa conservazione, si sono rivolti a una vasta risorsa di linee cellulari umane per cercare in silico piccole molecole i cui effetti contrastano o mimano NeuronAge. I composti i cui profili si opponevano a NeuronAge sono stati segnalati come potenziali neuroprotettori; quelli che lo rinforzavano come potenziali neurotossine. Test sperimentali nei vermi hanno validato diverse previsioni. Il metabolita di origine vegetale acido siringico e il farmaco vanoxerina hanno entrambi ridotto la degenerazione nei neuroni a rapido invecchiamento senza danneggiare quelli giovani, mentre agenti come Bay K8644 e WAY-100635 hanno esacerbato i danni ai neuriti e compromesso il comportamento. Perfino la resveratrolo, spesso pubblicizzata come protettiva, è emersa come pro-invecchiamento in questo sistema e ha aumentato la patologia neuronale.
Cosa significa per la salute del cervello
In sostanza, questo lavoro dimostra che anche all’interno di un singolo sistema nervoso, diversi tipi neuronali attraversano l’invecchiamento a velocità differenti e che questi orologi interni predicono quali cellule degenereranno e perderanno funzione prima. I neuroni sensoriali esposti al mondo esterno e con elevati livelli di produzione proteica appaiono particolarmente fragili. Collegando l’invecchiamento specifico dei neuroni a vie di espressione genica conservate, lo studio offre un modo per tradurre conoscenze da un verme semplice al cervello umano. Non meno importante, dimostra che le firme trascrittomiche dell’invecchiamento possono essere usate come filtro potente per identificare molecole che rallentano o accelerano la neurodegenerazione. Pur restando molto da fare prima che questi candidati possano essere considerati per terapie umane, l’approccio indica una prospettiva in cui non solo possiamo misurare l’età biologica di singoli tipi neuronali, ma anche progettare razionalmente interventi per mantenerli più giovani più a lungo.
Citazione: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Parole chiave: invecchiamento neuronale, neurodegenerazione, sintesi proteica, Caenorhabditis elegans, neuroprotezione