Clear Sky Science · ja
老化クロックは神経変性に脆弱または回復力のあるニューロン型を区別し、神経保護的介入を同定する
なぜある脳細胞は他より早く老いるのか
なぜ一部の脳細胞は若いうちに衰え、他は何十年も頑健でいられるのか?この問いはアルツハイマー病やパーキンソン病などの加齢性疾患の核心にある。本研究では、全神経系が細胞ごとにマッピングされている小さな線虫Caenorhabditis elegansを用い、異なるニューロン型がそれぞれ「生物学的年齢」を持ち、その年齢がどの細胞が変性するかを予測するかを検証した。研究は脆弱なニューロン型とそれらの衰弱を加速する分子過程を特定しただけでなく、ニューロンの老化を遅らせたり加速させたりする小分子も明らかにし、人間の脳にも応用可能な手がかりを示した。
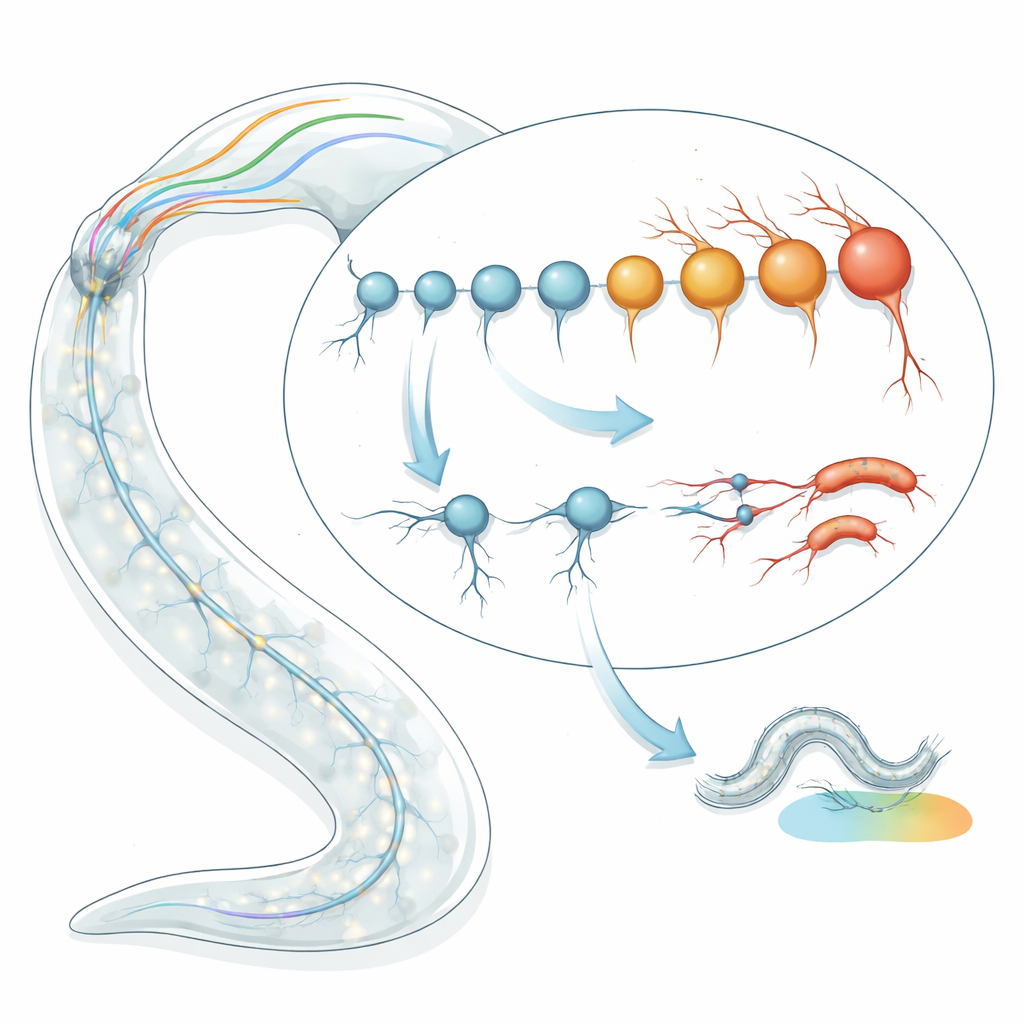
単一神経細胞の年齢を測る
研究チームはまず、トランスクリプトームに基づく「老化クロック」をC. elegansの個々のニューロン型に適用した。線虫の年齢を日数で見る代わりに、遺伝子発現パターンから各細胞型の生物学的年齢を推定した。特徴的な老化遺伝子シグネチャに基づくモデルと、時間とともに蓄積するランダムな変化を捉える別の独立したモデルという2つを用い、晩期幼虫と若い成体の128種類の明確に定義されたニューロン型のRNAシーケンスデータを解析した。驚くべきことに、同じ暦年齢のニューロン間で予測される生物学的年齢はほぼ2倍から4倍の幅があった。一部のニューロンは予想よりはるかに「若く」見え、他は早熟に「老いて」見え、これらの推定値は複数のデータセットとシーケンシング手法で一貫していた。
分子レベルの年齢から目に見える損傷と行動喪失へ
これらの年齢予測が実際の線虫で意味を持つかを確かめるため、研究者は蛍光マーカーを用いて選択したニューロンの物理的状態を時間を追って追跡した。生物学的に若いと予測されたニューロン(例えばI2、OLL、PHC)は、線虫の老化に伴ってごく一部の個体でのみ軽度の構造的損傷を示した。対照的に、老いていると予測されたニューロン(ASI、ASJ、ASKなど)は、晩期幼虫のほぼ半数で既に悪化の兆候を示し、成体1週間で約90%に達した。損傷は神経線維に沿った小さな腫れや突起として現れ、各軸索にほぼランダムに増加しており、これは固定された発生プログラムというより確率的な老化過程と一致する。初期の構造的衰退は実際の行動欠損にもつながった:特定の課題を単一のニューロン型が制御する回路では、そのニューロンの変性は病原体回避や塩に基づく学習の失敗と密接に一致した。
なぜ露出した感覚ニューロンは特に危険にさらされるのか
生物学的年齢の推定を線虫の全コネクトームにマッピングすると、顕著なパターンが現れた。最も老いたニューロンは頭部の繊毛を持つ感覚細胞に集まり、特に繊毛が外界に直接露出するアンフィドニューロンに集中していた。これらの細胞は化学物質や匂いなどの手がかりを検出し、神経ペプチドや受容体が豊富に備わっている。ニューロン型全体で、発現している神経ペプチドや受容体の数が多いほど生物学的年齢が高い相関が見られた一方で、シナプス数の単純な多さとは相関しなかった。感覚終末が外界に突出している繊毛ニューロンは最も老化が進んでおり、環境への暴露と高いシグナル負荷の両方が早期衰退を招く素因になっていることが示唆される。これは、人間の神経学でも、環境にさらされる嗅覚系の繊毛ニューロンがアルツハイマー病で最初に変性する例の一つであることと呼応する。
タンパク質生産は老化の駆動因子であり操作可能な取っ手である
これらの年齢差の背後にあるメカニズムを明らかにするために、チームはニューロンを生物学的年齢でグループ化し、遺伝子発現の傾向を調べた。リボソーム生合成、タンパク質合成、核小体機能に関連する過程が老いたニューロンで濃縮しており、シナプスおよび神経ペプチドのシグナル遺伝子の変化も見られた。これは、高いタンパク質生産がニューロンの摩耗を加速する負荷になりうることを示唆する。研究者らは次に、翻訳を部分的に遅らせる化合物であるシクロヘキシミドを穏やかな用量で試した。速く老いるニューロンでは、この穏やかな阻害が構造的損傷を有意に減らし、塩学習課題の成績を保護し、処置中止後も効果が持続した。一方、ゆっくり老いるニューロンはほとんど影響を受けなかった。これらの結果は、高い翻訳負荷がニューロン特異的脆弱性と関連し、タンパク質合成を抑えることで危険にさらされた細胞の構造的・機能的完全性を回復できることを示している。
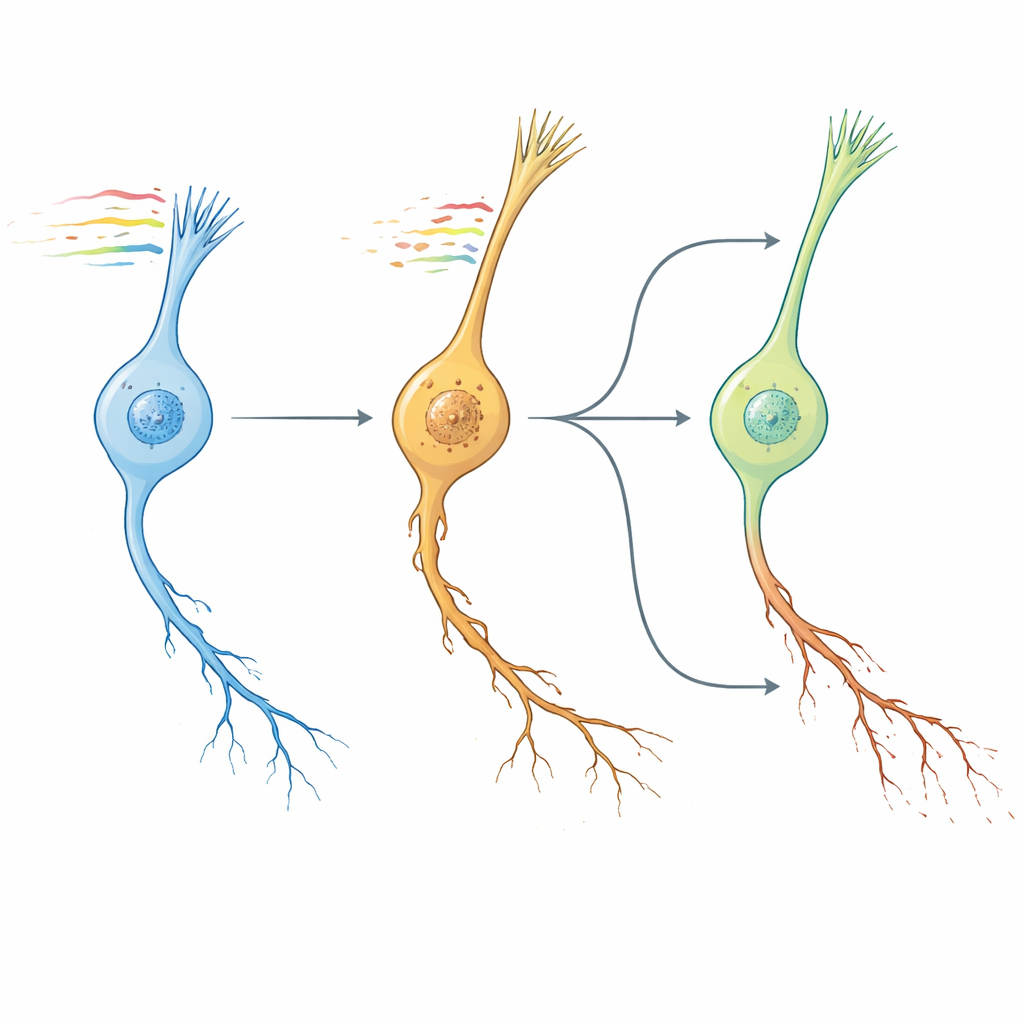
線虫のクロック、人間の脳、そして薬の候補
次に著者らは、線虫ニューロンの老化パターンが哺乳類の脳老化と類似しているかを問した。保存された遺伝子にわたる経路レベルの変化を比較すると、C. elegansのトランスクリプトミックな「NeuronAge」シグネチャは複数のマウスおよびヒトの脳領域の老化軌跡と密にクラスタリングし、若い血液因子、運動、食事由来化合物といった既知の長寿保護的介入は逆のパターンを示した。この保存性を利用して、彼らは大規模なヒト細胞株リソースを使い、Ne uronAge に拮抗または類似する小分子をインシリコで探索した。NeuronAge に反するプロファイルを持つ化合物は潜在的な神経保護剤として、これを強化するものは潜在的な神経毒として候補に挙げられた。線虫での実験的検証によりいくつかの予測が実証された。植物由来代謝物シリンギン酸(syringic acid)と薬物バノキセリン(vanoxerine)は速く老いるニューロンの変性を減らし、若いニューロンを傷つけなかった。一方、Bay K8644やWAY-100635といった薬剤は軸索損傷を悪化させ行動を損なった。しばしば保護的とされるレスベラトロールでさえ、本系では老化促進的に働き、ニューロン病理を増加させた。
脳の健康にとっての意味
要するに、この研究は単一の神経系内でさえ異なるニューロン型が異なる速度で老化を進め、その内部クロックがどの細胞が最初に変性して機能を失うかを予測することを示している。外界に面し高いタンパク質生産を行う感覚ニューロンは特に脆弱であるようだ。ニューロン特異的な老化を保存された遺伝子発現経路に結び付けることで、この研究は単純な線虫からヒト脳へと知見を翻訳する道筋を提供する。それと同時に、トランスクリプトミクスに基づく老化シグネチャが、神経変性を遅らせたり促進したりする分子を同定する強力なフィルターとして機能することを示している。これらの候補がヒト治療に用いられるまでにはまだ多くの課題が残るが、このアプローチは個々のニューロン型の生物学的年齢を測定し、それらをより長く若く保つための介入を合理的に設計する将来を示唆している。
引用: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
キーワード: ニューロンの老化, 神経変性, タンパク質合成, Caenorhabditis elegans, 神経保護