Clear Sky Science · pt
Relógios de envelhecimento delineiam tipos de neurônios vulneráveis ou resilientes à neurodegeneração e identificam intervenções neuroprotetoras
Por que algumas células cerebrais envelhecem mais rápido que outras
Por que algumas células do cérebro murcham cedo na vida enquanto outras permanecem robustas por décadas? Essa pergunta está no cerne de muitos transtornos do envelhecimento, do Alzheimer ao Parkinson. Neste estudo, os pesquisadores usaram um pequeno nematoide, Caenorhabditis elegans, cujo sistema nervoso inteiro é mapeado célula a célula, para investigar se tipos diferentes de neurônios têm suas próprias “idades biológicas” e se essas idades preveem quais células irão degenerar. O trabalho não apenas identifica tipos de neurônios vulneráveis e um processo molecular que acelera seu declínio, mas também revela pequenas moléculas que podem desacelerar ou acelerar o envelhecimento neuronal — oferecendo pistas que podem se estender ao cérebro humano.
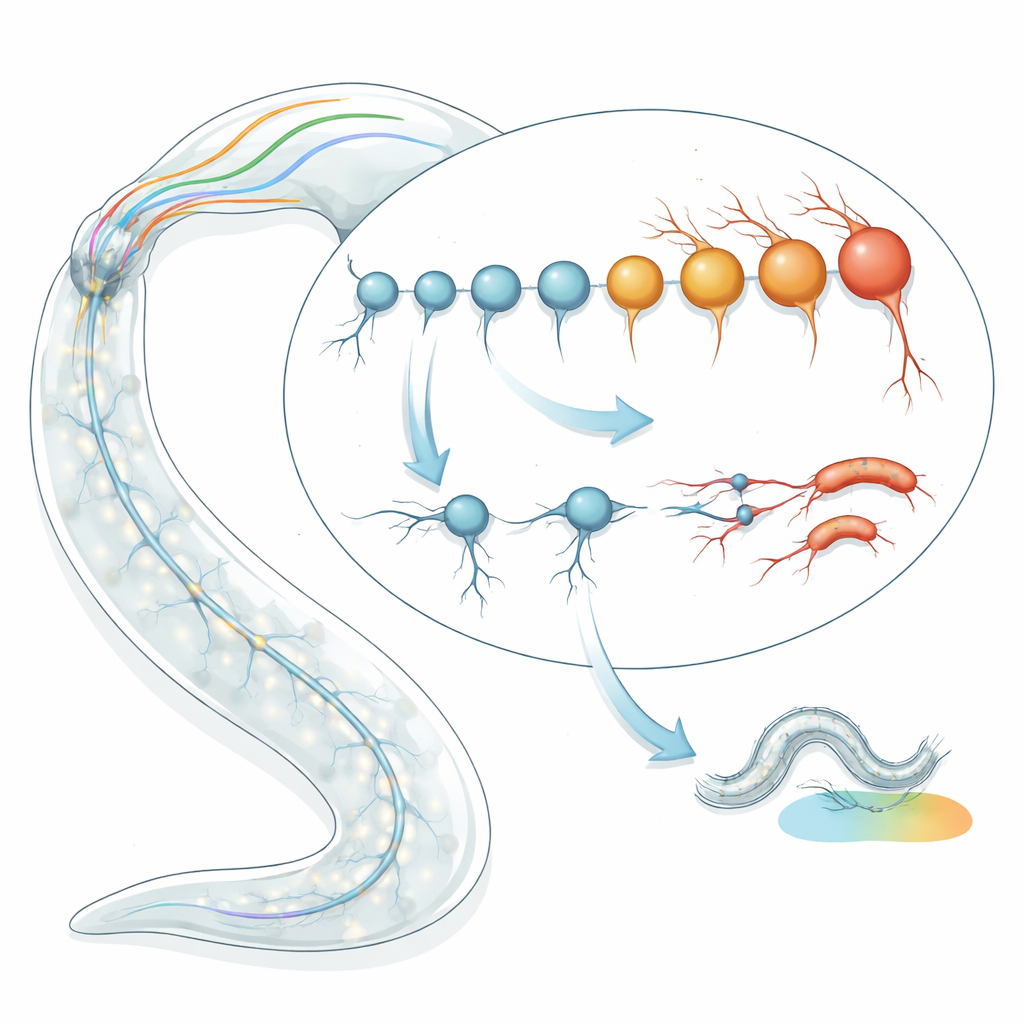
Medindo a idade de nervos celulares individuais
A equipe começou aplicando “relógios” transcriptômicos de envelhecimento a tipos neuronais individuais em C. elegans. Em vez de olhar para a idade do verme em dias, examinaram padrões de atividade gênica para estimar a idade biológica de cada tipo celular. Usando dois modelos de relógio independentes — um baseado em assinaturas gênicas características do envelhecimento e outro que captura como mudanças aleatórias se acumulam ao longo do tempo — analisaram dados de sequenciamento de RNA de 128 tipos neuronais bem definidos em larvas tardias e vermes adultos jovens. Surpreendentemente, encontraram uma variação de aproximadamente duas a quatro vezes na idade biológica prevista entre neurônios que tinham a mesma idade cronológica. Alguns neurônios pareceram muito “mais jovens” do que o esperado, enquanto outros pareceram prematuramente “velhos”, e essas estimativas foram consistentes em múltiplos conjuntos de dados e métodos de sequenciamento.
Da idade molecular ao dano visível e à perda de comportamento
Para testar se essas previsões de idade importavam em vermes reais, os pesquisadores acompanharam a condição física de neurônios selecionados ao longo do tempo usando marcadores fluorescentes. Neurônios previstos como biologicamente jovens (como I2, OLL e PHC) apresentaram apenas danos estruturais leves em uma minoria de animais à medida que os vermes envelheciam. Em contraste marcante, neurônios previstos como velhos (incluindo ASI, ASJ e ASK) já mostravam sinais de deterioração em quase metade das larvas tardias, subindo para cerca de 90% após uma semana de vida adulta. O dano apareceu como pequenas dilatações e brotos ao longo das fibras nervosas e aumentou de forma aproximadamente aleatória ao longo de cada neurita, consistente com um processo de envelhecimento estocástico em vez de um programa de desenvolvimento fixo. O declínio estrutural precoce também se traduziu em déficits comportamentais reais: em circuitos onde um único tipo de neurônio controla uma tarefa específica, a degeneração daquele neurônio coincidiu estreitamente com falhas na evitação de patógenos ou no aprendizado baseado em sal.
Por que neurônios sensoriais expostos correm mais risco
Mapear as estimativas de idade biológica no conectoma completo do sistema nervoso do verme revelou um padrão marcante. Os neurônios mais velhos se concentraram entre células sensoriais ciliadas na cabeça, especialmente neurônios das amfídeas cujos cílios estão diretamente expostos ao ambiente. Essas células detectam substâncias químicas, odores e outros sinais e são ricamente providas de neuropeptídeos e receptores. Entre os tipos neuronais, um maior número de neuropeptídeos e receptores expressos correlacionou-se com idade biológica mais avançada, enquanto o número bruto de sinapses não o fez. Neurônios ciliados cujos terminais sensoriais se projetam para o mundo exterior eram os mais envelhecidos, sugerindo que tanto a exposição ambiental quanto cargas elevadas de sinalização podem predispor esses neurônios ao declínio precoce. Isso ecoa a neurologia humana, onde neurônios ciliados expostos ao ambiente no sistema olfativo estão entre os primeiros a degenerar na doença de Alzheimer.
Produção de proteínas como motor — e alavanca — do envelhecimento
Para descobrir mecanismos por trás dessas diferenças de idade, a equipe agrupou neurônios por idade biológica e examinou tendências de expressão gênica. Encontraram que processos relacionados à biogênese de ribossomos, síntese proteica e função nucleolar estavam enriquecidos em neurônios mais velhos, junto com alterações em genes de sinalização sináptica e de neuropeptídeos. Isso apontou para a alta produção de proteínas como um possível fardo que acelera o desgaste neuronal. Os pesquisadores então testaram uma dose modesta de cicloeximida, um composto que retarda parcialmente a tradução. Em neurônios que envelhecem rápido, essa inibição suave reduziu significativamente o dano estrutural e preservou o desempenho em uma tarefa de aprendizado com sal, com efeitos protetores que persistiram mesmo após a interrupção do tratamento. Neurônios que envelhecem mais devagar, por outro lado, foram em grande parte não afetados. Esses resultados vinculam alta carga translacional à vulnerabilidade específica de certos neurônios e mostram que reduzir a síntese proteica pode restaurar a integridade estrutural e funcional em células em risco.
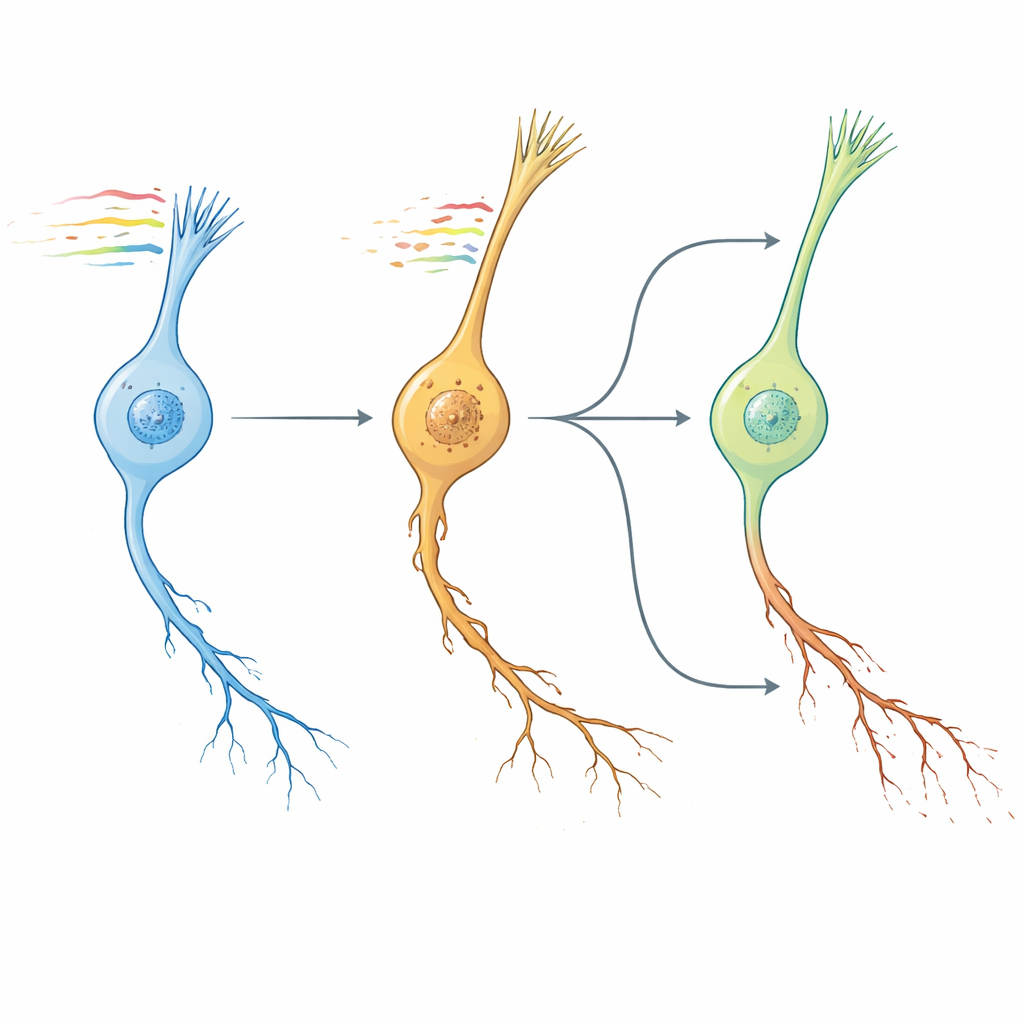
Relógios de verme, cérebros humanos e pistas para fármacos
Em seguida, os autores questionaram se o padrão de envelhecimento neuronal observado no verme se assemelhava ao envelhecimento cerebral em mamíferos. Ao comparar mudanças em nível de vias entre genes conservados, descobriram que a assinatura transcriptômica “NeuronAge” em C. elegans se agrupou de forma estreita com trajetórias de envelhecimento de múltiplas regiões do cérebro de camundongos e humanos, enquanto intervenções geroprotetoras conhecidas — como fatores presentes no sangue jovem, exercício e compostos dietéticos — mostraram padrões opostos. Aproveitando essa conservação, recorreram a um grande recurso de linhagens celulares humanas para buscar in silico pequenas moléculas cujos efeitos contrariassem ou imitassem o NeuronAge. Compostos cujos perfis se opunham ao NeuronAge foram sinalizados como potenciais neuroprotetores; aqueles que o reforçavam, como potenciais neurotoxinas. Testes experimentais em vermes validaram várias previsões. O metabólito de origem vegetal ácido siringico e o fármaco vanoxerina reduziram ambos a degeneração em neurônios de envelhecimento rápido sem prejudicar os neurônios jovens, enquanto agentes como Bay K8644 e WAY-100635 exacerbaram danos aos neuritos e prejudicaram o comportamento. Mesmo a resveratrol, frequentemente divulgada como protetora, emergiu como pró-envelhecimento neste sistema e aumentou a patologia neuronal.
O que isso significa para a saúde cerebral
Em essência, este trabalho mostra que mesmo dentro de um único sistema nervoso, diferentes tipos neuronais atravessam o envelhecimento em velocidades distintas, e que esses relógios internos preveem quais células irão degenerar e perder função primeiro. Neurônios sensoriais que enfrentam o mundo exterior e mantêm altos níveis de produção proteica parecem especialmente frágeis. Ao vincular o envelhecimento específico de neurônios a vias de expressão gênica conservadas, o estudo oferece uma forma de traduzir insights de um verme simples para o cérebro humano. Igualmente importante, demonstra que assinaturas transcriptômicas de envelhecimento podem ser usadas como um filtro poderoso para identificar moléculas que desaceleram ou aceleram a neurodegeneração. Embora ainda muito reste fazer antes que esses candidatos possam ser considerados para terapia humana, a abordagem aponta para um futuro em que não apenas poderemos medir a idade biológica de tipos neuronais individuais, mas também projetar intervenções racionais para mantê-los mais jovens por mais tempo.
Citação: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Palavras-chave: envelhecimento neuronal, neurodegeneração, síntese proteica, Caenorhabditis elegans, neoproteção