Clear Sky Science · pl
Zegary starzenia wyodrębniają typy neuronów podatne lub odporne na neurodegenerację i identyfikują interwencje neuroprotekcyjne
Dlaczego niektóre komórki mózgu starzeją się szybciej niż inne
Dlaczego niektóre komórki mózgu więdną wcześnie, podczas gdy inne pozostają odporne przez dziesięciolecia? To pytanie leży u podstaw wielu chorób związanych ze starzeniem się, od choroby Alzheimera po Parkinsona. W tym badaniu naukowcy użyli maleńkiego nicienia Caenorhabditis elegans, którego cały układ nerwowy jest zmapowany komórka po komórce, aby sprawdzić, czy różne typy neuronów mają własne „wiek biologiczny” i czy te wieki przewidują, które komórki ulegną degeneracji. Ich praca nie tylko wskazuje na podatne typy neuronów i proces molekularny przyspieszający ich pogorszenie, lecz także ujawnia małe molekuły, które mogą spowalniać lub przyspieszać starzenie neuronów — dając wskazówki, które mogą mieć znaczenie także dla mózgu człowieka.
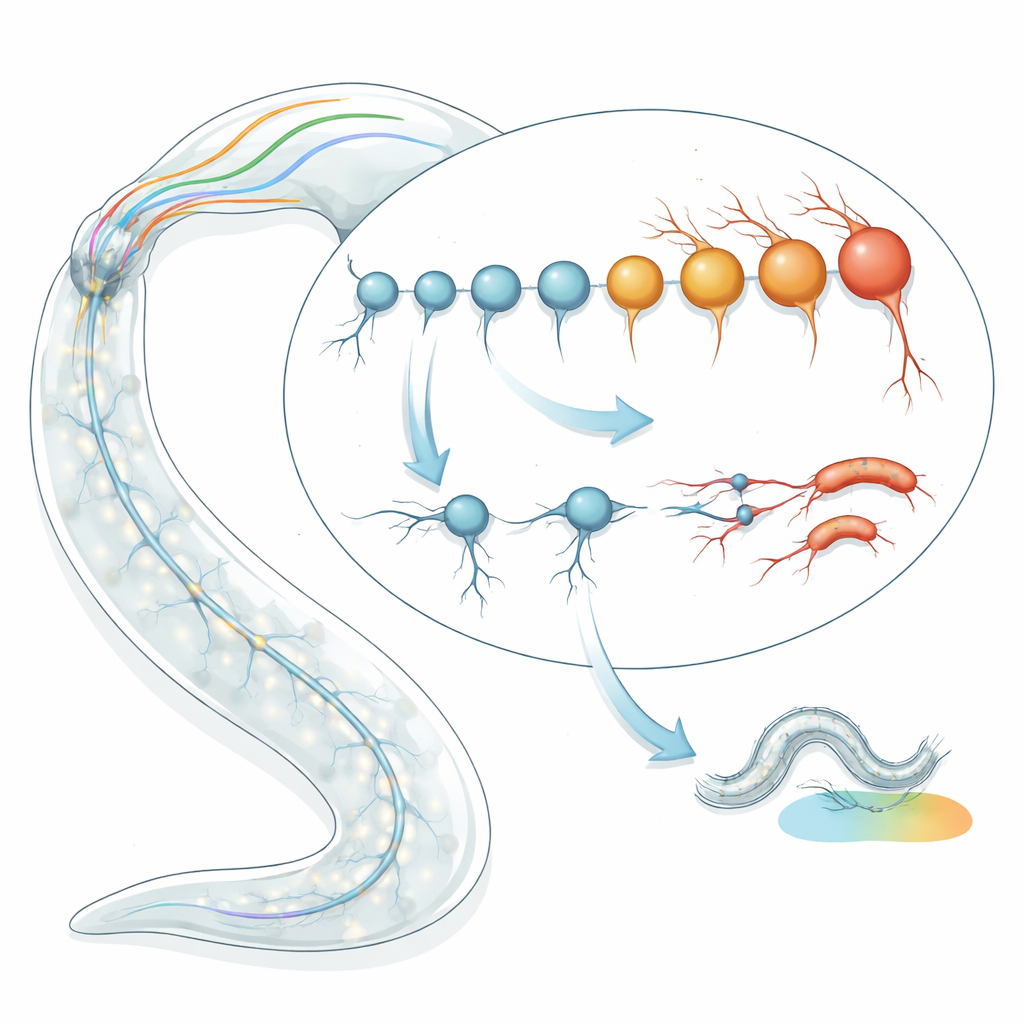
Mierzenie wieku pojedynczych komórek nerwowych
Zespół rozpoczął od zastosowania transkryptomicznych „zegarków starzenia” do poszczególnych typów neuronów u C. elegans. Zamiast patrzeć na wiek nicienia w dniach, analizowali wzorce aktywności genów, by oszacować wiek biologiczny każdego typu komórki. Korzystając z dwóch niezależnych modeli zegara — jednego opartego na charakterystycznych sygnaturach genów starzenia i drugiego, który wychwytuje, jak losowe zmiany kumulują się w czasie — przeanalizowali dane sekwencjonowania RNA dla 128 dobrze zdefiniowanych typów neuronów w późnych stadiach larwalnych i młodych dorosłych osobnikach. Co zaskakujące, znaleźli niemal dwukrotne do czterokrotnego rozpiętość w przewidywanym wieku biologicznym między neuronami o tym samym wieku chronologicznym. Niektóre neurony wydawały się znacznie „młodsze” niż oczekiwano, inne zaś przedwcześnie „starsze”, a te oszacowania były spójne w różnych zestawach danych i metodach sekwencjonowania.
Od wieku molekularnego do widocznych uszkodzeń i utraty zachowań
Aby sprawdzić, czy te prognozy wieku mają znaczenie w żywych robakach, badacze śledzili stan wybranych neuronów w czasie, używając znaczników fluorescencyjnych. Neurony przewidywane jako biologicznie młode (takie jak I2, OLL i PHC) wykazywały tylko łagodne uszkodzenia strukturalne u niewielkiej części osobników w miarę starzenia się robaków. W ostrym kontraście, neurony przewidywane jako stare (w tym ASI, ASJ i ASK) już w późnych stadiach larwalnych wykazywały oznaki pogorszenia u niemal połowy osobników, a odsetek ten wzrastał do około 90% w ciągu tygodnia dorosłości. Uszkodzenia manifestowały się jako drobne zgrubienia i wyrostki wzdłuż włókien nerwowych i pojawiały się mniej więcej losowo wzdłuż każdego neuritu, co jest zgodne z procesem starzenia o charakterze stochastycznym, a nie z ustalonym programem rozwojowym. Wczesne pogorszenie strukturalne przekładało się również na realne deficyty behawioralne: w obwodach, w których pojedynczy typ neuronu kontroluje konkretną funkcję, degeneracja tego neuronu ściśle korelowała z porażkami w unikaniu patogenów lub w uczeniu się opartego na soli.
Dlaczego odsłonięte neurony sensoryczne są szczególnie narażone
Mapowanie oszacowań wieku biologicznego na pełny konektom układu nerwowego robaka ujawniło uderzający wzorzec. Najstarsze neurony skupiały się wśród rzęskowych komórek sensorycznych w głowie, zwłaszcza neuronów amfidialnych, których rzęski są bezpośrednio wystawione na środowisko. Te komórki wykrywają związki chemiczne, zapachy i inne sygnały oraz obfitują w neuropeptydy i receptory. Wśród typów neuronów większa liczba ekspresjonowanych neuropeptydów i receptorów korelowała ze starszym wiekiem biologicznym, podczas gdy sama liczba synaps nie miała takiego związku. Neurony rzęskowe, których zakończenia sensoryczne wystają na zewnątrz, były najbardziej „zestarzałe”, co sugeruje, że zarówno narażenie na środowisko, jak i duże obciążenie sygnalizacyjne mogą predysponować je do wczesnego pogorszenia. To koresponduje z neurologią człowieka, gdzie neurony rzęskowe w systemie węchowym, narażone na środowisko, należą do pierwszych ulegających degeneracji w chorobie Alzheimera.
Produkcja białek jako czynnik napędzający — i punkt uchwytu — starzenia
Aby odkryć mechanizmy leżące u podstaw różnic wieku, zespół pogrupował neurony według wieku biologicznego i przeanalizował trendy ekspresji genów. Stwierdzili, że procesy związane z biogenezą rybosomów, syntezą białek i funkcją jąderka były wzbogacone w starszych neuronach, wraz ze zmianami w genach związanych z sygnalizacją synaptyczną i neuropeptydową. Wskazywało to na intensywną produkcję białek jako potencjalne obciążenie przyspieszające zużycie neuronów. Badacze przetestowali następnie umiarkowaną dawkę cykloheksymidu, związku, który częściowo spowalnia translację. W neuronach szybko się starzejących to łagodne zahamowanie znacząco zmniejszyło uszkodzenia strukturalne i zachowało wydajność w zadaniu uczenia się o soli, przy efektach ochronnych utrzymujących się nawet po zaprzestaniu leczenia. Neurony wolniej się starzejące były natomiast w dużej mierze niezmienione. Wyniki te łączą duże obciążenie translacyjne z podatnością specyficzną dla typów neuronów i pokazują, że przykręcenie syntezy białek może przywrócić integralność strukturalną i funkcjonalną komórek zagrożonych.
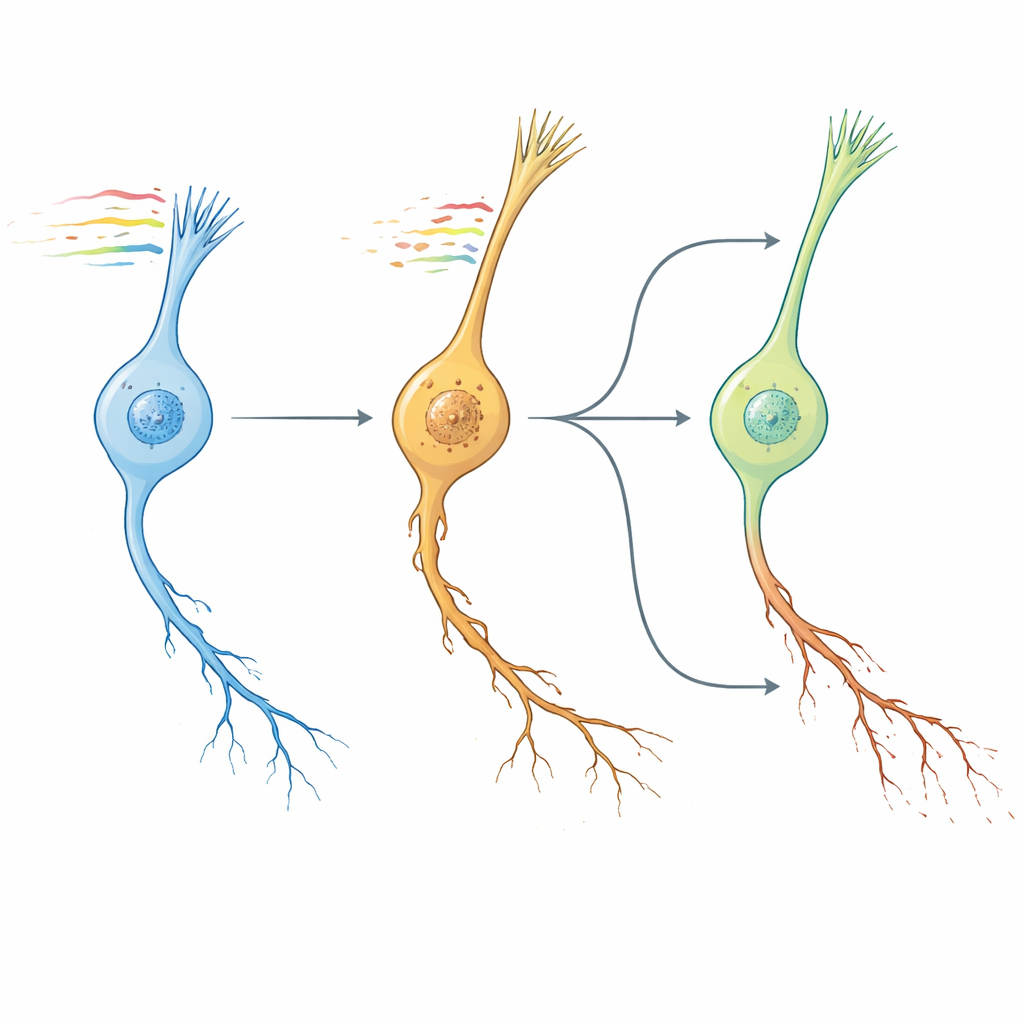
Zegary robaków, mózgi ludzi i kandydaci na leki
Następnie autorzy zapytali, czy wzorzec starzenia neuronów u robaka przypomina starzenie mózgu ssaków. Porównując zmiany na poziomie szlaków w zachowanych genach, odkryli, że transkryptomiczna sygnatura „NeuronAge” u C. elegans silnie grupowała się z trajektoriami starzenia z różnych regionów mózgów myszy i człowieka, podczas gdy znane interwencje geroprotekcyjne — takie jak młoda krew, ćwiczenia i związki dietetyczne — wykazywały przeciwstawne wzorce. Wykorzystując tę konserwację, sięgnęli do dużego zasobu linii komórkowych ludzkich, by in silico poszukać małych molekuł, których efekty przeciwdziałają lub naśladują NeuronAge. Związki, których profile przeciwstawiały się NeuronAge, zostały oznaczone jako potencjalne neuroprotektory; te, które go wzmacniały, jako potencjalne neurotoksyny. Testy eksperymentalne na robakach potwierdziły kilka przewidywań. Metabolit roślinny kwas syringowy i lek vanoxerine oba zmniejszały degenerację w szybko starzejących się neuronach, nie szkodząc młodszym, podczas gdy środki takie jak Bay K8644 i WAY-100635 nasilały uszkodzenia neuritów i pogarszały zachowanie. Nawet resweratrol, często przedstawiany jako ochronny, w tym układzie okazał się pro‑starzeniowy i zwiększał patologię neuronalną.
Co to oznacza dla zdrowia mózgu
W istocie ta praca pokazuje, że nawet w obrębie jednego układu nerwowego różne typy neuronów starzeją się w różnym tempie, a te wewnętrzne zegary przewidują, które komórki ulegną degeneracji i utracą funkcję jako pierwsze. Neurony sensoryczne narażone na środowisko i prowadzące wysoką aktywność produkcyjną białek wydają się szczególnie kruche. Powiązanie starzenia specyficznego dla neuronów z zachowanymi szlakami ekspresji genów daje sposób na przetłumaczenie wniosków z prostego robaka na mózg ludzki. Co równie ważne, pokazuje, że transkryptomiczne sygnatury starzenia mogą służyć jako potężny filtr do identyfikacji molekuł, które spowalniają lub przyspieszają neurodegenerację. Chociaż przed rozważeniem tych kandydatów do terapii u ludzi wciąż wiele pracy, podejście to wskazuje drogę ku przyszłości, w której nie tylko będziemy mierzyć wiek biologiczny poszczególnych typów neuronów, lecz także projektować interwencje, które utrzymają je młodszymi na dłużej.
Cytowanie: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Słowa kluczowe: starzenie neuronów, neurodegeneracja, synteza białek, Caenorhabditis elegans, neoprotekcja