Clear Sky Science · es
Los relojes del envejecimiento delimitan tipos neuronales vulnerables o resistentes a la neurodegeneración e identifican intervenciones neuroprotectoras
Por qué algunas células cerebrales envejecen más rápido que otras
¿Por qué algunas células cerebrales se marchitan temprano en la vida mientras otras se mantienen robustas durante décadas? Esta pregunta está en el núcleo de muchos trastornos del envejecimiento, desde el alzhéimer hasta el párkinson. En este estudio, los investigadores utilizaron un pequeño gusano redondo, Caenorhabditis elegans, cuyo sistema nervioso completo está mapeado célula por célula, para preguntar si distintos tipos neuronales tienen su propia “edad biológica” y si esas edades predicen qué células degenerarán. Su trabajo no solo identifica tipos neuronales vulnerables y un proceso molecular que acelera su declive, sino que también revela pequeñas moléculas que pueden ralentizar o acelerar el envejecimiento neuronal, ofreciendo pistas que podrían extenderse al cerebro humano.
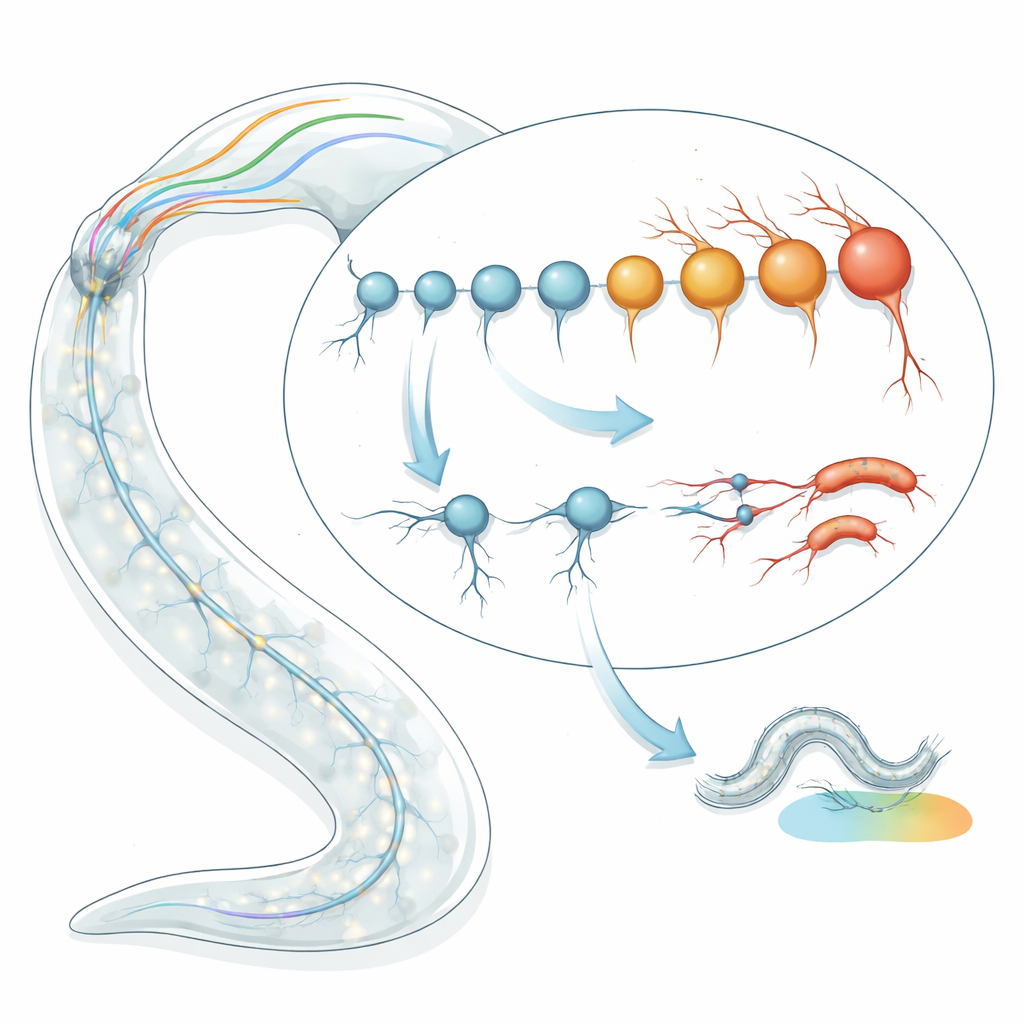
Temporizar la edad de células nerviosas individuales
El equipo comenzó aplicando “relojes” transcriptómicos del envejecimiento a tipos neuronales individuales en C. elegans. En lugar de observar la edad del gusano en días, examinaron patrones de actividad génica para estimar la edad biológica de cada tipo celular. Utilizando dos modelos de reloj independientes —uno basado en firmas génicas características del envejecimiento y otro que captura cómo se acumulan cambios aleatorios con el tiempo— analizaron datos de secuenciación de ARN para 128 tipos neuronales bien definidos en larvas tardías y gusanos adultos jóvenes. Sorprendentemente, encontraron una variación de casi dos a cuatro veces en la edad biológica predicha entre neuronas que tenían la misma edad cronológica. Algunas neuronas parecían mucho más “jóvenes” de lo esperado, mientras que otras mostraban un envejecimiento prematuro, y estas estimaciones fueron coherentes a través de múltiples conjuntos de datos y métodos de secuenciación.
De la edad molecular al daño visible y la pérdida de conducta
Para probar si estas predicciones de edad importaban en gusanos reales, los investigadores siguieron la condición física de neuronas seleccionadas a lo largo del tiempo usando marcadores fluorescentes. Las neuronas predichas como biológicamente jóvenes (como I2, OLL y PHC) mostraron solo daños estructurales leves en una minoría de animales a medida que los gusanos envejecían. En marcado contraste, las neuronas predichas como viejas (incluidas ASI, ASJ y ASK) ya mostraban signos de deterioro en casi la mitad de las larvas tardías, aumentando hasta alrededor del 90 % en la primera semana de adultez. El daño se manifestaba como pequeñas hinchazones y crecimientos a lo largo de las fibras nerviosas, y aumentaba de forma aproximadamente aleatoria a lo largo de cada neurita, consistente con un proceso de envejecimiento estocástico más que con un programa de desarrollo fijo. El declive estructural temprano también se tradujo en déficits conductuales reales: en circuitos donde un único tipo neuronal controla una tarea específica, la degeneración de esa neurona se correspondía estrechamente con fallos en la evitación de patógenos o en el aprendizaje basado en sal.
Por qué las neuronas sensoriales expuestas tienen un riesgo especial
Mapear las estimaciones de edad biológica en el conectoma completo del sistema nervioso del gusano reveló un patrón llamativo. Las neuronas más viejas se agruparon entre las células sensoriales ciliadas en la cabeza, especialmente las neuronas amfídicas cuyas cilias están directamente expuestas al entorno. Estas células detectan químicos, olores y otras señales y están dotadas de numerosos neuropéptidos y receptores. Entre los tipos neuronales, un mayor número de neuropéptidos y receptores expresados se correlacionó con una edad biológica mayor, mientras que el mero número de sinapsis no lo hizo. Las neuronas ciliadas cuyas terminaciones sensoriales protruyen hacia el exterior del cuerpo fueron las más envejecidas, lo que sugiere que tanto la exposición ambiental como las altas cargas de señalización pueden predisponerlas a un declive temprano. Esto recuerda a la neurología humana, donde neuronas ciliadas expuestas al ambiente en el sistema olfativo están entre las primeras en degenerar en la enfermedad de Alzheimer.
La producción de proteínas como motor —y como diana— del envejecimiento
Para descubrir los mecanismos detrás de estas diferencias de edad, el equipo agrupó neuronas según su edad biológica y examinó tendencias en la expresión génica. Encontraron que procesos relacionados con la biogénesis de ribosomas, la síntesis de proteínas y la función nucleolar estaban enriquecidos en neuronas más viejas, junto con cambios en genes de señalización sináptica y de neuropéptidos. Esto apuntó a una elevada producción de proteínas como una carga posible que acelera el desgaste neuronal. Los investigadores probaron entonces una dosis modesta de cicloheximida, un compuesto que ralentiza parcialmente la traducción. En neuronas de envejecimiento rápido, esta inhibición suave redujo significativamente el daño estructural y preservó el rendimiento en una tarea de aprendizaje con sal, con efectos protectores que persistieron incluso después de suspender el tratamiento. Las neuronas de envejecimiento más lento, en cambio, se vieron en gran medida no afectadas. Estos resultados vinculan la alta carga traduccional con la vulnerabilidad específica de ciertas neuronas y muestran que reducir la síntesis de proteínas puede restaurar la integridad estructural y funcional en células en riesgo.
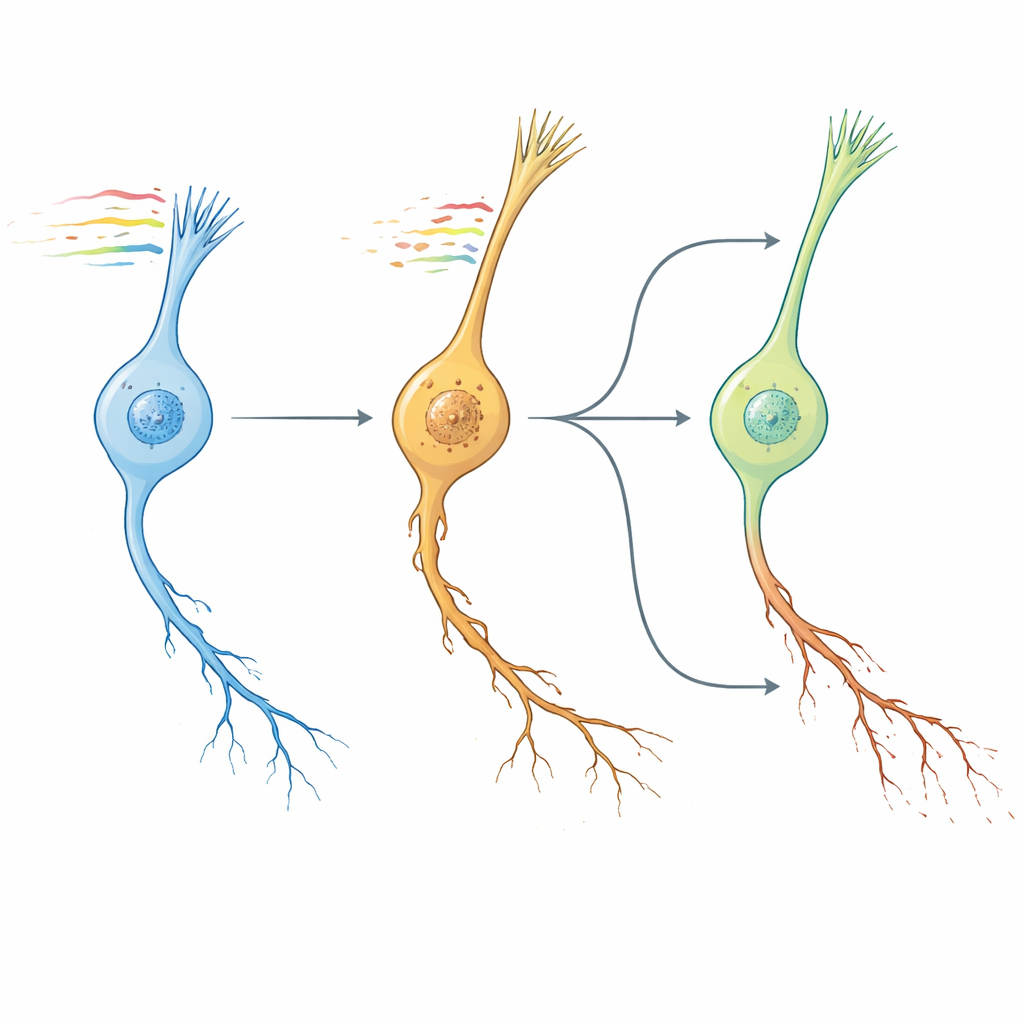
Relojes en gusanos, cerebros humanos y candidatos farmacológicos
A continuación, los autores se preguntaron si el patrón de envejecimiento neuronal en gusanos se parecía al envejecimiento cerebral en mamíferos. Al comparar cambios a nivel de vías entre genes conservados, encontraron que la firma transcriptómica “NeuronAge” en C. elegans se agrupaba estrechamente con trayectorias de envejecimiento de múltiples regiones cerebrales de ratón y humano, mientras que intervenciones geroprotectoras conocidas —como factores de sangre joven, ejercicio y compuestos dietéticos— mostraban patrones opuestos. Aprovechando esta conservación, recurrieron a un gran recurso de líneas celulares humanas para buscar in silico pequeñas moléculas cuyos efectos contrarrestaran o imitaran NeuronAge. Los compuestos cuyos perfiles se oponían a NeuronAge fueron señalados como potenciales neuroprotectores; los que lo reforzaban, como potenciales neurotoxinas. Pruebas experimentales en gusanos validaron varias predicciones. El metabolito de origen vegetal ácido siringico y el fármaco vanoxerina redujeron la degeneración en neuronas de envejecimiento rápido sin dañar a las jóvenes, mientras que agentes como Bay K8644 y WAY-100635 exacerbaron el daño de las neuritas e impidieron el comportamiento. Incluso la resveratrol, a menudo promocionada como protectora, resultó ser pro-envejecimiento en este sistema e incrementó la patología neuronal.
Qué significa esto para la salud cerebral
En esencia, este trabajo muestra que incluso dentro de un único sistema nervioso, distintos tipos neuronales avanzan en el envejecimiento a ritmos diferentes, y que estos relojes internos predicen qué células degenerarán y perderán función primero. Las neuronas sensoriales que están expuestas al mundo exterior y mantienen altos niveles de producción proteica parecen especialmente frágiles. Al vincular el envejecimiento específico de neuronas con vías de expresión génica conservadas, el estudio ofrece una vía para trasladar conocimientos de un gusano simple al cerebro humano. Igual de importante, demuestra que las firmas transcriptómicas del envejecimiento pueden usarse como un filtro potente para identificar moléculas que ralentizan o aceleran la neurodegeneración. Aunque queda mucho por hacer antes de que estos candidatos puedan considerarse para terapia humana, el enfoque apunta hacia un futuro en el que no solo podamos medir la edad biológica de tipos neuronales individuales, sino también diseñar de forma racional intervenciones para mantenerlos más jóvenes por más tiempo.
Cita: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Palabras clave: envejecimiento neuronal, neurodegeneración, síntesis de proteínas, Caenorhabditis elegans, neprotección