Clear Sky Science · he
שעוני ההזדקנות מפרידים סוגי נוירונים הפגיעים או החסינים לנוירודגנרציה ומזהים התערבויות נוירופרוטקטיביות
מדוע תאי מוח מסוימים מזדקנים מהר יותר מאחרים
מדוע תאים מסוימים במוח נובלים מוקדם בחיים בעוד שאחרים שומרים על עמידות למשך עשורים? שאלה זו עומדת בלבן של מחלות רבות הקשורות להזדקנות, מאלצהיימר ועד פרקינסון. במחקר זה השתמשו החוקרים בתולעת קטנה עגולה, Caenorhabditis elegans, שמערכת העצבים כולה ממופה בה תאם לתא, כדי לבדוק האם סוגי נוירונים שונים בעלי "גיל ביולוגי" משלהם והאם גיל זה מנבא אילו תאים יתנו מענה לנוירודגנרציה. עבודתם לא רק מזהה סוגי נוירונים פגיעים ותהליך מולקולרי שמאיץ את התדרדרותם, אלא גם חושפת מולקולות קטנות שיכולות להאט או להאיץ את הזדקנות הנוירונים — ומספקת רמזים שעשויים לחול גם על המוח האנושי.
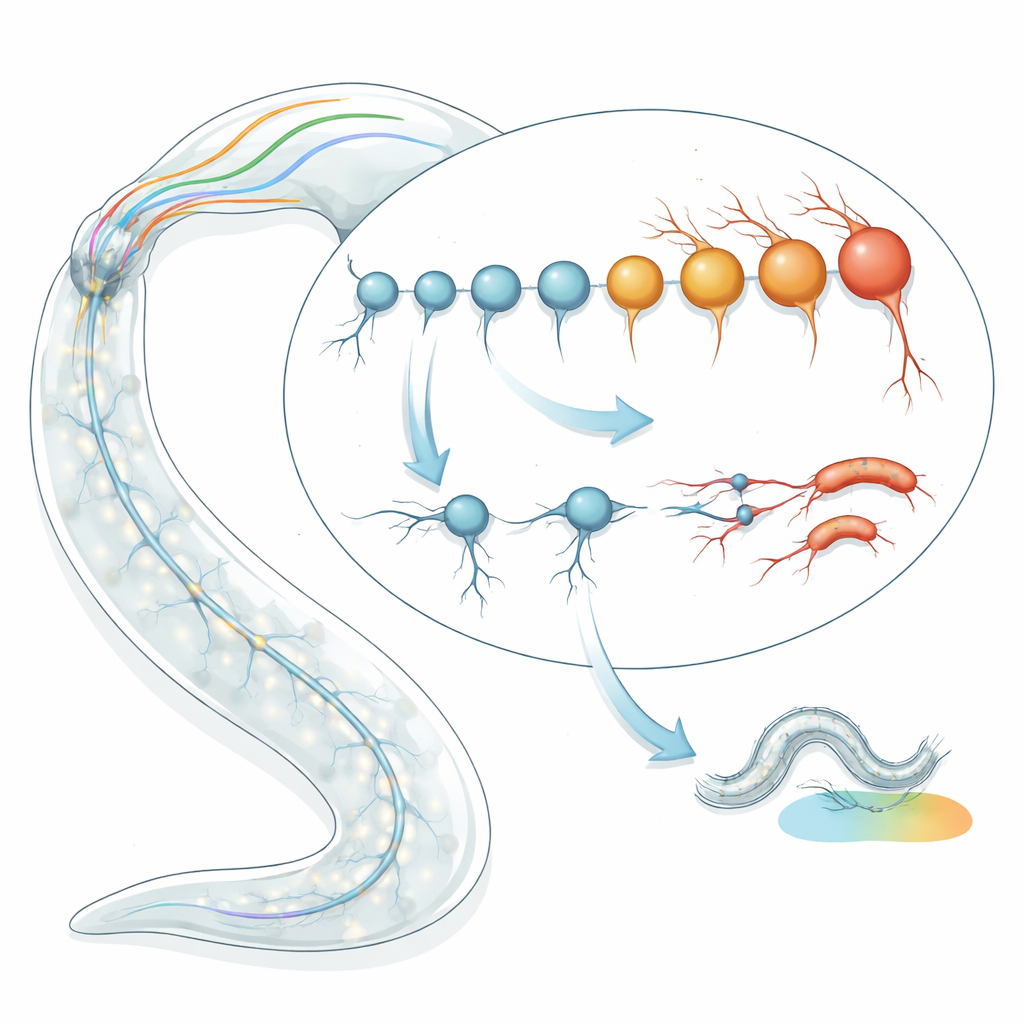
תזמון גילם של תאי עצב בודדים
הצוות החל ביישום "שעוני" הזדקנות טרנסקריפטומיים על סוגי הנוירונים הבודדים ב‑C. elegans. במקום לבחון את גיל התולעת בימים, הם ניתחו דפוסי ביטוי גנים כדי לאמוד את הגיל הביולוגי של כל סוג תא. באמצעות שני מודלי שעון עצמאיים — אחד המבוסס על חתימות גנטיות טיפוסיות של הזדקנות ואחר שמלכד כיצד שינויים אקראיים מצטברים לאורך זמן — הם ניתחו נתוני ריצוף RNA עבור 128 סוגי נוירונים מוגדרים היטב בעכבישונים מאוחרים ובתולעים בוגרות צעירות. באופן מפתיע הם מצאו פיזור של פי שניים עד ארבעה בגיל הביולוגי המוערך בין נוירונים על אף שהיה להם אותו גיל כרונולוגי. חלק מהנוירונים הופיעו "צעירים" באופן מובהק ביחס לציפייה, בעוד שאחרים נראו "זקנים" לפני זמנם, וההערכות הללו היו עקביות לאורך מספר מערכי נתונים ושיטות ריצוף.
מגיל מולקולרי לנזק נראה ולעיכוב התנהגותי
כדי לבדוק האם תחזיות הגיל הללו חשובות בתולעים אמיתיות, עקבו החוקרים לאורך זמן אחר מצבם הפיזי של נוירונים נבחרים באמצעות סמנים פלואורסצנטיים. נוירונים שחזו להם גיל ביולוגי צעיר (כגון I2, OLL ו‑PHC) הראו נזק מבני קל בקבוצה קטנה של פרטים כאשר התולעים הזדקנו. בניגוד מוחלט, נוירונים שחזו להם גיל ביולוגי מבוגר (כולל ASI, ASJ ו‑ASK) כבר הראו סימני הידרדרות בכמעט מחצית העכבישונים המאוחרים, וקצב זה עלה לכ‑90% בשבוע המבוגר. הנזק הופיע כבצקות זעירות והתארגויות לאורך הסיבים העצביים והתגבר באופן שנראה רנדומלי לאורך כל נויריט, תואם לתהליך הזדקנות סטוכסטי ולא לתוכנית התפתחותית תקנית. דעיכה מבנית מוקדמת זו תורגמה גם לפגמים התנהגותיים ממשיים: במעגלים שבהם סוג נוירון בודד שולט במשימה מסוימת, הדגנרציה של אותו נוירון התאימה באופן הדוק לכישלונות במניעת פתוגנים או בלמידה מבוססת מלח.
מדוע נוירונים חושיים חשופים בסיכון מיוחד
מיפוי הערכות הגיל הביולוגי על קונקטום מערכת העצבים המלא של התולעת חשף דפוס בולט. הנוירונים המזדקנים ביותר התקבצו בתאים חושיים מסוככים (ciliated) בראש, במיוחד נוירוני האמפיד שהזימים שלהם חשופים ישירות לסביבה. תאים אלה מזהים חומרים כימיים, ריחות ורמזים נוספים ועשירים בניורופפטידים וקולטנים. בין סוגי הנוירונים, מספר גדול יותר של נאורופפטידים וביטוי קולטנים נקשרו לגיל ביולוגי מבוגר יותר, בעוד שמספר הסינפסות כשלעצמו לא היה קשור. נוירונים מסוככים שהסיומות החושיות שלהם בולטות החוצה לעולם החיצון היו המבוגרים ביותר, מה שמרמז ששילוב של חשיפה סביבתית ועומס איתות גבוה עלול להטות אותם לדהייה מוקדמת. זה מהדהד נירולוגיה אנושית, שבה נוירונים מסוככים וחושיים במערכת הריח הם בין הראשונים להידרדר במחלת אלצהיימר.
ייצור חלבון כמניע — וכאמצעי לתמרון ההזדקנות
כדי לגלות מנגנונים מאחורי הבדלים אלה בגיל, קיבצו החוקרים נוירונים לפי גיל ביולוגי ובחנו מגמות ביטוי גנים. הם מצאו שתהליכים הקשורים לביוגנזה של ריבוזומים, סינתזת חלבון ותפקוד הגרעינון היו מועשרים בנוירונים מבוגרים יותר, לצד שינויים בגנים הקשורים לסינפטיקה ולאיתות נאורופפטידי. הממצא הזה הצביע על עומס גבוה של ייצור חלבון כאפשרות שמאיצה בלאי נוירונלי. החוקרים בדקו אז מנה מתונה של ציקלוהקסימיד, תרכובת שעושה האטה חלקית בתרגום. בנוירונים המזדקנים במהירות, עיכוב עדין זה הפחית משמעותית את הנזק המבני ושמר על ביצועים במטלת למידה מבוססת מלח, וההשפעות המגנות נמשכו גם לאחר הפסקת הטיפול. נוירונים המזדקנים לאט יותר, לעומת זאת, הושפעו במידה מועטה. תוצאות אלה מקשרות עומס תרגום גבוה לפגיעות ספציפית לנוירון ומראות כי הורדת סינתזת החלבון יכולה לשחזר שלמות מבנית ותפקודית בתאים בסיכון.
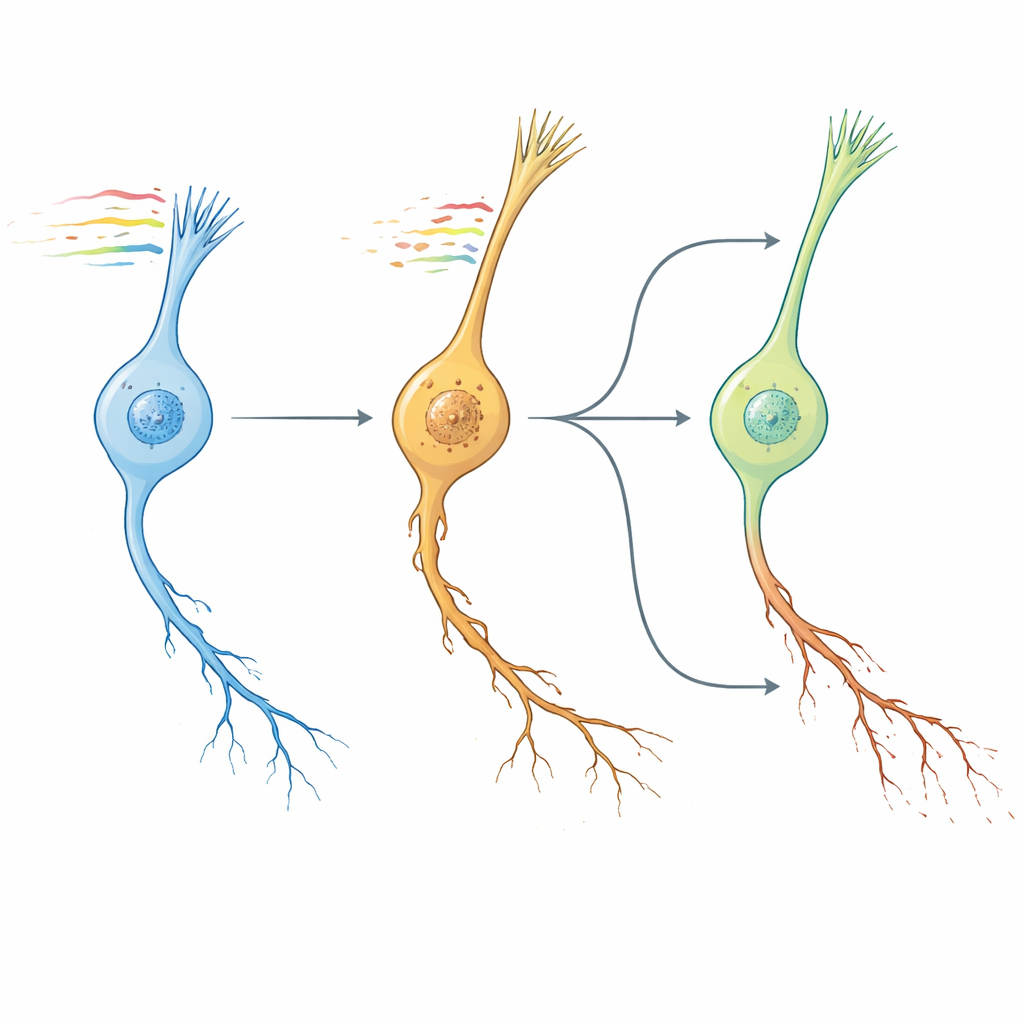
שעוני תולעת, מוח אנושי ומולקולות מובילות
בהמשך שאלו המחברים האם דפוס הזדקנות הנוירון שהתגלגל בתולעת דומה להזדקנות המוח ביונקים. בהשוואה של שינויים ברמת מסלולים בגנים משומרים, הם מצאו שחתימת ה‑"NeuronAge" הטרנסקריפטומית ב‑C. elegans התקבצה באופן הדוק עם מסלולי הזדקנות ממספר אזורי מוח בעכבר ובאדם, בעוד שהתערבויות גרופרוטקטיביות ידועות — כגון גורמים שנמצאים בדם צעיר, פעילות גופנית ותרכובות תזונתיות — הראו דפוסים מנוגדים. בהסתמך על השימור הזה, פנו למשאב גדול של קווי תאים אנושיים כדי לחפש בצורה חישובית מולקולות קטנות שהשפעתן מנוגדת או מחקה את NeuronAge. תרכובות שהפרופילים שלהן עמדו נגד NeuronAge סומנו כפוטנציאליות לנוירו‑מגנות; אלו שהחיזקו אותה סומנו כטוקסיות אפשריות. ניסויים בתולעים אישרו מספר תחזיות. המטבוליט הצמחי סירינגין וחומר התרופה וונוקסרין הפחיתו דגנרציה בנוירונים המזדקנים במהירות מבלי להזיק לצעירים, בעוד סוכנים כגון Bay K8644 ו‑WAY‑100635 החמירו נזק נויריטי ופגעו בהתנהגות. אפילו רזברטרול, שלעתים קרובות מתואר כמגן, התגלה במערכת זו כמעודד הזדקנות והגביר פתולוגיה נוירונלית.
מה המשמעות עבורך ועבור בריאות המוח
בעיקרון, עבודה זו מראה שגם בתוך מערכת עצבים בודדת, סוגי נוירונים שונים מזדקנים בקצבים שונים, ושהשעונים הפנימיים הללו מנבאים אילו תאים יידרדרו ויאבדו תפקוד ראשונים. תאי חוש המתמודדים עם העולם החיצוני ומפעילים רמות גבוהות של ייצור חלבון נראים פגיעים במיוחד. באמצעות קישור הזדקנות ספציפית לנוירון למסלולי ביטוי גנים ששמורים בין המינים, המחקר מציע דרך לתרגם תובנות מתולעת פשוטה אל המוח האנושי. ובאותה מידה, הוא מדגים שחתימות הזדקנות טרנסקריפטומיות יכולות לשמש כמסננת חזקה לזיהוי מולקולות שמאטות או מהירות נוירודגנרציה. למרות שנותרו צעדים רבים לפני שהמועמדות הללו תיחשבנה לטיפול אנושי, הגישה מצביעה על עתיד שבו נוכל לא רק למדוד את הגיל הביולוגי של סוגי נוירונים בודדים, אלא גם לעצב התערבויות בצורה רציונלית כדי לשמור עליהם צעירים לאורך זמן רב יותר.
ציטוט: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
מילות מפתח: הזדקנות נוירונאלית, נוירודגנרציה, סינתזת חלבון, Caenorhabditis elegans, נוירו‑הגנה