Clear Sky Science · ru
Часы старения выявляют типы нейронов, уязвимые или устойчивые к нейродегенерации, и определяют нейропротективные вмешательства
Почему некоторые клетки мозга стареют быстрее других
Почему одни клетки мозга увядают рано, тогда как другие остаются стойкими десятилетиями? Этот вопрос лежит в основе многих возрастных расстройств, от болезни Альцгеймера до болезни Паркинсона. В этом исследовании учёные использовали крошечного круглого червя Caenorhabditis elegans, у которого вся нервная система картирована поклеточно, чтобы выяснить, имеют ли разные типы нейронов свои «биологические возрасты» и предсказывают ли эти возрасты, какие клетки будут дегенерировать. Их работа не только локализует уязвимые типы нейронов и молекулярный процесс, ускоряющий их упадок, но и выявляет малые молекулы, которые могут замедлять или ускорять старение нейронов — давая подсказки, которые могут быть применимы и к человеческому мозгу.
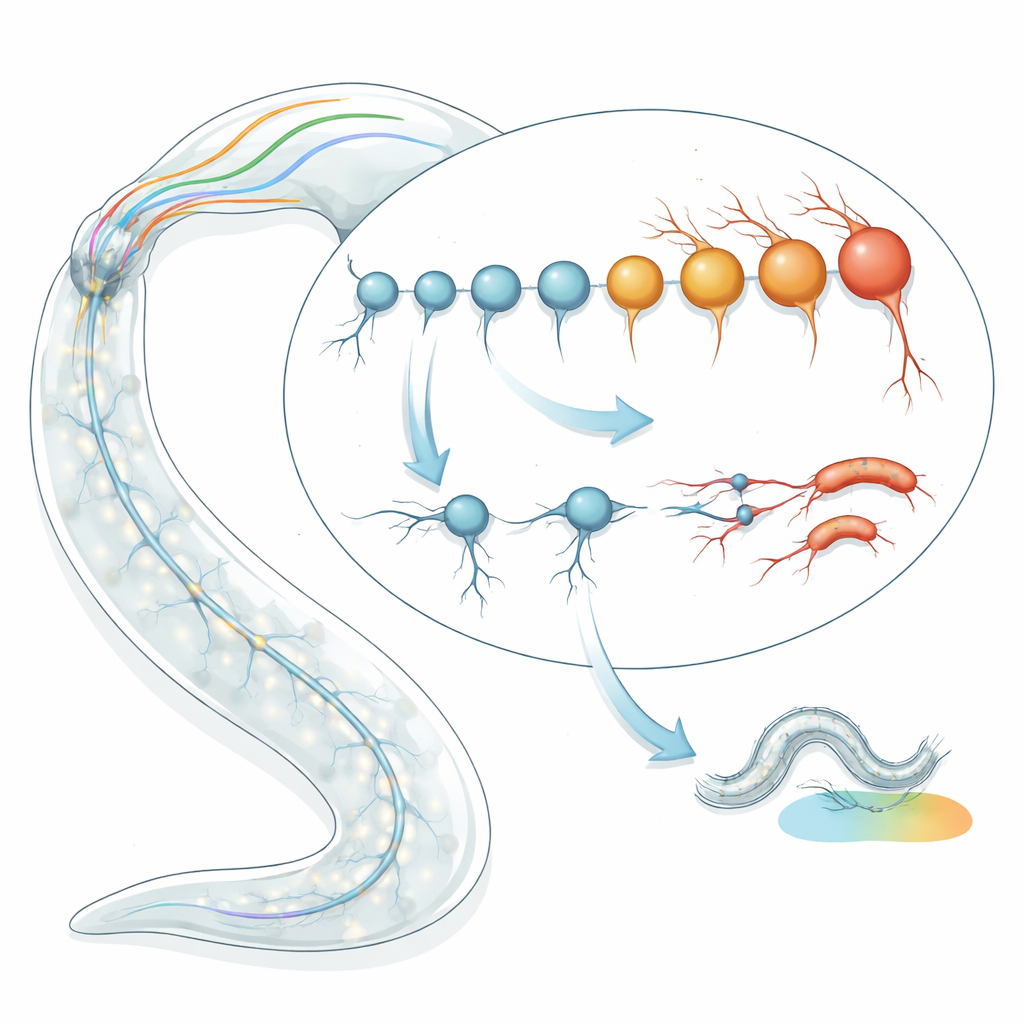
Определение возраста отдельных нервных клеток
Команда начала с применения транскриптомных «часов старения» к отдельным типам нейронов у C. elegans. Вместо того чтобы смотреть на возраст червя в днях, они анализировали схемы активности генов, чтобы оценить биологический возраст каждого типа клеток. Используя две независимые модели часов — одну, основанную на характерных сигнатурах старения генов, и другую, отражающую накопление стохастических изменений со временем — исследователи проанализировали данные РНК‑секвенирования для 128 хорошо определённых типов нейронов в поздних личиночных и молодых взрослых стадиях. Удивительно, но они обнаружили почти двух- до четырёхкратный разброс в предсказанном биологическом возрасте среди нейронов, равных по хронологическому возрасту. Некоторые нейроны выглядели намного «моложе», чем ожидалось, тогда как другие казались преждевременно «старыми», и эти оценки были согласованы в нескольких наборах данных и методах секвенирования.
От молекулярного возраста к видимым повреждениям и утрате поведения
Чтобы проверить, имеют ли эти возрастные предсказания значение в реальных червях, исследователи отслеживали физическое состояние выбранных нейронов с течением времени с помощью флуоресцентных маркеров. Нейроны, предсказанные как биологически молодые (например, I2, OLL и PHC), демонстрировали лишь небольшие структурные повреждения у меньшинства животных по мере старения. В резком контрасте нейроны, предсказанные как старые (включая ASI, ASJ и ASK), уже показывали признаки ухудшения почти у половины поздних личинок, достигая примерно 90% к неделе взрослой жизни. Повреждения проявлялись в виде крошечных вздутий и отростков вдоль нервных волокон и появлялись примерно случайным образом вдоль каждого нейрита, что согласуется со стохастическим процессом старения, а не с фиксированной программой развития. Раннее структурное ухудшение также выражалось в реальных поведенческих дефицитах: в цепях, где один тип нейронов контролирует конкретную задачу, дегенерация этого нейрона чётко коррелировала с нарушениями избегания патогенов или обучением, основанным на соли.
Почему подвергшиеся воздействию сенсорные нейроны особенно уязвимы
Наложение оценок биологического возраста на полностью картированную коннектому нервной системы червя выявило поразительную закономерность. Самые старые нейроны концентрировались среди ресничных сенсорных клеток в голове, особенно среди амфидных нейронов, чьи реснички непосредственно контактируют с окружающей средой. Эти клетки обнаруживают химические вещества, запахи и другие сигналы и богаты нейропептидами и рецепторами. По типам нейронов большее число экспрессируемых нейропептидов и рецепторов коррелировало с более старым биологическим возрастом, в то время как простое количество синапсов не коррелировало. Ресничные нейроны, чьи сенсорные окончания выступают наружу, оказывались наиболее возрастными, что указывает на то, что как воздействие среды, так и высокая нагрузка сигнальной активности могут предрасполагать их к раннему упадку. Это отзывается в человеческой неврологии: ресничные нейроны обонятельной системы, подвергающиеся внешнему воздействию, входят в число первых, которые дегенерируют при болезни Альцгеймера.
Синтез белка как движущая сила — и точка воздействия — старения
Чтобы раскрыть механизмы, лежащие в основе этих возрастных различий, команда сгруппировала нейроны по биологическому возрасту и проанализировала тенденции экспрессии генов. Они обнаружили, что процессы, связанные с биогенезом рибосом, синтезом белка и функцией нуклеолуса, были обогащены в стареющих нейронах, наряду с изменениями в генах синаптической и нейропептидной сигнализации. Это указало на высокую продукцию белка как возможное бремя, ускоряющее износ нейронов. Затем исследователи протестировали умеренную дозу хлоргидина/циклоэхимида (cycloheximide), соединения, частично замедляющего трансляцию. В быстро стареющих нейронах такое мягкое подавление заметно уменьшало структурные повреждения и сохраняло выполнение задачи по обучению на соли, причём защитные эффекты сохранялись даже после прекращения лечения. Нейроны с более медленным старением, напротив, в основном не реагировали. Эти результаты связывают высокую трансляционную нагрузку с нейронно-специфической уязвимостью и показывают, что снижение синтеза белка может восстановить структурную и функциональную целостность находящихся под риском клеток.
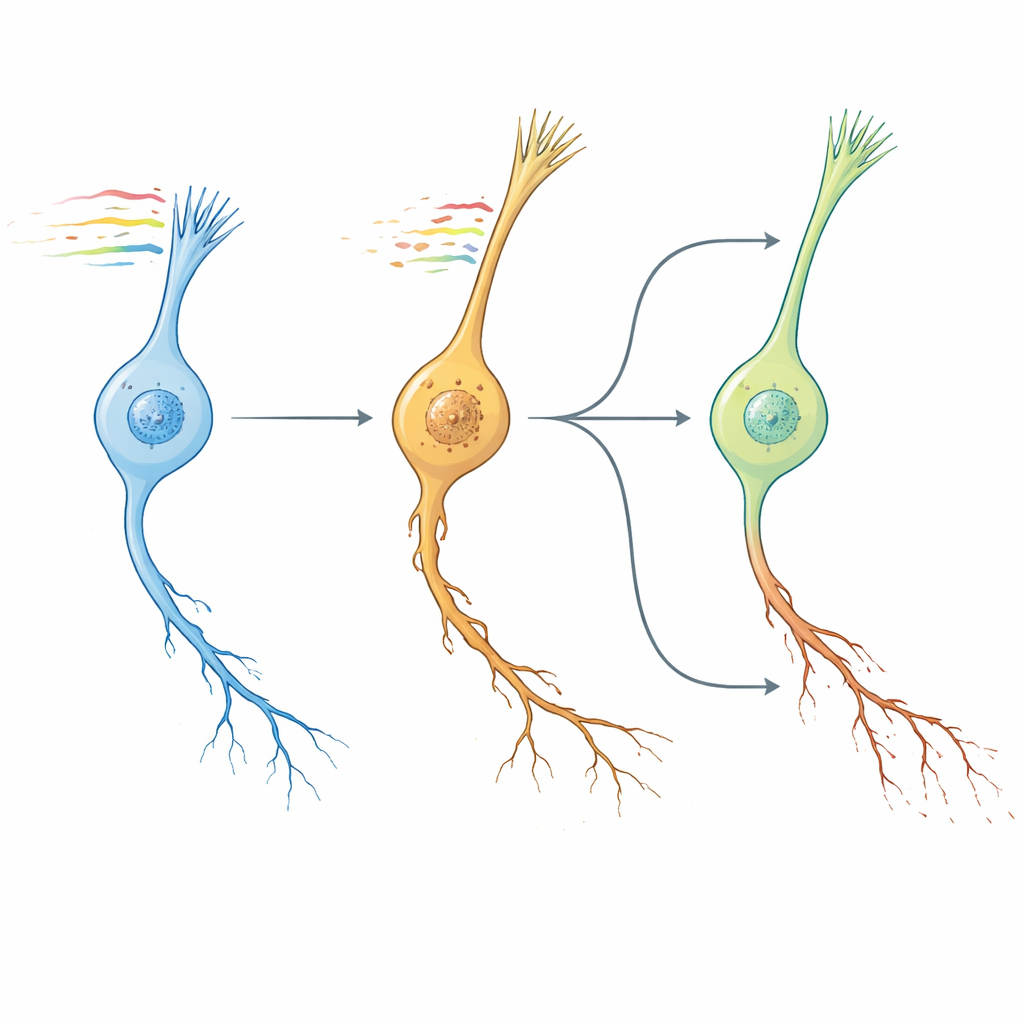
Часы червя, мозги человека и кандидаты в лекарства
Далее авторы поинтересовались, напоминает ли модель старения нейронов у червя старение мозга у млекопитающих. Сравнивая изменения на уровне путей среди консервативных генов, они обнаружили, что транскриптомная сигнатура «NeuronAge» у C. elegans тесно группируется с траекториями старения из нескольких областей мозга мышей и человека, тогда как известные геропротективные вмешательства — такие как факторы молодости в крови, физические упражнения и диетические соединения — демонстрировали противоположные паттерны. Воспользовавшись этой консервацией, они обратились к большой базе данных человеческих клеточных линий, чтобы в силу искать малые молекулы, эффекты которых противодействуют или имитируют NeuronAge. Соединения, чьи профили противоречили NeuronAge, были помечены как потенциальные нейропротекторы; те, которые подкрепляли его, — как потенциальные нейротоксины. Экспериментальные испытания на червях подтвердили несколько предсказаний. Растительный метаболит сирингиновая кислота и препарат ваноксерин оба уменьшали дегенерацию в быстро стареющих нейронах, не повреждая молодые, тогда как агенты вроде Bay K8644 и WAY-100635 усугубляли повреждения нейритов и нарушали поведение. Даже ресвератрол, часто рекламируемый как защитный, в этой системе проявил про-стареющий эффект и увеличивал нейрональную патологию.
Что это значит для здоровья мозга
По сути, эта работа показывает, что даже внутри одной нервной системы разные типы нейронов стареют с разной скоростью, и что эти внутренние часы предсказывают, какие клетки первым подвергнутся дегенерации и утратят функцию. Сенсорные нейроны, контактирующие с внешней средой и обладающие высокой продукцией белка, кажутся особенно хрупкими. Связав нейронно-специфическое старение с консервативными путями экспрессии генов, исследование предлагает путь для переноса знаний от простого червя к человеческому мозгу. Не менее важно то, что показано: транскриптомные сигнатуры старения могут служить мощным фильтром для выявления молекул, которые замедляют или ускоряют нейродегенерацию. Хотя предстоит ещё много работы, прежде чем эти кандидаты смогут быть рассмотрены для терапии у человека, подход указывает на будущее, в котором мы сможем не только измерять биологический возраст отдельных типов нейронов, но и рационально разрабатывать вмешательства, чтобы поддерживать их молодость как можно дольше.
Цитирование: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Ключевые слова: старение нейронов, нейродегенерация, синтез белка, Caenorhabditis elegans, нейропротекция