Clear Sky Science · nl
Verouderingsklokken geven weer welke neuronentypes kwetsbaar of veerkrachtig zijn voor neurodegeneratie en identificeren neuroprotectieve interventies
Waarom sommige hersencellen sneller verouderen dan andere
Waarom verwelken sommige hersencellen vroeg in het leven terwijl andere tientallen jaren robuust blijven? Deze vraag staat centraal bij veel ouderdomsgerelateerde aandoeningen, van de ziekte van Alzheimer tot Parkinson. In deze studie gebruikten onderzoekers een klein rondwormpje, Caenorhabditis elegans, waarvan het volledige zenuwstelsel cel voor cel in kaart is gebracht, om te onderzoeken of verschillende neuronentypes hun eigen “biologische leeftijden” hebben en of die leeftijden voorspellen welke cellen zullen degenereren. Hun werk geeft niet alleen de kwetsbare neuronentypes en een moleculair proces aan dat hun achteruitgang versnelt, maar identificeert ook kleine moleculen die neuronale veroudering kunnen vertragen of versnellen — aanwijzingen die mogelijk ook op het menselijk brein toepasbaar zijn.
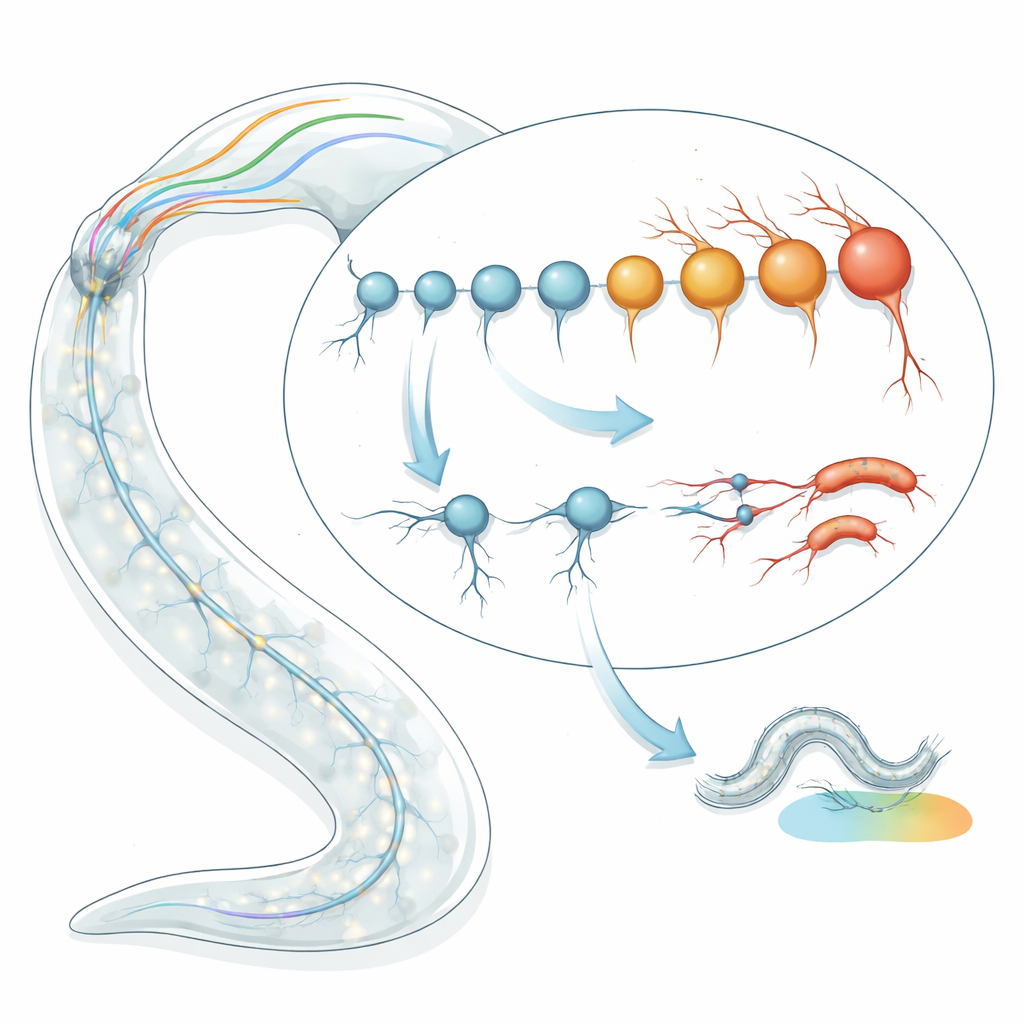
De leeftijd van individuele zenuwcellen timen
Het team begon met het toepassen van transcriptomische “verouderingsklokken” op afzonderlijke neuronentypes in C. elegans. In plaats van naar de leeftijd van de worm in dagen te kijken, onderzochten ze patronen van genactiviteit om de biologische leeftijd van elk celtype te schatten. Met twee onafhankelijke klokmodellen — één gebaseerd op karakteristieke verouderings-genhandtekeningen en een andere die vastlegt hoe willekeurige veranderingen in de loop van de tijd zich ophopen — analyseerden ze RNA-sequencinggegevens voor 128 goed gedefinieerde neuronentypes in laat larvale en jonge volwassen wormen. Tot hun verrassing vonden ze bijna een twee- tot viermaal verschil in voorspelde biologische leeftijd tussen neuronen die allemaal dezelfde chronologische leeftijd hadden. Sommige neuronen leken veel “jonger” dan verwacht, terwijl andere voortijdig “oud” leken te zijn, en deze schattingen waren consistent over meerdere datasets en sequencingmethoden.
Van moleculaire leeftijd naar zichtbare schade en verloren gedrag
Om te testen of deze leeftijdsvoorspellingen relevant waren in levende wormen, volgden de onderzoekers de fysieke toestand van geselecteerde neuronen in de tijd met behulp van fluorescerende markers. Neuronen die als biologisch jong werden voorspeld (zoals I2, OLL en PHC) vertoonden slechts milde structurele schade bij een minderheid van de dieren naarmate de wormen ouder werden. In scherp contrast vertoonden neuronen die als oud werden voorspeld (waaronder ASI, ASJ en ASK) al tekenen van achteruitgang bij bijna de helft van de late larven, oplopend tot ongeveer 90% binnen een week van volwassenheid. De schade manifesteerde zich als kleine zwellingen en uitgroeiingen langs de zenuwvezels en nam ongeveer willekeurig toe langs elk neuriet, wat overeenkomt met een stochastisch verouderingsproces in plaats van een vast ontwikkelingsprogramma. Vroege structurele achteruitgang vertaalde zich ook in echte gedragsdeficits: in circuits waar één neuronentype een specifieke taak beheerst, kwam degeneratie van dat neuron sterk overeen met falen in het vermijden van pathogenen of in leergedrag gebaseerd op zout.
Waarom blootgestelde sensorische neuronen extra risico lopen
Door schattingen van biologische leeftijd op het volledige connectoom van de worm te projecteren, ontstond een opvallend patroon. De oudste neuronen clusterden onder gecilieerde sensorische cellen in het hoofd, met name amphid-neuronen waarvan de cilia direct aan de omgeving blootgesteld zijn. Deze cellen detecteren chemicaliën, geuren en andere signalen en zijn rijk voorzien van neuropeptiden en receptoren. Over neuronentypes heen correleerde een hoger aantal tot expressie komende neuropeptiden en receptoren met een oudere biologische leeftijd, terwijl het absolute aantal synapsen dat niet deed. Gecilieerde neuronen waarvan de sensorische uiteinden uitpuilen naar de buitenwereld waren het meest verouderd, wat suggereert dat zowel blootstelling aan de omgeving als een zware signaalbelasting hen vatbaarder maakt voor vroege achteruitgang. Dit sluit aan bij menselijke neurologie, waar in de reuksystemen omgevingsblootgestelde, gecilieerde neuronen tot de eerste behoren die degenereren bij de ziekte van Alzheimer.
EIwitproductie als aandrijver — en als aangrijpingspunt — van veroudering
Om mechanismen achter deze leeftijdsverschillen te achterhalen, groeperen de onderzoekers neuronen op biologische leeftijd en onderzochten genexpressietrends. Ze vonden dat processen gerelateerd aan ribosoombiogenese, eiwitsynthese en nucleolaire functie verrijkt waren in oudere neuronen, samen met veranderingen in synaptische en neuropeptide-signaleringsgenen. Dit duidde op intensieve eiwitproductie als een mogelijke last die neuronaal slijtageproces versnelt. De onderzoekers testten vervolgens een bescheiden dosis cycloheximide, een verbinding die translatie gedeeltelijk vertraagt. In snel verouderende neuronen verminderde deze milde remming aanzienlijk de structurele schade en behield het de prestaties in een zout-leertaak, met beschermende effecten die zelfs aanhielden nadat de behandeling was gestopt. Langzaam verouderende neuronen waren daarentegen grotendeels onaangetast. Deze resultaten koppelen een hoge translatiebelasting aan neuronspecifieke kwetsbaarheid en tonen aan dat het terugschakelen van eiwitsynthese structurele en functionele integriteit in risiconeuronen kan herstellen.
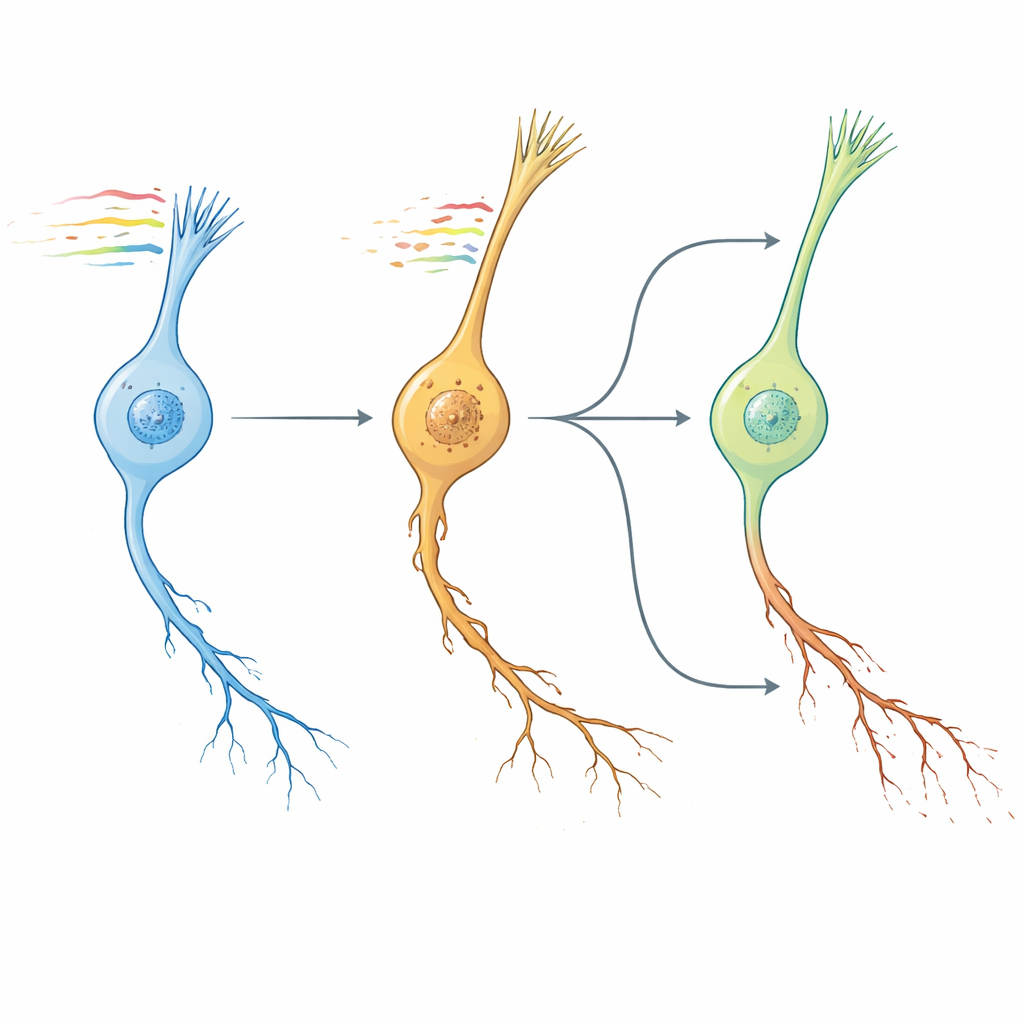
Wormklokken, menselijke hersenen en medicijnkandidaten
Vervolgens onderzochten de auteurs of het verouderingspatroon van wormneuronen leek op hersenveroudering bij zoogdieren. Door pathway-niveau veranderingen te vergelijken over geconserveerde genen, vonden ze dat de transcriptomische “NeuronAge”-handtekening in C. elegans nauw clustert met verouderingstrajecten uit meerdere muis- en menselijke hersenregio’s, terwijl bekende geroprotectieve interventies — zoals factoren uit jong bloed, lichaamsbeweging en dieetgerelateerde verbindingen — tegengestelde patronen vertoonden. Gebruikmakend van deze conservering richtten ze zich op een groot humaan cellijnresource om in silico te zoeken naar kleine moleculen waarvan de effecten NeuronAge tegengaan of nabootsen. Verbindingen met profielen die NeuronAge tegenwerkten werden aangeduid als potentiële neuroprotectoren; diegene die het versterkten als mogelijke neurotoxines. Experimentele tests in wormen valideerden meerdere voorspellingen. Het plantaardige metaboliet syringinezuur en het geneesmiddel vanoxerine verminderden beide degeneratie in snel verouderende neuronen zonder jonge neuronen te schaden, terwijl middelen zoals Bay K8644 en WAY-100635 neurietschade verergerden en gedrag aantastten. Zelfs resveratrol, vaak geroemd als beschermend, bleek in dit systeem pro-verouderend en verhoogde neuronale pathologie.
Wat dit betekent voor hersengezondheid
In wezen toont dit werk aan dat, zelfs binnen één zenuwstelsel, verschillende neuronentypes met verschillende snelheden door veroudering gaan, en dat deze interne klokken voorspellen welke cellen het eerst zullen degenereren en hun functie verliezen. Sensorische neuronen die zijn blootgesteld aan de buitenwereld en die hoge niveaus van eiwitproductie hebben, blijken bijzonder kwetsbaar. Door neuronspecifieke veroudering te koppelen aan geconserveerde genexpressiepatronen, biedt de studie een manier om inzichten uit een eenvoudig wormmodel naar het menselijk brein te vertalen. Even belangrijk is dat het aantoont dat transcriptomische verouderingshandtekeningen gebruikt kunnen worden als een krachtig filter om moleculen te identificeren die neurodegeneratie vertragen of versnellen. Hoewel er nog veel werk te doen is voordat deze kandidaten voor menselijke therapie in aanmerking komen, wijst de benadering op een toekomst waarin we niet alleen de biologische leeftijd van individuele neuronentypes kunnen meten, maar ook op rationele wijze interventies kunnen ontwerpen om ze langer jong te houden.
Bronvermelding: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Trefwoorden: neurale veroudering, neurodegeneratie, eiwitsynthese, Caenorhabditis elegans, neuroprotectie